Սպիտակուցներ

Սպիտակուցներ (պրոտեիններ, պոլիպեպտիդներ[Ն 1]), բարձրամոլեկուլային օրգանական միացություններ, որոնք կազմված են պեպտիդային կապով իրար միացած ալֆա-ամինաթթուներից։ Կենդանի օրգանիզմներում սպիտակուցների ամինաթթվային հաջորդականությունը որոշվում է գենետիկական կոդով, սինթեզելիս հիմնականում օգտագործվում է ամինաթթուների 20 տեսակ։ Ամինաթթուների տարբեր հաջորդականություններն առաջացնում են տարբեր հատկություններով օժտված սպիտակուցներ։ Ամինաթթվի մնացորդները սպիտակուցի կազմում կարող են ենթարկվել նաև հետատրանսլյացիոն ձևափոխությունների, ինչպես բջջում ֆունկցիայի իրականացման ժամանակ, այնպես էլ մինչև ֆունկցիայի իրականացումը։ Հաճախ կենդանի օրգանիզմներում սպիտակուցի երկու տարբեր մոլեկուլներ միանում են միմյանց՝ առաջացնելով բարդ սպիտակուցային կոմպլեքսներ, ինչպիսին, օրինակ, ֆոտոսինթեզի սպիտակուցային կոմպլեքսն է։
Կենդանի օրգանիզմներում սպիտակուցների գործառույթները բազմազան են։ Սպիտակուց ֆերմենտները կատալիզում են օրգանիզմում ընթացող կենսաքիմիական ռեակցիաները և կարևոր դեր են խաղում նյութափոխանակության մեջ։ Որոշ սպիտակուցներ կատարում են կառուցվածքային և մեխանիկական գործառույթ՝ առաջացնելով բջջային կմախքը։ Սպիտակուցները կարևոր դեր են կատարում նաև բջիջների ազդանշանային համակարգում, իմունային պատասխանում և բջջային ցիկլում։
Սպիտակուցները մարդու և կենդանիների սննդի կարևոր մասն են կազմում (միս, թռչնամիս, ձուկ, կաթ, ընկուզեղեն, ընդավոր, հացահատիկային բույսեր), քանի որ այս օրգանիզմներում սինթեզվում է միայն անհրաժեշտ սպիտակուցների մի մասը։ Մարսողության գործընթացում սննդի մեջ պարունակվող սպիտակուցները քայքայվում են մինչև ամինաթթուներ, որոնք հետագայում օգտագործվում են սպիտակուցի կենսասինթեզում՝ օրգանիզմի սեփական սպիտակուցների սինթեզի համար, կամ քայքայման գործընթացը շարունակվում է էներգիա ստանալու համար։
Սեքվենավորման մեթոդով առաջին սպիտակուցի՝ ինսուլինի ամինաթթվային հաջորդականության բացահայտման համար Ֆրեդերիկ Սենգերը 1958 թվականին ստացավ Նոբելյան մրցանակ քիմիայի բնագավառում։ Ռենտգենային ճառագայթների դիֆրակցիայի մեթոդով 1950-ական թվականներին առաջին անգամ ստացվել է հեմոգլոբինի և միոգլոբինի եռաչափ կառույցները Մաքս Պեուցի և Ջոն Քենդրյուի կողմից համապատասխանաբար, որոնց համար 1962 թվականին նրանք ևս ստացել են քիմիայի բնագավառում Նոբելյան մրցանակ[1][2]։
Ուսումնասիրման պատմություն[խմբագրել | խմբագրել կոդը]

Սպիտակուցները՝ որպես առանձին կենսաբանական մոլեկուլների դաս, առանձնացվել են 18-րդ դարում ֆրանսիացի քիմիկոս Անտուան դե Ֆուրկուրի և այլ գիտնականների կողմից, ովքեր հայտնաբերեցին սպիտակուցների՝ թթվի կամ ջերմության ազդեցությամբ կոագուլացվելու (դենատուրացվելու) ընդունակությունը։ Այդ ժամանակ ուսումնասիրվեցին ալբումինը կամ ձվի սպիտակուցի սպիտակուցը, ֆիբրինը՝ արյան սպիտակուցը և գլյուտենը՝ հացահատիկներից։
19-րդ դարի սկզբում արդեն որոշ տեղեկություններ կային սպիտակուցի տարրական կառուցվածքի մասին։ Հայտնի էր, որ հիրդրոլիզվելիս սպիտակուցներն առաջացնում են ամինաթթուներ։ Այդ ամինաթթուներից որոշները, օրինակ՝ գլիցինը և լեյցինը, մանրամասն նկարագրվել են։ Հոլանդացի գիտնական Գերարդ Մուլդերը սպիտակուցների քիմիական կազմի հիման վրա ենթադրեց, որ համարյա բոլոր սպիտակուցներն ունեն նման էմպիրիկ բանաձև։ 1836 թվականին Մուլդերը առաջ քաշեց սպիտակուցների կառուցվածքի առաջին մոդելը։ Հիմնվելով ռադիկալների տեսության վրա՝ նա որոշ ճշգրտումներից հետո եզրահանգեց, որ սպիտակուցի տարրական կառուցվածքային միավորը ունի հետևյալ բաղադրությունը՝ C40H62N10O12։ Այս միավորը Մուլդերն անվանեց «պրոտեին» (Pr) (հունարեն՝ πρῶτος, պրոտոս՝ առաջին,առաջնային), իսկ տեսությունը՝ «պրոտեինի տեսություն»[3]։ Պրոտեին տերմինը առաջարկել էր դեռ շվեդ քիմիկոս Յակոբ Բերցելիուսը[4]։ Մուլդերի պատկերացումների համաձայն՝ յուրաքանչյուր սպիտակուց կազմված է մի քանի պրոտեինային միավորներից, ֆոսֆորից և ծծբից։ Օրինակ՝ ֆիբրինի բանաձևը նա առաջարկում էր գրել այսպես՝ 10PrSP: Մուլդերը ուսումնասիրել է նաև սպիտակուցների քայքայման պրոդուկտները՝ ամինաթթուները, և տվել լեյցինի մոլեկուլային զանգվածը սխալի փոքր տոկոսով՝ 131 դալտոն։ Մինչև 1850-ական թվականների ավարտը պրոտեինի տեսությունը լայնորեն տարածված էր, սակայն նոր տվյալների կուտակման հետ այն սկսեց ենթարկվել քննադատության։
19-րդ դարի վերջում արդեն ուսումնասիրվել էին սպիտակուցի կազմի մեջ մտնող ամինաթթուների մեծ մասը։ 1880-ական թվականների վերջում ռուս գիտնական Ալեքսանդր Դանիլևսկին հայտնաբերեց սպիտակուցի մոլեկուլում (CO-NH) պեպտիդային խմբերի առկայությունը[5][6]։ 1894 թվականին գերմանացի ֆիզիոլոգ Ալբրեխտ Կոսելը առաջ քաշեց մի տեսություն, որով փաստեց, որ հենց ամինաթթուներն են սպիտակուցների կառուցվածքային միավորները[7]։ 20-րդ դարի սկզբում գերմանացի քիմիկոս Էմիլ Ֆիշերը փորձնականորեն ապացուցեց, որ սպիտակուցները կազմված են ամինաթթուների մնացորդներից, որոնք միմյանց միացած են պեպտիդային կապերով։ Նա էլ հենց իրականացրեց սպիտակուցի ամինաթթվային հաջորդականության առաջին վերլուծությունը և բացատրեց պրոտեոլիզի երևույթը։
Օրգանիզմում սպիտակուցների ունեցած կենտրոնական դերը անբացահայտ մնաց մինչև 1926 թվականը, երբ ամերիկացի քիմիկոս Ջեյմս Սամները (Քիմիայի Նոբելյան մրցանակի դափնեկիր) ցույց տվեց, որ ուրեազ ֆերմենտը սպիտակուց է[8]։

Մաքուր սպիտակուցների առանձնացման բարդությունը դժվարացնում էր այդ բնագավառում ուսումնասիրությունների ընթացքը։ Սպիտակուցների առաջին ուսումնասիրությունները տարվել են այն պոլիպեպտիդների վրա, որոնք հեշտությամբ և մեծ քանակով մաքրվում էին՝ արյան սպիտակուցներ, ձվի սպիտակուց, տարբեր թույներ, խոշոր եղջերավոր անասունների մարսողական ֆերմենտներ։ 1950-ականների վերջում Armour Hot Dog Co. ընկերությունը կարողացավ առանձնացնել ցուլի ենթաստամոքսային գեղձի ռիբոնուկլեազ A ֆերմենտը, որը շատ հետազոտությունների օբյեկտ դարձավ։
Այն գաղափարը, թե սպիտակուցի երկրորդային կառուցվածքը ամինաթթվային հիմքերի միջև առաջացող ջրածնային կապերի արդյունք է, առաջ է քաշել Ուիլյամ Աստբերին 1933 թվականին, բայց երկրորդային կառուցվածքը բացատրած առաջին գիտնականը Լայնուս Պոլինգն է։ Հետագայում Ուոլտեր Կաուզմանը, հիմնվելով Կայ Լինդերստրյոմ-Լանգանի աշխատանքների վրա, բացատրեց սպիտակուցի երրորդային կառուցվածքում առաջացող կապերի առաջացման մեխանիզմները։ 1940-50-ական թվականներին Ֆրեդերիկ Սենգերը մշակեց սպիտակուցների սեքվենավորման մեթոդ, որի միջոցով 1955 թվականին նա բացահայտեց ինսուլինի երկու շղթաների ամինաթթվային հաջորդականությունները[9][10][11]՝ ապացուցելով, որ սպիտակուցները ամինաթթուների գծային, այլ ոչ թե ճյուղավորված պոլիմերներ են։ Խորհրդային գիտնականների կողմից սեքվենավորված առաջին սպիտակուցը եղել է ասպարտատամինոտրանսֆերազ ֆերմենտը (1972)[12][13].
Սպիտակուցների առաջին տարածական կառույցները ստացվել են ռենտգենային ճառագայթների դիֆրակցիայի մեթոդով և հայտնի են դարձել 1950-60-ական թվականներին, իսկ միջուկային մագնիսական ռեզոնանսի մեթոդով ստացված կառույցները՝ 1980-ականներին։ 2012 թվականին «Սպիտակուցների շտեմարանը» (Protein Data Bank) պարունակում էր սպիտակուցների ավելի քան 87000 կառույցներ[14]։
21-րդ դարում սպիտակուցների հետազոտությունները նոր թափ ստացան, սկսեցին ուսումնասիրվել ոչ միայն առանձին սպիտակուցները, այլ տարբեր բջիջների, հյուսվածքների և օրգանիզմների մեծ քանակով սպիտակուցների քանակական և հետտրանսլյացիոն ձևափոխությունները։ Կենսինֆորմատիկայի մեթոդով հնարավոր դարձավ մշակել ոչ միայն ռենտգենակառուցվածքային անալիզի տվյալները, այլև կանխորոշել սպիտակուցի հնարավոր կառուցվածքը՝ հիմնվելով նրա ամինաթթուների հաջորդականության վրա։ Ներկայումս խոշոր սպիտակուցների կոմպլեքսների կրիոէլեկտրոնային ուսումնասիրությունը և համակարգչային ծրագրերի օգնությամբ սպիտակուցների դոմենների կառուցվածքի կանխորոշումն ունեն համարյա ատոմային մակարդակի ճշտություն[15]։
Հատկություններ[խմբագրել | խմբագրել կոդը]
Չափսեր[խմբագրել | խմբագրել կոդը]

Սպիտակուցի չափսը կարող է չափվել ամինաթթվային մնացորդների քանակով կամ դալտոններով (մոլեկուլային զանգված), բայց մոլեկուլների հարաբերական մեծության պատճառով այն արտահայտվում է կիլոդալտոններով՝ կԴա։ Խմորասնկերի սպիտակուցները միջինում կազմված են 466 ամինաթթուների մնացորդներից և ունեն 53 կԴա մոլեկուլային զանգված։ Ներկայումս հայտնի ամենամեծ սպիտակուցներից մեկը՝ տիտինը, մտնում է մկանի սարկոմերների կազմության մեջ։ Այս սպիտակուցի իզոմորֆ ձևերն ունեն 3000-3700 կԴա մեծություն։ Մարդու ձկնաձև մկանի (լատին․՝ soleus) տիտին սպիտակուցը կազմված է 38 138 ամինաթթուներից[16]։
Սպիտակուցների մոլեկուլային զանգվածի որոշման համար օգտագործվում են գել-ֆիլտրացիայի, պոլիակրիլամիդային գելում էլեկտրոֆորեզի, մաս-սպեկտորոսկոպիկական անալիզի, սեդիմենտացիոն անալիզի և այլ մեթոդներ[17]։
Ֆիզիկաքիմիական հատկություններ[խմբագրել | խմբագրել կոդը]
Ամֆոտերություն[խմբագրել | խմբագրել կոդը]

Սպիտակուցներն օժտված են ամֆոտերությամբ. արտաքին պայմաններից կախված՝ կարող են ցուցաբերել թթվային կամ հիմնային հատկություններ։ Սպիտակուցների կազմում կան մի քանի տեսակի ֆունկցիոնալ խմբեր, որոնք ջրային միջավայրում իոնացվում են, դրանք են թթու ամինաթթուների կողմնային կարբօքսիլ խմբերը (ասպարգինաթթու, գլուտամինաթթու) և ազոտ պարունակող կողմնային շղթաների ամինաթթուները (առաջին հերթին լիզինի ε-ամինոխումբը և արգինինի ամիդային CNH(NH2 մնացորդը, ավելի քիչ՝ հիստիդինի իմիդազոլային մնացորդը։ Յուրաքանչյուր սպիտակուց բնութագրվում է իզոէլեկտրական կետով (pI), որը միջավայրի թթվայնության (pH-ի) արժեքն է այն միջավայրում, որտեղ սպիտակուցի մոլեկուլի գումարային էլեկտրական լիցքը զրո է, այսինքն՝ մոլեկուլը չի տեղափոխվում էլեկտրական դաշտում (օրինակ՝ էլեկտրոֆորեզի ժամանակ)։ Իզոէլեկտրական կետում սպիտակուցի հիդրատացիան և լուծելիությունը ունեն նվազագույն արժեքը։ pI-ի մեծությունը կախված է ամինաթթուների հիմնական թթվային և հիմնային խմբերի հարաբերությունից։ Մեծ թվով թթվային մնացորդներ պարունակող սպիտակուցների իզոէլեկտրական կետը գտնվում է թթվային հատվածում, հիմնային մնացորդների դեպքում՝ հիմնային հատվածում։ pI-ի արժեքը կարող է փոփոխվել՝ իոնային ուժից և բուֆերային լուծույթից կախված, քանի որ չեզոք աղերն ազդում են սպիտակուցի ֆունկցիոնալ խմբերի իոնիզացման վրա։ pI-ը կարելի է որոշել թթվահիմնային տիտրավորման կամ իզոէլեկտրոֆոկուսավորման մեթոդներով[17].
pI-ն ընդհանուր առմամբ կախված է սպիտակուցի կատարած գործառույթից. ողնաշարավորների շատ հյուսվածքային սպիտակուցների իզոէլեկտրական կետը ընկած է 5,5-7,0-ի սահմաններում, սակայն որոշ դեպքերում այն կարող է ընդունել խիստ տարբերվող արժեք, օրինակ՝ պեպսինի՝ ստամոքսահյութի ֆերմենտի դեպքում pI ~ 1[18], իսկ սալմինի՝ սաղմոնի սերմնահյութի պրոտամինի դեպքում՝ pI ~ 12՝ արգինինի մեծ պարունակության հաշվին։ Նուկլեինաթթուներին ֆոսֆատային խմբի էլեկտրոստատիկական փոխհարաբերության հաշվին միացող սպիտակուցները, հաճախ հիմնական սպիտակուցներն են։ Այսպիսի սպիտակուցներ են հիստոններն ու պրոտամինները։
Լուծելիություն[խմբագրել | խմբագրել կոդը]
Սպիտակուցները տարբերվում են ըստ ջրում լուծելիության։ Ջրում լուծվող սպիտակուցներն անվանում են ալբումիններ, որոնցից են, օրինակ, արյան և կաթի սպիտակուցները։ Ջրում չլուծվող սպիտակուցներից կամ սկլերոպրոտեիններից են, օրինակ, կերատինը, ֆիբրոինը, որը մտնում է մետաքսաթելի և սարդոստայնի բաղադրության մեջ[19]։ Սպիտակուցի լուծելիությունը պայմանավորված է ոչ միայն կառուցվածքով, այլ նաև արտաքին գործոններով՝ լուծիչի բնույթով, իոնային ուժով, լուծույթի pH-ով[17]։
Սպիտակուցները լինում են նաև հիդրոֆիլ (ջուր ձգող) և հիդրֆոբ (ջուր վանող)։ Հիդրոֆիլ սպիտակուցներ են ցիտոպլազմայի, կորիզի, միջբջջային նյութի սպիտակուցների մեծ մասը, այդ թվում կերատինը և ֆիբրիոինը։ Հիդրոֆոբ սպիտակուցներ են կենսաբանական թաղանթի կազմի մեջ մտնող սպիտակուցները, որոնք փոխհարաբերության մեջ են մտած թաղանթի հիրդոֆոբ լիպիդների հետ[20] (այս սպիտակուցները, որպես կանոն, ունեն նաև հիդրոֆիլ հատվածներ)։
Բնափոխում[խմբագրել | խմբագրել կոդը]

Սպիտակուցի բնափոխումը կամ դենատուրացիան երկրորդային, երրորդային կամ չորրորդային կառուցվածքի կորստի հետ կապված ցանկացած փոփոխությունն է, որը հանգեցնում է սպիտակուցի ակտիվության և/կամ ֆիզիկաքիմիական հատկությունների փոփոխությանը։ Որպես կանոն, սպիտակուցները օրգանիզմում բավականին կայուն են և հարմարված օրգանիզմի ներքին պայմաններին[8]։ Այս պայմանների կտրուկ փոփոխությունը բերում է սպիտակուցի բնափոխմանը։ Բնափոխման պատճառները կարող են լինել մեխանիկական (կտրուկ տեղափոխում, թափահարում), ֆիզիկական (տաքացում, սառեցում, ուլտրաձայն, ճառագայթում) և քիմիական (թթուներ և հիմքեր, մակերեսային ակտիվ նյութեր, միզանյութ)[17]։
Սպիտակուցի բնափոխումը կարող է լինել նաև ամբողջական կամ մասնակի, դարձելի և անդարձելի։ Անդարձելի բնափոխման ամենատարածված օրինակը ձվի սպիտակուցի բնափոխումն է բարձր ջերմաստիճանի ազդեցությամբ։ Թափանցիկ օվալբումին սպիտակուցը խտանում է, դառնում անլուծելի և անթափանց։ Բնափոխումը որոշ դեպքերում դարձելի է, ինչպես, օրինակ, ջրում լուծվող սպիտակուցների՝ ամոնիումի աղերով նստեցման և մաքրման մեջ կիրառման ժամանակ[21]։
Կառուցվածք[խմբագրել | խմբագրել կոդը]

Սպիտակուցի մոլեկուլները գծային պոլիմերներ են, որոնք կազմված են α-L-ամինաթթուների մնացորդներից (մոնոմերներ)։ Սպիտակուցի կազմի մեջ կարող են մտնել նաև ձևափոխված ամինաթթվային մնացորդներ և ոչ ամինաթթվային ծագում ունեցող բաղադրիչներ։ Սպիտակուցների կազմում ամինաթթուների նշանակման համար օգտագործում են մեկ կամ երեք տառից բաղկացած կրճատումներ։ Քանի որ կենդանի օրգանիզմների կազմի մեջ մտնող սպիտակուցների մեծամասնությունը կազմված են 20 ամինաթթուներից, այս պատճառով կարող է թվալ, թե սպիտակուցների հնարավոր թիվը փոքր է և սահմանափակ։ Իրականում, օրինակ՝ հինգ ամինաթթվային մնացորդ պարունակող սպիտակուցի մոլեկուլների հնարավոր թիվը գերազանցում է 3 միլիոնը, 100 ամինաթթվային մնացորդի դեպքում տարբերակների թիվը 10130-ից ավելի է։
2-10 ամինաթթվային մնացորդից կազմված մոլեկուլները հաճախ անվանվում են պեպտիդներ, իսկ ավելի բարդ պոլիմերները՝ սպիտակուցներ։ Այս բաժանումը, սակայն, պայմանական է։
Սպիտակուցի կազմավորման ժամանակ մի ամինաթթվի α-կարբօքսիլ խմբի (-COOH) և մյուսի α-ամինոխմբի (-NH2) միջև առաջանում է պեպտիդային կապ։ Սպիտակուցի ծայրերն կոչվում են N- և C- ծայրեր, ինչը պայմանավորված է նրանով, թե որ ֆունկցիոնալ խմբերն են ազատ՝ -NH2-ը, թե -COOH-ը։ Ռիբոսոմի վրա սպիտակուցի կենսասինթեզի ժամանակ առաջին N-ծայրային ամինաթթվային մնացորդը սովորաբար մեթիոնինն է, մյուս ամինաթթուները միանում են նախորդի C- ծայրին։
Կազմավորման մակարդակներ[խմբագրել | խմբագրել կոդը]

Լինդեստրյոմ-Լանգը առաջարկել է առանձնացնել սպիտակուցի կազմավորման 4 մակարդակ՝ առաջնային, երկրորդային, երրորդային և չորրորդային կառուցվածքներ։ Չնայած այսպիսի բաժանումը որոշ դեպքերում հնացած է, այն շարունակվում է լայնորեն օգտագործվել[3]։ Պոլիպեպտիդի առաջնային կառուցվածքը (ամինաթթվային մնացորդների հաջորդականությունը) որոշվում է գենով և գենետիկական գաղտնագրով, ավելի բարձր մակարդակները ձևավորվում են սպիտակուցների ֆոլդինգի ընթացքում (անգլ.՝ fold՝ ծալել)[22]։ Չնայած որ սպիտակուցի տարածական կառուցվածը որոշվում է հիմնականում ամինաթթվային հաջորդականությամբ, այն բավական շարժուն է և կարող է պայմանավորվել արտաքին միջավայրի պայմաններով։ Այս պատճառով արտաքին միջավայրում սպիտակուցը ընդունում է էներգետիկ տեսակետից ավելի ձեռնտու տարածական կառուցվածք[3]։
Առաջնային կառուցվածք[խմբագրել | խմբագրել կոդը]

Առաջնային կառուցվածքը պոլիպեպտիդային շղթայում ամինաթթվային մնացորդների հաջորդականությունն է։ Սպիտակուցի առաջնային կառուցվածքը, որպես կանոն, նկարագրում են մեկ կամ երեք տառերից բաղկացած նշանակումների օգտագործմամբ։
Առաջնային կառուցվածքի կարևոր հատկություններից է կոնսերվատիվ միտումը, որը որոշակի գործառույթ ունեցող ամինաթթվային մնացորդների խմբերի կայուն ամբողջությունն է և հանդիպում է շատ սպիտակուցներում։ Կոնսերվատիվ միտումները պահպանվում են տեսակների էվոլյուցիայի ընթացքում։ Դրանք օգտագործվում են անհայտ սպիտակուցի ֆունկցիան պարզելու համար[23]։ Սպիտակուցների ամինաթթվային կազմի համանմանությամբ կարելի է պարզել տաքսոնների միջև գոյություն ունեցող էվոլյուցիոն կապերը։
Սպիտակուցի առաջնային կառուցվածքը հնարավոր է որոշել սպիտակուցների սեքվենավորման կամ մՌՆԹ-ի առաջնային կառուցվածքի միջոցով՝ օգտագործելով գենետիկական գաղտնագիրը։
Երկրորդային կառուցվածք[խմբագրել | խմբագրել կոդը]
Երկրորդային կառուցվածքը սպիտակուցի պոլիպեպտիդային շղթայի հատվածների տեղային դասավորությունն է, որը կայունացվում է ջրածնային կապերի միջոցով։ Ստորև ներկայացված են սպիտակուցի երկրորդային կառուցվածքի տիպերը[22]՝
- α-պարույր՝ մոլեկուլի երկար առանցքի շուրջը խիտ դասավորված են պարույրները, մեկ պարույրում կա 3,6 ամինաթթվային մնացորդ, մեկ քայլը 0,54 նմ է (մեկ ամինաթթվային մնացորդը՝ 0,15 նմ)[24]։ Պարույրը պահպանում է իր ձևը պեպտիդային խմբերի H և O ատոմների միջև առաջացող պեպտիդային կապերով։ α-պարույրը կարող է լինել աջ և ձախ պարուրված, սպիտակուցներում գերակշռում է աջ պարուրված տարբերակը։ Պարույրը քանդվում է գլուտամինաթթվի, լիզինի, արգինինի էլեկտրոստատիկ փոխհարաբերությունը։ Ասպարգինի, սերինի, թրեոնինի և լեյցինի մնացորդները միմյանց մոտ դասավորվելիս կարող են խանգարել պարույրի ձևավորմանը, պրոլինի մնացորդն առաջացնում է շղթայի ծռում, որը նույնպես քանդում է α-պարույրը։
- β-պարույր (շարժական շերտեր)՝ մի քանի կեռմանաձև պոլիպեպտիդային շղթաներ, որոնցում ջրածնային կապեր առաջանում են հադնիպակաց շղթաների կամ միմյանցից հեռու դասավորված ամինաթթվային մնացորդների միջև[25]։ Այս շղթաներն իրենց N-ծայրով ուղղված են հակառակ (հակազուգահեռ կողմնորոշում)։ β-պարույրի առաջացման համար կարևոր կողմնային ամինաթթվային մնացորդներից են գլիցինն ու ալանինը։
- π-պարույր,
- 310-պարույր,
- չկարգավորված հատվածներ։
Երրորդային կառուցվածք[խմբագրել | խմբագրել կոդը]
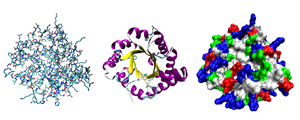
Երրորդային կառուցվածքը պոլիպեպտիդային շղթայի տարածական դասավորությունն է։ Այն կազմված է երկրորդային կառուցվածքի տարրերից, որոնք կայունացվում են տարբեր փոխհարաբերությունների, հատկապես հիդրոֆոբ փոխհարաբերության շնորհիվ։ Կայուն երրորդային կառուցվածքում կան՝
- կովալենտ կապեր ցիստեինի երկու մնացորդների միջև՝ դիսուլֆիդային կապեր,
- իոնային կապեր հանդիպակաց դասավորված ամինաթթվային մնացորդների երկու խմբերի միջև,
- ջրածնային կապեր,
- հիդրոֆոբ փոխհարաբերություն։ Սպիտակուցի մոլեկուլը ջրի հետ փոխհարաբերվելիս ընդունում է այնպիսի կառուցվածք, որտեղ ոչ բևեռային ամինաթթուների կողմնային խմբերը մեկուսանում են ջրային լուծույթից, իսկ բևեռային խմբերը՝ հայտնվում մոլեկուլի մակերեսին։
Սպիտակուցների երրորդային կառուցվածքի ուսումնասիրությունը ցույց է տվել, որ երկրորդային և ատոմային տարածական կառուցվածքների միջև կարելի է առանձնացնել նաև երրորդ մակարդակը՝ կառուցվածքային դրդապատճառը։ Այն որոշվում է սպիտակուցի դոմենի սահմաններում երկրորդային կառուցվածքի տարրերի (α-պարույր և β-պարույր) միմյանց նկատմամբ ունեցած դասավորությամբ։ Սպիտակուցի դոմենը կոմպակտ գլոբուլին է, որը կարող է ինքնուրույն գոյություն ունենալ կամ մտնել ավելի մեծ սպիտակուցի կազմության մեջ։ Պատկերի աջում պատկերված գլոբուլյար սպիտակուցի՝ տրիոզոֆոսֆատիզոմերազի կառուցվածքային դրդապատճառն անվանվում է α/β-գլան։ 8 զուգահեռ դասավորված β-պարույրներն առաջացնում են β-գլան, որն իր հերթին գտնվում է 8 α-պարույրներից կազմված մեկ այլ գլանի ներսում։ Այսպիսի կառուցվածք ունեն սպիտակուցների 10%-ը[26]։
Կառուցվածքային դրդապատճառները հանդիպում են նաև այն սպիտակուցների մոտ, որոնք չունեն ֆունկցիոնալ և էվոլյուցիոն կապեր։ Կառուցվածքային դրդապատճառներն օգտագործվում են սպիտակուցների դասակարգման մեջ, ինչպես, օրինակ, CATH-ը կամ SCOP-ն է[26]։
Սպիտակուցի տարածական կառուցվածքի որոշման համար օգտագործվում են ռենտգենկառուցվածքային անալիզը, միջուկային մագնիսական ռեզոնանսը և մի շարք մանրադիտակային մեթոդներ։
Չորրորդային կառուցվածք[խմբագրել | խմբագրել կոդը]
Չորրորդային կամ ենթամիավորումային, դոմենային կառուցվածքը մեկ սպիտակուցային կոմպլեքսի ներսում տարբեր պոլիպեպտիդային շղթաների փոխադարձ դասավորությունն է։ Չորրորդային կառուցվածքի մեջ մտնող սպիտակուցի մոլեկուլները ռիբոսոմի վրա առաջանում են առանձին-առանձին և միայն սպիտակուցի սինթեզից հետո ձևավորում վերմոլեկուլային չորրորդային կառույցը։ Չորրորդային կառուցվածքի մեջ կարող են մտնել ինչպես նման, այնպես էլ տարբերվող պոլիպեպտիդային շղթաներ։ Չորրորդային կառուցվածքի կայունացմանը մասնակցում են նույն փոխհարաբերությունները, ինչ երրորդայինի դեպքում։ Վերմոլեկուլային այսպիսի սպիտակուցային կառուցվածքները կարող են պարունակել տասնյակ մոլեկուլներ։
Դասակարգումն ըստ կառուցվածքի[խմբագրել | խմբագրել կոդը]
Ըստ ընդհանուր կառուցվածքի՝ սպիտակուցները բաժանվում են երեք խմբերի՝
- Ֆիբրիլյար սպիտակուցներ - առաջացնում են պոլիմերներ, նրանց կառուցվածքը սովորաբար կայուն է, որը պահպանվում է շղթաների միջև առկա փոխհարաբերությունների շնորհիվ։ Ֆիբրիլյար սպիտակուցներն առաջացնում են միկրոթիթեղներ, միկրոխողովակներ, ֆիբրիլներ, պահպանում հյուսվածքների և բջիջների կառուցվածքը տարածության մեջ։ Ֆիբրիլյար սպիտակուցներից են կերատինը և կոլագենը։
- Գլոբուլյար սպիտակուցներ - ջրում լուծվող սպիտակուցներ, մոլեկուլի ձևը փոքրիշատե գնդաձև է։
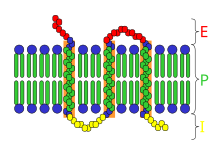
- Թաղանթային սպիտակուցներ - ունեն բջջաթաղանթը հատող դոմեններ, բայց հիմնական մասը ուղղված է դեպի ցիտոպլազմա կամ միջբջջային տարածություն։ Թաղանթային կամ մեմբրանային սպիտակուցները կատարում են ռեցեպտորների դեր, իրականացնում են ազդակի փոխանցումը և ապահովում տարբեր միացությունների միջմեմբրանային տեղափոխությունը։
Պարզ և բարդ սպիտակուցներ[խմբագրել | խմբագրել կոդը]

Բացի պեպտիդային շղթաներից, շատ սպիտակուցների կազմի մեջ կարող են մտնել նաև ոչ ամինաթթվային խմբեր։ Այս առանձնահատկությունը հաշվի առնելով՝ սպիտակուցները բաժանվում են երկու խմբի՝ պարզ և բարդ սպիտակուցներ (պրոտեիդներ)։ Պարզ սպիտակուցները կազմված են միայն պոլիպեպտիդային շղթաներից, բարդ սպիտակուցները պարունակում են նաև ոչ ամինաթթվային կամ պրոսթետիկ խմբեր։ Պրոսթետիկ խմբի բնույթից կախված՝ տարբերում են բարդ սպիտակուցների հետևյալ դասերը[19]՝
- Գլիկոպրոտեինների պրոսթետիկ խումբը կովալենտ կապով միացած ածխաջրերի մնացորդներ են։ Մուկոպոլիսախարարիդային մնացորդներ պարունակող գլիկոպրոտեինները պատկանում են պրոտեոգլիկանների շարքին։ Ածխաջրային մնացորդների հետ կապի առաջացմանը մասնակցում են սերինի կամ թրեոնինի հիդրօքսիլ խմբերը։ Ներկորիզային սպիտակուցների մեծ մասը և հատկապես իմունոգլոբուլինները գլիկոպրոտեիններ են։ Պրոտեոգիլկաններում ածխաջրային մասը կազմում է մոլեկուլի ընդհանուր զանգվածի մոտ 95%-ը, այն ներբջջային կմախքի հիմնական մասն է։
- Լիպոպրոտեինների պրոսթետիկ խումբը ոչ կովալենտ կապով կապված լիպիդներ են։ Արյան մեջ լիպիդների տեղափոխմանը մասնակցում են սպիտակուց-ապոլիպոպրոտեինները՝ կապվելով լիպիդների հետ։
- Մետաղպրոտեիդները պարունակում են դոնոր-ակցեպտորային կապով միացած մետաղի իոններ։ Մետաղպրոտեիդների շարքում կան այնպիսի սպիտակուցներ, որոնք կատարում են դեպոնացնող և տրանսպորտային ֆունկցիաներ (օրինակ՝ երկաթ պարունակող ֆերիտինը, տրանսֆերինը, ֆերմենտներ՝ ցինկ պարունակող՝ կարբոանհիդրազ և այլ սուպերօքսիդդիսմուտազներ, որոնք ակտիվ կենտրոնում պարունակում են պղնձի, մագնեզիումի, երկաթի և այլ մետաղների իոններ։
- Նուկլեոպրոտեիդները պարունակում են ոչ կովալենտ կապով կապված ԴՆԹ կամ ՌՆԹ։ Նուկլեոպրոտեիդներից է քրոմատինը, որից կազմված են քրոմոսոմները։
- Ֆոսֆոպրոտեինների պրոսթետիկ խումբը ոչ կովալենտ կապով կապված ֆոսֆորական թթվի մնացորդն է։ Ֆոսֆատը բարդ եթերային կապ է հաստատում սերինի, թրեոնինի և թիրոզինի հիդրօքսիլ խմբի հետ։ Ֆոսֆոպրոտեին է օրինակ կաթի կազեին սպիտակուցը[27]։
- Քրոմպրոտեիդների պրոսթետիկ խումբը տարբեր քիմիական բնույթ ունեցող մնացորդ է, որը, սակայն, գունավորված է։ Քրոմպրոտեիդներ են մետաղ պարունակող պորֆրինիային խմբով սպիտակուցները, որոնք կատարում են տարբեր գործառույթներ, օրինակ՝ հեմոպրոտեինները, որոնք՝ որպես պրոսթետիկ խումբ, պարունակում են հեմ (հեմոգլոբին և ցիտոքրոմներ), ֆլավոպրոտեիդներ ֆլավինային խմբով և այլն։
Սպիտակուցի կենսաֆիզիկա[խմբագրել | խմբագրել կոդը]
Սպիտակուցի ֆիզիկական հատկությունները բջջում շատ բարդ են։ Վարկածներից մեկի համաձայն՝ սպիտակուցը բջջում ունի կարգավորված բյուրեղանման կառուցվածք՝ ապերիոդիկ բյուրեղի տեսք[28][29]։ Այս վարկածը հաստատվում է ռենտգենկառուցվածքային անալիզի (մինչև 1 անգստրեմ չափում)[30], փաթեթավորման մեծ պտության[31], բնափոխման գործընթացի համակարգայնության[32] և այլ փաստերի միջոցով[33]։
Մյուս վարկածի՝ ներգլոբուլյար շարժումների ժամանակ սպիտակուցի՝ հեղուկանման կառուցվածք ունենալու օգտին են խոսում նեյրոնների սփռման[34], մյոս-բաուերովյան սպեկտրոսկոպիայի[35][36] վերաբերյալ տվյալները։
Սինթեզ[խմբագրել | խմբագրել կոդը]

Կենսասինթեզ[խմբագրել | խմբագրել կոդը]
Ունիվերսալ եղանակ՝ ռիբոսոմային սինթեզ[խմբագրել | խմբագրել կոդը]
Սպիտակուցները կենդանի օրգանիզմների կողմից սինթեզվում են ամինաթթուներից՝ գեներում գաղտնագրված տեղեկատվության հիման վրա։ Յուրաքանչյուր սպիտակուց կազմված է ամինաթթվային մնացորդների մենահատուկ հաջորդականությունից, որը որոշվում է սպիտակուցը գաղտնագրող գենի նուկլեոտիդային հաջորդականությամբ։ Տրանսլյացիան պոլիպեպտիդային շղթայի ամինաթթվային հաջորդականությունը նուկլեոտիդային հաջորդականության վերածելու հատուկ եղանակ է։ Այս գաղտնագիրը որոշվում է կոդոններով, որոնք ՌՆԹ-ի եռնուկլեոտիդ հաջորդականություններ են և այն ամինաթթուներով, որոնք մտնում են պոլիպեպտիդի կազմի մեջ։ Օրինակ՝ ԱՈՒԳ հաջորդականությանը համապատասխանում է մեթիոնին ամինաթթուն։ Քանի որ ԴՆԹ-ն բաղկացած է 4 տեսակի նուկլեոտիդներից, հնարավոր կոդոնների թիվը 64-ն է։ Իսկ սպիտակուցների կազմի մեջ մտնող ամինաթթուների թիվն ընդամենը 20-ն է։ Այս պատճառով, շատ ամինաթթուներ որոշվում են մեկից ավելի կոդոններով։ 3 կոդոններ ծառայում են որպես պոլիպեպտիդային շղթայի սինթեզի ավարտն ազդարարողներ։ Այս կոդոններն անվանվում են տերմինալ կամ ստոպ կոդոններ[37]։
Սպիտակուցը գաղտնագրող գեները, սկզբում տրանսկրիպցվում են ՌՆԹ պոլիմերազների միջոցով՝ առաջացնելով մատրիցային ՌՆԹ (մՌՆԹ)։ Դեպքերի ճնշող մեծամասնության ժամանակ կենդանի օրգանիզմների սպիտակուցները սինթեզվում են ռիբոսոմներում, որոնք ցիտոպլազմայում գտնվող բազմաբաղկացուցիչ մոլեկուլային համալիրներ են։ Ռիբոսոմներում պոլիպեպտիդային շղթայի սինթեզը մՌՆԹ-ի հիմքի վրա անվանվում է տրանսլյացիա[37]։
Սպիտակուցների ռիբոսոմային սինթեզը նույնանման է պրոկարիոտների և էուկարիոտների մոտ, բայց որոշ առումներով տարբերվում է։ Այսպես, օրինակ՝ պրոկարիոտների մՌՆԹ-ն կարող է տրանսլացվել տրանսկրիպցիայից անմիջապես հետո և նույնիսկ մինչև տրանսկրիպցիայի ավարտը[38]։ Էուկարիոտների մոտ առաջնային տրանսկրիպտը սկզբում պետք է ենթարկվի որոշ հետտրանսկրիպցիոն ձևափոխությունների, որն անվանվում է ՌՆԹ պրոցեսինգ և տեղափոխվել ցիտոպլազմային այն հատվածը, որտեղ տեղի է ունենալու տրանսլյացիան։ Սպիտակուցի սինթեզի արագությունն ավելի մեծ է պրոկարիոտների մոտ և կարող ա հասնել մեկ վայրկյանում 20 ամինաթթու արագության[39].
Մինչև տրանսլյացիայի սկիզբը ամինոացիլ-փՌՆԹ-սինթետազները մենահատուկ կերպով միանում են ամինաթթուներին համապատասխանող փՌՆԹ-ների հետ։ ՓՌՆԹ-ի հակակոդոն անվանվող հատվածը կոմպլեմենտար կերպով կարող միանալ մՌՆԹ-ի կոդոնի հետ՝ ապահովելով գենետիկական գաղտնագրի համապատասխան փՌՆԹ-ի ամինաթթվային մնացորդի միացումը պոլիպեպտիդային շղթային։
Տրանսլյացիայի սկզբնական փուլի՝ ինիցիացիայի ընթացքում, ռիբոսոմը ճանաչում է ինիցիացիայի կոդոնը, որին սպիտակուցային ինցիացիայի գործոնների միջոցով միանում է ամինոացիլ մեթիոնինային փՌՆԹ-ն։ Ստարտ կոդոնի ճանաչումից հետո ռիբոսոմի փոքր ենթամիավորմանն է միանում մեծ ենթամիավորումը և սկսվում է տրանսլյացիայի երկրորդ փուլը՝ էլոնգացիան։ ԻՌՆԹ-ի վրա 5'-ից 3' ռիբոսոմի կատարած յուրաքանչյուր քայլում ընթերցվում է մեկ կոդոն, ջրածնային կապեր են առաջանում փՌՆԹ-ի հակակոդոնի և իՌՆԹ-ի կոդոնի միջև, համապատասխան ամինաթթվային մնացորդը միանում է աճող պեպտիդի վերջին ամինաթթվային մնացորդին՝ ձևավորվում է պեպտիդային կապ։ Այս գործը կատալիզում է պեպտիդիլտրանսֆերազային կենտրոնը ձևավորող ռիբոսոմային ՌՆԹ-ն։ Այս կենտրոնում ազոտի և ածխածնի ատոմները գրավում են այնպիսի դիրք, որի դեպքում ռեակցիան կարող է հաջողությամբ իևականանալ։ Տրանսլյացիայի վերջին եզրափակիչ փուլը տերմինացիան է, երբ ռիբոսոմը հասնում է ստոպ կոդոնին։ Ստոպ կոդոնին հասնելուց հետո տերմինացիայի գործոնները հիդրոլիզում են վերջին փՌՆԹ-ի և պոլիպեպտիդային շղթայի միջև. սպիտակուցի սինթեզը դադարում է։ Ռիբոսոմում սպիտակուցները միշտ սինթեզվում են N- կամ C- ծայրից[37]։
Ոչ ռիբոսոմային սինթեզ[խմբագրել | խմբագրել կոդը]
Ստորակարգ սնկերի և որոշ բակտերիաների մոտ հայտնի է լրացուցիչ, ոչ ռիբոսոմային կամ բազմաֆերմենտային պեպտիդների սինթեզը։ Այս պեպտիդների սինթեզը, իրականացվում է բարձրամոլեկուլային համալիրի՝ NRS-սինթազի միջոցով, առանց ռիբոսոմների անմիջական մասնակցության։ NSR- սինթազը սովորաբար կազմված է մի քանի դոմեններից կամ առանձին սպիտակուցներից, որոնք իրականացնում են ամինաթթուների ընտրությունը, պեպտիդային կապի առաջացումը և սինթեզված պեպտիդի անջատումը։ Այս դոմենները միասին առաջացնում են մոդուլ։ Յուրաքանչյուր մոդուլը ապահովում է մի ամինաթթվի միացումը սինթեզվող պեպտիդին։ NRS-սինթազները, այսպիսով, կարող են բաղկացած լինել մեկ կամ ավելի մոդուլներից։ Այս համալիրների ներսում կարող են մտնել նաև այնպիսի դոմեններ, որոնք կարողանում են իզոմերացնել L-ամինաթթուները D-ձևի[40][41]։
Քիմիական սինթեզ[խմբագրել | խմբագրել կոդը]
Կարճ սպիտակուցները կարող են սինթեզվել քիմիական եղանակով՝ օրգանական սինթեզի մեթոդների, օրինակ՝ լիգազի կիրառությամբ[42]։ Պեպտիդի քիմիական սինթեզը հիմնականում տեղի է ունենում C-ից դեպի N- ծայրը, ի հակառակ՝ ռիբոսոմներում ընթացող սինթեզի։ Քիմիական անալիզի մեթոդով ստանում են կարճ իմունոգեն պեպտիդներ՝ էպիտոպներ, որոնք հետագայում ներարկում են կենդանիներին՝ յուրահատուկ հակամարմինների և հիբրիդոմների ստացման նպատակով։ Բացի այդ, այս մեթոդն օգտագործվում է նաև որոշ ֆերմենտների ինհիբիտորների ստացման համար[43]։ Քիմիական սինթեզը թույլ է տալիս սպիտակուցի կազմի մեջ ներառել մյուս սպիտակուցներում չհանդիպող ամինաթթվային մնացորդներ, որոնց կողմնային շղթաներին, օրինակ, միացած են ֆլյոուրեսցենտ (լուսարձակող) նշագրեր։ Սպիտակուցների քիմիական սինթեզի մեթոդներն ունեն որոշ սահմանափակումներ. 300-ից ավելի ամինաթթվային մնացորդ պարունակող պեպտիդների սինթեզը ոչ արդյունավետ է, սինթեզված պեպտիդները կարող են ունենալ ոչ ճիշտ երրորդային կառուցվածք, բացակայեն բնութագրական հետտրանսլյացոն ձևափոխությունները։
Հետտրանսլյացիոն ձևափոխություններ[խմբագրել | խմբագրել կոդը]
Տրանսլյացիայից հետո սպիտակուցների մեծ մասը ենթարկվում է հետագա քիմիական ձևափոխությունների, որոնք միասին անվանվում են հետտրանսլյացիոն ձևափոխություններ[44]։ Հայտնի է սպիտակուցների հետտրանսլյացիոն ձևափոխությունների ավելի քան երկու հարյուր եղանակ[45].
Հետտրանսլյացիոն ձևափոխությունները կարող են կարգավորել սպիտակուցի գոյության տևողությունը բջջում, սպիտակուցի ֆերմենտային ակտիվությունը և փոխհարաբերությունը այլ սպիտակուցների հետ։ Որոշ դեպքերում հետտրանսլյացիոն ձևափոխությունները կարևոր են սպիտակուցների հասունացման համար։ Օրինակ՝ ինսուլինի և որոշ հորմոնների հասունացման ժամանակ պոլիպեպտիդային շղթայի օրգանական պրոտեոլիզը անհրաժեշտ է, պլազմային թաղանթի սպիտակուցների դեպքում՝ գլիկոզիլացումը։
Հետտրանսլյացիոն ձևափոխությունները կարող են լինել լայնորեն տարածված, այնպես էլ հազվադեպ հանդիպող և մենահատուկ։ Ունիվերսալ ձևափոխության օրինակ է ուբիքվիտինացումը (սպիտակուցին մի քանի մոլեկուլից կազմված ուբիքվիտինի շղթայի միացումը), որը ծառայում է պրոռեասոմայի կողմից սպիտակուցի ճեղքման ազդանշան[46]։ Հաջորդ տարածված ձևափոխությունը գլիկոզիլացումն է․ ընդունված է, որ մարդու սպիտակուցների կեսից ավելին գլիկոզիլացված են[47]։ Հազվադեպ հանդիպող ձևափոխություններից է տուբուլինի թիրոզինացումը, դեթրիոզինացումը և պոլիգլիցիլացումը[48]։
Միևնույն սպիտակուցը կարող է ենթարկվել բազմակի ձևափոխությունների։ Այսպես օրինակ, հիստոնները՝ էուկարիոտների քրոմատինի կազմի մեջ մտնող սպիտակուցները, տարբեր պայմաններում կարող են ենթարկվել ավելի քան 150 տարբեր ձևափոխությունների[49]։
Հետտրանսլյացիոն ձևափոխությունները բաժանվում են հետևյալ խմբերի՝
- գլխավոր շղթայի ձևափոխություն,
- մեթիոնինի N-ծայրային մնացորդի ճեղքում,
- օրգանական պրոտեոլիզ․ մոլեկուլի ծայրից կամ կենտրոնից սպիտակուցի հատվածի հեռացումը,
- տարբեր քիմիական խմբերի միացում ազատ ամինո- և կարբօքսիլ խմբերին (N-ացիլացում, միրիստոիլացում և այլն),
- ամինաթթուների կողմնային շղթաների ձևափոխություն,
- ոչ մեծ քիմիական խմբերի միացում և ճեղքում (գլիկոլիզացում, ֆոսֆորիլացում և այլն),
- լիպիդների և ածխաջրերի միացում,
- ստանդարտ ամինաթթվային մնացորդների փոխարինում ոչ ստանդարտով (ցիտրուլինի առաջացում),
- ցիստեինի մնացորդների միջև դիսուլֆիդային կամրջակների առաջացում,
- ոչ մեծ սպիտակուցների միացում (սումոիլացում, ուբիքվիտինացում)։
Կյանքի ցիկլ[խմբագրել | խմբագրել կոդը]
Ներբջջային տրանսպորտ և դասավորում[խմբագրել | խմբագրել կոդը]

Էուկարիոտ բջիջների ցիտոպլազմայում սինթեզվող սպիտակուցները պետք է տեղափոխվեն բջջի տարբեր օրգանոիդներ, դեպի բջջակորիզ, միտոքոնդրիումներ, էնդոպլազմային ցանց, Գոլջիի ապարատ, լիզոսոմներ և այլ։ Որոշ սպիտակուցներ էլ պետք է դուրս բերվեն արտաբջջային տարածություն[50]։ Որպեսզի սպիտակուցը տեղափոխվի կամ հայտնվի բջջի անհրաժեշտ հատված, այն պետք է օժտված լինի յուրահատուկ պիտակով։ Այս պիտակը դեպքերի մեծ մասում հենց տվյալ սպիտակուցի ամինաթթվային հաջորդականության մի մասն է (գլխավորող պեպտիդ կամ սպիտակուցի ազդանշանային հաջորդականություն)․ որոշ դեպքերում այս պիտակը օլիգոսախարիդներ են, որոնք մոլեկուլին միանում են հետտրանսլյացիոն ձևափոխությունների արդյունքում[51]։
Սպիտակուցների տեղափոխումը էնդոպլազմային ցանց ընթանում է սպիտակուցի սինթեզին զուգահեռ, քանի որ ԷՑ-ի ազդանշանային հաջորդականություն կրող սպիտակուցներ սինթեզող ռիբոսոմները նստում են ԷՑ-ի արտաքին մեմբրանի վրա[52]։ ԷՑ-ից սպիտակուցի մոլեկուլները տեղափոխվում են Գոլջիի ապարատ, լիզոսոմներ և ապա արտաքին մեմբրան կամ արտաբջջային տարածություն՝ վեզիկուլյար տրանսպորտի միջոցով։ Սպիտակուցները կորիզ են թափանցում կորիզի անցուղիների միջոցով։ Միտոքոնդրիումներ և քլորոպլաստներ թափանցումը կատարվում է հատուկ սպիտակուցիային անցուղի-տրանսլոկատորների միջոցով՝ շապերոնների մասնակցությամբ։
Կառուցվածքի պահպանում և դեգրադացիա[խմբագրել | խմբագրել կոդը]
Սպիտակուցի կանոնավոր տարածական կառուցվածքի պահպանումը կարևոր է նորմալ կենսագործունեության համար։ Սպիտակուցների ագրեգացիա առաջացնող ոչ ճիշտ ֆոլդինգը կարող է պայմանավորված լինել մուտացիաներով, օքսիդացմամբ, սթրեսային պայմաններով կամ բջջի ֆիզիոլոգիայի ընդհանուր փոփոխություններով։ Սպիտակուցների ագրեգացիան օրգանիզմի ծերացման բնորոշ երևույթ է։ Ենթադրվում է, որ սպիտակուցների ոչ կանոնավոր ֆոլդինգը պատճառ է դառնում շատ հիվանդությունների՝ մուկովիսցիդոզի, նեյրոդեգեներատիվ հիվանդությունների (Ալցհայմերի, Հանդինգտոնի, Պարկինսոնի հիվանդություններ) սրմանը[53]։
Էվոլյուցիայի ընթացքում բջիջները ձեռք են բերել սպիտակուցների ագրեգացիային հակազդելու չորս հիմնական մեխանիզմներ։ Առաջին երկուսը՝ շապերոնների միջոցով կրկնակի ֆոլդինգը կամ ռեֆոլդինգը և պորտեազների միջոցով՝ սպիտակուցի ճեղքումը, հանդիպում է բակտերիաների և բարձրակարգ օրգանիզմների մոտ։ Աուտոֆագիան և ոչ ճիշտ ֆոլնդինգի ենթարկված սպիտակուցների կուտակումը հատուկ մեմբրանային օրգանելներում հատուկ է միայն էուկարիոտներին[25][54]։
Շապերոններ[խմբագրել | խմբագրել կոդը]
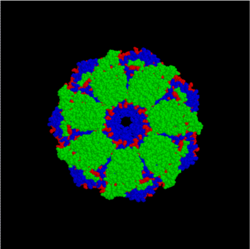
Սպիտակուցների՝ բնափոխումից հետո կանոնավոր եռաչափ կառուցվածքը վերականգնելու հատկությունը թույլ է տալիս ենթադրել, որ սպիտակուցի վերջնական կառուցվածքի մասին առկա ամբողջ տեղեկատվությունը պահվում է մոլեկուլի ամինաթթվային հաջորդականությունում։ Սպիտակուցի կայուն կոնֆորմացիան (անգլ.՝ conformation՝ տարածական կառուցվածք) մյուս հնարավոր կոնֆորմացիաների համեմատ օժտված է նվազագույն ազատ էներգիայով[55]։
Բջիջներում կան սպիտակուցի հատուկ խմբեր, որոնց ֆունկցիան մյուս սպիտակուցների ճիշտ ֆոլդինգ իրականացնելն է վերջիններիս սինթեզից հետո, ինչպես նաև սպիտակուցների կառուցվածքը վերականգնելը վնասումից հետո, սպիտակուցային համալիրների կառուցումը և դիսոցացումը։ Այս սպիտակուցներն անվանվում են շապերոններ։ Շատ շապերոնների կոնցենտրացիան բջջում, աճում է արտաքին միջավայրի ջերմաստիճանի բարձրացման հետ․ այս շապերոնները պատկանում են Hsp (անգլ.՝ heat shock proteins խմբին[56]։ Շապերոնների նորմալ աշխատանքը կարելի է ցույց տալ α-կրիստալինի շապերոնի օրինակով։ Այն մտնում է մարդու աչքի ոսպնյակի կազմի մեջ․ շապերոնի մուտացիան բերում է ոսպնյակի մթագմանը, առաջանում է կատարակտ[57]։
Պրոտեոլիզ[խմբագրել | խմբագրել կոդը]
Սպիտակուցի մոլեկուլները բջջի կողմից ոչնչացվում են, եթե երրորդային կառուցվածքը հնարավոր չի վերականգնել։ Սպիտակուցների դեգրադացիան իրականացնող ֆերմենտներն անվանվում են պրոտեազներ։ Պրոտեազները բաժանվում են երկու խմբի՝
- Էնդոպեպտիդազներ կամ պեպտիդային շղթայի ներսում պեպտիդային կապերը խզող ֆերմենտներ, որոնք ճանաչում և կապվում են սուբստրատի կարճ ամինաթթվային հաջորդականության հետ և յուրահատուկ կերպով հիդրոլիզում որոշակի ամինաթթվային մնացորդներ։
- Էկզոպեպտիդազներ կամ ֆերմենտներ, որոնք ճեղքում են շղթայի ծայրերի պեպտիդային կապերը։ Ամինոպեպտիդազները ճեղքում են N-ծայրի, իսկ կարբոքսիպեպտիդազները՝ C-ծայրի պեպտիդային կապերը, դիպեպտիդազները ճեղքում են միայն դիպեպտիդները։
Կատալիզի մեխանիզմի հիման վրա կենսաքիմիայի և մոլեկուլային կենսաբանության համաշխարհային միությունը առանձնացնում է մի քանի պրոտեազների դասեր՝ սերինային պրոտեազներ, ասպարգինային պրոտեազներ, ցիստեինային պրոտեազներ և մետաղպրոտեազներ[58]։
Պրոտեազի հատուկ տեսակ՝ պրոտեասոմը, մեծ բազմաենթամիավորում պրոտեազ է, որն առկա է էուկարիոտների, արքեաների և որոշ բակտերիաների կորիզում և ցիտոպլազմայում[59][60]։
Թիրախ սպիտակուցը պրոտեասոմայով քայքայելու համար, այն պետք է նշվի փոքր սպիտակուցով՝ ուբիկվիտինով։ Ուբիկվիտինի միացումը կատալիզում է ուբիքվիտինլիգազը։ Ուբիքվիտինի առաջին մոլեկուլի միացումը լիգազի համար ազդանշան է մյուս մոլեկուլների միացման համար։ Արդյունքում սպիտակուցին միանում է պոլիուբիքվիտինային շղթա, որը միանում է պորտեասոմայի հետ և ապահովում թիրախ-սպիտակուցի ճեղքումը[59][60]։ Այս համակարգն անվանվում է ուբիքվիտին-կախյալ սպիտակուցների դեգրադացում։ Ներբջջային սպիտակուցի 80-90%-ը դեգրադացվում է պրոտեասոմաների միջոցով։
Սպիտակուցների դեգրադացումը պերօքսիսոմներում կարևոր է շատ բջջային գործընթացների նորմալ ընթացքի համար, այդ թվում՝ բջջային ցիկլ, գեների էքսպրեսիայի կարգավորում և օքսիդային սթրեսի պատասխանի ձևավորում։
Աուտոֆագիա[խմբագրել | խմբագրել կոդը]

Աուտոֆագիան լիզոսոմներում (կաթնասուններ) կամ վակուոլներում (խմորասնկեր) երկարակյաց կենսամոլեկուլների, հատկապես, սպիտակուցների և օրգանոիդների դեգրադացիայի գործընթացն է։ Աուտոֆագին ցանկացած նորմալ բջջի կենսագործունեության մի մասն է, այն կարող են խթանել օրգանիզմում սննդարար նյութերի բացակայությունից առաջացող ազդակները, վնասված օրգանոիդների առկայությունը և վերջապես ցիտոպլազմայում մասամբ բնափոխված սպիտակուցների և նրանց մնացորդների առկայությունը[61]։
Տարբերում են աուտոֆագիայի երեք տեսակ՝ միկրոաուտոֆագիա, մակրոաուտոֆագիա և շապերոն-կախյալ աուտոֆագիա։
ՄԻկրոաուտոֆագիայի ժամանակ մակրոմոլեկուլները և բջջաթաղանթի մնացորդները կլանվում են լիզոսոմի կողմից։ Այսպիսով բջիջը ընդունակ է քայքայել սպիտակուցները էներգիայի կամ կառուցվածքային նյութի բացակայության պայմաններում։ Միկրոաուտոֆագիան տեղի է ունենում նորմալ պայմաններում ևս և ընտրողական գործընթաց չէ։ Միկրոաուտոֆագիայի ժամանակ կարող են կլանվել նաև օրգանոիդները։ Այսպես օրինակ խմորասնկերի մոտ նկարագրված է պերօքսիսոմների և կորիզի մասնակի աուտոֆագիան, որի դեպքում սակայն բջիջը պահպանում է իր կենսագործունեությունը[61]։
Մակրոաուտոֆագիայի ժամանակ ցիտոպլազմայի մի հատվածը, որը պարունակում է որոշ օրգանոիդներ, շրջափակվում է թաղանթային կառուցվածք ունեցող գոյացությամբ, որը նման է էնդոպլազմային ցանցին։ Արդյունքում այդ հատվածը առանձնանում է ցիտոպլազմայի մյուս տեղամասերից երկշերտ թաղանթով։ Այսպիսի երկմեմբրան գոյացություններն անվանվում են աուտոֆագոսոմներ։ Աուտոֆագոսոմները ձուլվում են լիզոսոմների հետ՝ ձևավորելով աուտոֆագոլիզսոսոմներ, որոնցում օրգանոիդները և աուտոֆագոսոմների մյուս պարունակությունը քայքայվում է և մարսվում։ Ենթադրվում է, որ մակրոաուտոֆագիան նույնպես ընտրողական գործընթաց չէ, չնայած հաճախ նշվում է, որ մակրոաուտոֆագիայի միջոցով բջիջը կարող է ընտրողաբար ազատվել ծերացած օրգանոիդներից[61]։
Աուֆոֆագիայի երրորդ տեսակը շապերոն-կախյալ աուտոֆագիան է, որի ժամանակ տեղի է ունենում մասամբ բնափոխված սպիտակուցների ուղղորդված տեղափոխությունը լիզոսոմի թաղանթով դեպի նրա ներսը, որտեղ այս սպիտակուցները քայքայվում են։ Աուտոֆագիայի այս տեսակը նկարագրված է միայն կաթնասունների մոտ և խթանվում է սթրեսով[54]։

JUNQ և IPOD[խմբագրել | խմբագրել կոդը]
Սթրեսի ժամանակ, երբ էուկարիոտ բջիջը չի կարողանում հաղթահարել մեծ քանակով չբնափոխված սպիտակուցների առկայությունը, այն կարող է ուղղորդել սպիտակուցները JUNQ և IPOD ժամանակավոր օրգանոիդների մեջ[62]։
JUNQ-ը (անգլ.՝ JUxta Nuclear Quality control compartment, մերձկորիզային գոյացություն, որը կարգավորում է սպիտակուցների որակը), կապված է կորիզաթաղանթի արտաքին թաղանթի հետ և պարունակում է ուբիքվիտինային սպիտակուցներ, որոնք կարող են արագ անցնել ցիտոպլազմա, շապերոններ և պրոտեոսոմներ։ JUNQ-ի ենթադրելի ֆունկցիան սպիտակուցների վերաֆոլդինգն է և/կամ սպիտակուցների դեգրադացիան[25]։
IPOD-ը (անգլ.՝ Insoluble Protein Deposit անլուծելի սպիտակուցների պահպանման վայր) գտնվում է կենտրոնական վակուոլի մոտ և պարունակում է անշարժ ագրեգատներ, որոնք ֆոմիրացնում են սպիտակուցների ամիլոիդները։ Այս սպիտակուցների կուտակումը IPOD-ում կանխարգելում է վերջիններիս փոխհարաբերությունը նորմալ բջջային կառույցների հետ, որի պատճառով ենթադրում են, որ այս գործընթացն ունի պաշտպանական նշանակություն[25]։
Սպիտակուցի ֆունկցիաներն օրգանիզմում[խմբագրել | խմբագրել կոդը]
Ինչպես մյուս կենսաբանական մակրոմոլեկուլները (բազմաշաքարներ, լիպիդներ և նուկլեինաթթուներ), սպիտակուցները բոլոր կենդանի օրգանիզմների անհրաժեշտ բաղադրամաս են և խաղում են կարևոր դեր բջջի կենսագործունեությունում։ Սպիտակուցները իրականացնում են նյութափոխանակության գործընթացները։ Նրանք կազմում են ներբջջային կառույցները՝ օրգանոիդները և բջջակմախքը, արտազատվում են միջբջջային տարածություն, որտեղ կարող են իրականացնել միջբջջային հաղորդակցությանը, մասնակցել սննդանյութերի հիդրոլիզին և միջբջջային նյութի ձևավորմանը։
Ըստ գործառույթի` սպիտակուցների դասակարգումը շատ պայմանական է, քանի որ նույն սպիտակուցը կարող է իրականացնել մի քանի ֆունկցիա։ Այսպիսի բազմաֆունկցիոնալ սպիտակուցի օրինակ է լիզիլ-փՌՆԹ-սինթետազը, որը ամինոացիլ-փՌՆԹ-սինթետազ է, այն ոչ միայն միացնում է լիզինի մնացորդը փՌՆԹ-ին, այլև կարգավորում է որոշ գեների տրանսկրիպցիան[63]։
Շատ սպիտակուցներ ունեն ֆերմենտատիվ ակտիվություն։ Ֆերմենտ է շարժողական միոզին սպիտակուցը, կարգավորիչ սպիտակուցներ պրոտեինկինազները, փոխադրիչ սպիտակուց նատրիում-կալիումական ադենոզինֆոսֆատազ և այլն։

Կատալիտիկ ֆունկցիա[խմբագրել | խմբագրել կոդը]
Սպիտակուցների ամենից հայտնի ֆունկցիան օրգանիզմում տարբեր քիմիական ռեակցիաների կատալիզն է։ Ֆերմենտները սպիտակուցներ են, որոնք օժտված են յուրահատուկ կատալիտիկ ակտիվությամբ, այսինքն յուրաքանչյուր ֆերմենտ կատալիզում է մեկ կամ համանման ռեակցիաներ։ Ֆերմենտները կատալիզում են բարդ մոլեկուլների ճեղքումը (կատաբոլիզմ) և սինթեզը (անաբոլիզմ), ինչպես նաև ռեպլիկացիան, ռեպարացիան և ՌՆԹ-ի մատրիցային սինթեզը։ 2013 թվականի տվյալներով նկարագրված է ավելի քան 5000 տարբեր ֆերմենտներ[64][65]։ Ֆերմենտների մասնակցությամբ ռեակցիայի արագությունը կարող է շատ շեշտակի աճել։ Օրինակ՝ օրոտիդի-5'-ֆոսֆատդեկարբօքսիլազի կողմից կատալիզվող ռեակցիան 1017 անգամ ավելի արագ է ընթանում չկատալիզվող ռեակցիայի համեմատությամբ[66]։ Այն մոլեկուլները, որոնք միանում են ֆերմենտին և փոփոխվում են ռեակցիայի արդյունքում, անվանվում են սուբստրատներ։
Չնայած որ ֆերմենտները կազմված են հարյուրավոր ամինաթթվային մնացորդներից, սուբստրատի հետ փոխազդում է նրանց միայն մի փոքր մասը, իսկ 3-4` առաջնային կառուցվածքում միմյանցից հեռու դասավորված ամինաթթվային մնացորդներ ուղղակիորեն մասնակցում են կատալիզին[67]։ Ֆերմենտի մոլեկուլի այն հատվածը, որն ապահովում է սուբստրատի միացումը և կատալիզը, անվանվում է ֆերմենտի ակտիվ կենտրոն։
1992 թվականին կենսաքիմիայի և մոլեկուլային կենսաբանության միջազգային միությունը առաջարկեց ֆերմենտների անվանակարգման վերջնական տարբերակ, որը հիմնված էր կատալիզվող ռեակցիայի բնույթի վրա[68]։ Այս անվանակարգման համաձայն՝ ֆերմենտի անվանումը միշտ պետք է ունենա -ազ վերջավորությունը և ձևավորվի կատալիզվող ռեակցիայի և սուբստրատի անվանումներից։ Յուրաքանչյուր ֆերմենտ ստանում է յուրահատուկ կոդ, որով հեշտությամբ հնարավոր է պարզել նրա դիրքը ֆերմենտների հիերարխիայում։ Ըստ կատալիզվող ռեակցիայի բնույթի` ֆերմենտները բաժանվում են 6 դասերի՝
- ՖԴ 1։ Օքսիդոռեդուկտազներ, կատալիզում են օքսիդավերականգնման ռեակցիաները
- ՖԴ 2։ Տրանսֆերազներ, կատալիզում են քիմիական խմբերի տեղափոխումը սուբստրատի մի մոլեկուլից դեպի մյուսը
- ՖԴ 3։ Հիդրոլազներ, կատալիզում են քիմիական կապերի հիդրոլիզը
- ՖԴ 4։ Լիազներ, կատալիզում են քիմիական կապերի ճեղքումն առանց հիդրոլիզի պրոդուկտներից մեկում կրկնակի կապերի առաջացմամբ
- ՖԴ 5։ Իզոմերազներ, կատալիզում են սուբստրատի մոլեկուլում կառուցվածքային և երկրաչափական փոփոխությունները
- ՖԴ 6։ Լիգազներ, դիֆոսֆատային կապի կամ եռֆոսֆատի հիդրոլիզի միջոցով կատալիզում են քիմիական կապերի առաջացումը։
Կառուցվածքային ֆունկցիա[խմբագրել | խմբագրել կոդը]
Բջջակմախքի կառուցվածքային սպիտակուցները բջջին և օրգանոիդներին տալիս են որոշակի ձև և մասնակցում են բջջի ձևի փոփոխմանը։ Կառուցվածքային սպիտակուցների մեծամասնությունը ֆիլամենտային է. օրինակ՝ ակտինի և տուբուլինի մոնոմերները՝ գլոբուլյար, լուծվող սպիտակուցներ են, բայց պոլիմերիզացումից հետո առաջացնում են երկար շղթաներ, որոնցից էլ կազմվում է բջջակմախքը[69]։ Կոլագենը և էլաստինը, շարակցական հյուսվածքի (օրինակ՝ աճառի) միջբջջային նյութի կարևոր բաղադրամասերն են, իսկ կերատինից են կազմված մազերը, եղունգները, թռչունների փետուրները և որոշ օրգանիզմների խեցիները։

Պաշտպանական ֆունկցիա[խմբագրել | խմբագրել կոդը]
Տարբերում են սպիտակուցների պաշտպանական ֆունկցիայի մի քանի տեսակներ.
- Ֆիզիկական պաշտպանություն։ Օրգանիզմի ֆիզիկական պաշտպանությունը ապահովում է կոլագենը, որը ձևավորում է շարակցական հյուսվածքի միջբջջային նյութը, կերատինը՝ պոզերի, մազերի, փետուրների, թեփուկների և էպիդերմիսի այլ հավելվածների գլխավոր բաղադրամասը։ Այս սպիտակուցները հիմնականում համարվում են կառուցվածքային սպիտակուցները։ Այս սպիտակուցներից է նաև ֆիբրինոգենը և թրոմբինը[70], որոնք մասնակցում են արյան մակարդմանը։
- Քիմիական պաշտպանություն։ Թույների հետ սպիտակուցի մոլեկուլների միացումը կարող է ապահովել դետոքսիկացումը։ Մարդու կարևոր նշանակություն ունեն լյարդի բջիջների դետոքսիկացնող ֆերմենտները, որոնք քայքայում են թույները, դարձնում լուծելի և ապահովում օրգանիզմից արագ դուրսբերումը[71]։
- Իմունային համակարգ։ Սրանք արյան և այլ կենսաբանական հեղուկների կազմի մեջ մտնող պիտակուցներն են, որոնք մասնակցում են վնասվածքի և ախտածինների հանդեպ ձևավորվող իմունային պատասխանի ձևավորմանը։ Կոմպլեմենտի համակարգի սպիտակուցները և հակամարմինները (իմունոգլոբուլինները) մասնակցում են ախտածինների դեմ պայքարին, նրանք չեզոքացնում են բակտերիաները, վիրուսները և օտարածին այլ սպիտակուցներ։ Հակամարմինները կարող են ներզատվել միջբջջային տարածություն կամ ամրանալ հատուկ մասնագիտացած B-լիմֆոցիտների՝ պլազմոցիտների թաղանթների վրա[72]։
Կարգավորիչ ֆունկցիա[խմբագրել | խմբագրել կոդը]
Բջջում իրականացվող շատ գործընթացներ կարգավորվում են սպիտակուցների կողմից, որոնք էներգիայի աղբյուր չեն և կառուցվածքային նյութ չեն բջջի համար։ Այս սպիտակուցներն ապահովում են բջջային ցիկլի, տրանսկրիպիցիայի, տրանսլյացիայի, սպլայսինգի (անգլ.՝ splice՝ միահյուսել) և բազմաթիվ այլ գործընթացների կարգավորումը։ Սպիտակուցների կարգավորիչ ֆունկցիան իրականանում է կամ ֆերմենտատիվ ակտիվության կամ այլ մոլեկուլների հետ սպեցիֆիկ կապի շնորհիվ։ Այսպես օրինակ՝ տրանսկրիպցիայի գործոնները, ակտիվատոր սպիտակուցները և ռեպրեսոր սպիտակուցները կարող են կարգավորել գեների տրանսկրիպցիայի ինտենսիվությունը՝ կապվելով կարգավորիչ հաջորդականությունների հետ։ Տրանսլյացիայի մակարդակում շատ ի-ՌՆԹ-ների ընթերցումը կարգավորվում է նաև սպիտակուցային գործոնների միացումով[73]։
Ներբջջային գործընթացների կարգավորման մեջ կարևոր դեր են խաղում պրոտեինկինազները և պոտեինֆոսֆատազները. սրանք այն ֆերմենտներն են, որոնք ակտիվացնում կամ ճնշում են այլ սպիտակուցների ակտիվությունը՝ միացնելով կամ ճեղքելով ֆոսֆատային խումբը։

Ազդանշանային ֆունկցիա[խմբագրել | խմբագրել կոդը]
Ազդանշանային ֆունկցիան սպիտակուցների` որպես ազդանշանային նյութեր ծառայելու հատկությունն է։ Սպիտակուցները մասնակցում են բջիջների, հյուսվածքների, օրգանների և օրգանիզմների միջև ազդանշանի փոխանցմանը։ Հաճախ սպիտակուցների ազդանշանային և կարգավորիչ ֆունկցիաները միացվում են, քանի որ շատ ներբջջային կարգավորիչ սպիտակուցներ նույնպես մասնակցում են ազդանշանի փոխանցմանը։
Ազդանշանային ֆունկցիան իրականացնում են սպիտակուց հորմոնները, ցիտոկինները, աճի գործոնները և այլն։
Հորմոնները տեղափոխվում են արյան միջոցով։ Կենդանական հորմոնների մեծամասնությունը սպիտակուցներ են կամ պեպտիդներ։ Ռեցեպտորի հետ հորմոնի միացումն ապահովում է ազդանշանը, որին հաջորդում է բջջի պատասխան ռեակցիան։ Հորմոնները կարգավորում են արյան և բջիջների նյութերի կոնցենտրացիան, աճը, բազմացումը և այլ գործընթացներ։ Այսպիսի սպիտակուցներից է, օրինակ, ինսուլինը, որն արյան մեջ կարգավորում է գլյուկոզի կոնցենտրացիան։
Բջիջները միմյանց հետ փոխազդեցության մեջ են մտնում միջբջջային նյութով փոխադրվող ազդանշանային սպիտակուցների միջոցով։ Այս սպիտակուցներին են պատկանում, օրինակ՝ ցիտոկինները և աճի գործոնները։
Ցիտոկինները պեպտիդային ազդանշանային մոլեկուլներ են, որոնք կարգավորում են այլ բջիջների հետ փոխհարաբերությունը, որոշում նրանց կյանքի տևողությունը, խթանում կամ ճնշում աճը, մասնագիտացումը, ֆունկցիոնալ ակտիվությունը և ապոպտոզը, ապահովում՝ իմունային, ներզատական և նյարդային համակարգերի համակարգված գործունեությունը։ Ցիտոկինների օրինակ է ուռուցի ներկրոզի գործոնը, որը օրգանիզմի բջիջներին է փոխանցում է բորբոքման ազդակները[74]։
Տրանսպորտային ֆունկցիա[խմբագրել | խմբագրել կոդը]
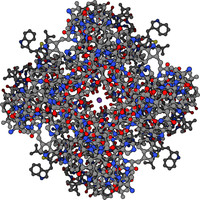
Մանր մոլեկուլների տեղափոխմանը մասնակցող լուծելի սպիտակուցները, պետք է սուբստրատի հետ ունենան մեծ աֆինություն, երբ սուբստրատի կոնցենտրացիան մեծ է, հեշտությամբ ազատվի, երբ սուբստրատի կոնցենտրացիան ցածր է։ Տրանսպորտային սպիտակուցների օրինակ է հեմոգլոբինը և հեմոգլոբինային մյուս սպիտակուցները, որը թթվածինը թոքերից տեղափոխում է հյուսվածքներ և ածխաթթու գազը՝ հյուսվածքներից թոքեր[75]։
Որոշ թաղանթային սպիտակուցներ մասնակցում են թաղանթի միջով փոքր մոլեկուլների տեղափոխմանը՝ փոխելով թաղանթի թափանցելիությունը։ Թաղանթի լիպիդները անջրաթափանց են (հիդրոֆոբ), որը կանխարգելում է բևեռային մոլեկուլների և լիցքավորված իոնների դիֆուզիան։ Մեմբրանային տրանսպորտային սպիտակուցները դասակարգում են սպիտակուց անցուղիներ և սպիտակուց տեղափոխողներ։ Սպիտակուցային անցուղիները ունեն ջրով լցված անցքեր, որոնք թույլ են տալիս իոններին՝ իոնային անցուղիների կամ ջրի մոլեկուլներին՝ ակվապորին սպիտակուցների միջոցով, տեղափոխվել մեմբրանի ներսով։ Շատ իոնային անցուղիներ մասնագիտացած են միայն մեկ իոնի տեղափոխման համար, օրինակ՝ կալցիումային և նատրիումային անցուղիները հաճախ տարբերում են այս իրար նման իոնները և անցկացնում նրանցից միայն մեկը[76]։ Սպիտակուց տեղափոխողները ֆերմենտների պես միանում են իոնին կամ տեղափոխման ենթակա մոլեկուլին և ի տարբերություն անցուղիների տեղափոխումը կարող են իրականացնել ԱԵՖ-ի էներգիայի հաշվին։ ԱԵՖ սինթետազը, որն ԱԵՖ-ի սինթեզն իրականացնում է պրոտոնային գրադիենտի հաշվին, նույնպես կարող է դասվել թաղանթային սպիտակուցների թվին[77]։
Պահեստային ֆունկցիա[խմբագրել | խմբագրել կոդը]
Այս սպիտակուցներից են օրինակ սերմնավոր բույսերի բջիջներում և կենդանիների ձվաբջիջներում որպես էներգիայի և կառուցվածքային նյութի պահեստ ծառայող սպիտակուցները (օրինակ՝ 7S և 11S գլոբուլիններ)[78]։ Շատ այլ սպիտակուցներ օրգանիզմում օգտագործվում են որպես ամինաթթուների աղբյուր, որոնք իրենց հերթին մետաբոլիզմը կարգավորող կենսաբանական ակտիվ միացությունների նախորդներն են։
Ռեցեպտորային ֆունկցիա[խմբագրել | խմբագրել կոդը]
Սպիտակուցային ռեցեպտորները կարող են գտնվել ինչպես ցիտոպլազմայում, այնպես էլ ներդրված լինել բջջաթաղանթի մեջ։ Մոլեկուլի մի մասը ընդունում է ազդանշանը, որը սովորաբար քիմիական միացություն է, հազվադեպ՝ լույս, մեխանիկական ազդեցություն և այլ ազդակներ։ Մոլեկուլի որոշակի հատվածի վրա տեղի ունեցած ազդեցության հետևանքով սպիտակուց ռեցեպտորը ենթարկվում է կոնֆորմացիոն փոփոխության։ Արդյունքում փոխվում է մոլեկուլի մյուս մասի կոնֆորմացիան, տեղի է ունենում ազդակի փոխանցումը դեպի բջջային մյուս բաղադրամասեր։ Գոյություն ունի ազդակի փոխանցման մի քանի մեխանիզմ։ Որոշ ռեցեպտորներ կատալիզում են որոշակի քիմիական ռեակցիա, մյուսները ծառայում են որպես իոնային անցուղիներ, ազդակի ազդեցությամբ փակվում կամ բացվում են, երրորդները յուրահատուկ կերպով միանում են ներբջջային միջնորդներին։ Մեմբրանային ռեցեպտորների մոլեկուլի այն մասը, որը միանում է ազդանշանային մոլեկուլին, գտնվում է բջջի մակերեսին, իսկ ազդակը փոխանցող դոմենը՝ ներսում[79]։
Շարժողական ֆունկցիա[խմբագրել | խմբագրել կոդը]

Շարժողական սպիտակուցների մի ամբողջ խումբ ապահովում է օրգանիզմի շարժումը՝ մկանների կծկումը, այդ թվում լոկոմոցիան (միոզին), օրգանիզմում բջիջների շարժը (օրինակ՝ լեյկոցիտների ամեոբաձև շարժումը), թարթիչների և մտրակների շարժումը, ինչպես նաև ներբջջային ակտիվ ուղղորդված տրանսպորտը՝ կինեզին, դինեին։ Դինեինները և կինեզինները մոլեկուլի տեղափոխումն իրականացնում են միկրոխողովակների երկարությամբ՝ ԱԵՖ-ի հիդրոլիզի էներգիայի հաշվին։ Դինեինները տեղափոխում են մոլեկուլները և օրգանոիդները բջջի ծայրամասային հատվածներից դեպի ցենտրոսոմ, կինեզինները՝ հակառակ ուղղությամբ[80][81]։ Դինեինները ապահովում են նաև էուկարիոտների թարթիչների և մտրակների շարժումը։ Միոզինի ցիտոպլազմային ձևերը կարող են մասնակցել միկրոֆիլամենտներով մոլեկուլների և օրգանոիդների շարժին։
Սպիտակուցները նյութափոխանակության մեջ[խմբագրել | խմբագրել կոդը]
Միկրօրգանիզմների և բույսերի մեծ մասն ընդունակ են սինթեզել 20 ստանդարտ ամինաթթուները և այլ լրացուցիչ՝ ոչ ստանդարտ, ինչպիսին օրինակ՝ ցինտրուլինն է։ Եթե ամինաթթուները կան արտաքին միջավայրում, նույնիսկ միկրօրգանիզմներն են պահպանում էներգիան՝ ամինաթթուները տեղափոխելով բջջի ներս և անջատելով կենսասինթետիկ ուղիները[82]։
Այն ամինաթթուները, որոնք կենդանիների օրգանիզմում չեն կարող սինթեզվել անվանվում են՝ անփոխարինելի ամինաթթուներ։ Կենսասինթեզի հիմնական ֆերմենտները, օրինակ՝ ասպարտատկինազը, որը կատալիզում է լիզինի, մեթիոնինի և թրեոնինի ձևավորման առաջին ռեակցիան, բացակայում են կենդանիների մոտ։
Կենդանիները հիմնականում ամինաթթուներն ստանում են սննդի սպիտակուցներից։ Սպիտակուցները քայքայվում են մարսողության ընթացքում, սպիտակուցները թթվային միջավայրում և պրոտեազների միջոցով բնափոխվում են։ Որոշ ամինաթթուներ օգտագործվում են սպիտակուցների սինթեզում, իսկ մնացածը գլյուկոնեոգենեզի ընթացքում վերածվում են գյուկոզի կամ օգտագործվում են Կրեբսի ցիկլում։ Որպես էներգիա սպիտակուների կիրառումը հատկապես կարևոր է քաղցի ժամանակ, երբ օրգանիզմի սեփական սպիտակուցները, հատկապես՝ մկանների սպիտակուցները ծառայում են էներգիայի աղբյուր[83]։ Ամինաթթուները նաև օրգանիզմի համար ազոտի աղբյուր են։
Սպիտակուցների սննդում օգտագործման որոշակի չափանիշ մարդու համար չկա։ Հաստ աղիքի միկրոֆլորայի կողմից սինթեզվում են այնպիսի ամինաթթուներ, որոնք հաշվի չեն առնվում սպիտակուցային նորմերի կազման մեջ։
Ուսումնասիրման մեթոդներ[խմբագրել | խմբագրել կոդը]
Սպիտակուցների կառուցվածը և ֆունկցիաներն ուսումնասիրում են ինչպես in vitro՝ մաքրված պրեպարատների վրա, այնպես էլ in vivo՝ օրգանիզմի բնական միջավայրում։ Մաքուր սպիտակուցների ուսումնասիրումը կառավարելի պայմաններում կարևոր թ կինետիկ առանձնահատկությունների, ֆերմենտների կատալիտիկ ակտիվության և այլ ֆունկցիաների որոշման համար։In vivo ուսումնասիրությունը թույլ է տալիս պարզել, թե սպիտակուցը որտեղ է ակտիվ և ինչ ֆունկցիա է կատարում[84]։
Մոլեկուլային և բջջային կենսաբանություն[խմբագրել | խմբագրել կոդը]

Մոլեկուլային կենսաբանության մեթոդներն օգտագործվում են բջջում սպիտակուցների սինթեզը և տեղադրությունը ուսումնասիրելու նպատակով։ Լայնորեն կիրառվում է սպիտակուցների տեղագրությունը, որը հիմնված է բջջում քիմերային սպիտակուցների սինթեզի վրա, քիմերային սպիտակուցը կազմված է ուսումնասիրման ենթակա սպիտակուցից միացած այլ սպիտակուցի, օրինակ՝ կանաչ ֆլուրիսցենտ սպիտակուցի հետ (GFP)[85]: Այս սպիտակուցի տեղադրությունը կարելի է տեսնել ֆլոուրիսցենտ մանրադիտակի օգնությամբ[86]։ Բացի այդ, սպիտակուցների տեղադրությունը կարելի է որոշել նաև նրանց միացող հակամարմինների միջոցով, որոնք իրենց հերթին կրում են ֆլոուրիսցենտ նշում։ Հաճախ ուսումնասիրվող սպիտակուցի հետ պատկերում են նաև օրգանոիդների սպիտակուցները, որը թույլ է տալիս ավելի ճշգրիտ որոշել սպիտակուցի տեղադրությունը բջջում[87]։
Իմունոքիմիական մեթոդներում կիրառվում են ֆերմենտների հետ կոնյուգացվող հակամարմիններ, որի արդյունքը բերում է ռեակցիայի գունավորմանը, ինչը հնարավոր է դառնում քանակապես որոշել։ Ավելի հազվադեպ օգտագործվում է բջջային ֆրակցիաների սպիտակուցների ուլտրացենտրիֆուգման մեթոդը՝ սախարոզի կամ ցեզիումի քլորիդի հետ[88][89]։
Դասական մեթոդներից է նաև իմունոէլեկտրոնային միկրոսկոպիան, որը սկզբունքորեն նման է իմունոֆլոուրիսցենտ միկրոսկոպիային, այն տարբերությամբ, որ օգտագործվում է էլեկտրոնային մանրադիտակ։ Ուսումնասիրման ենթակա նմուշը պատրաստվում է էլեկտրոնային մանրադիտակով ուսումնասիրման, մշակվում հակամարմիններով, որոնք իրենց հերթին միացած են էլեկտրոնային-դիմացկուն նյութի, որպես կանոն՝ ոսկու հետ[90]։
Սայտ-ուղղորդված մուտագենեզի միջոցով հետազոտողները կարող են որոշել սպիտակուցի ամինաթթվային հաջորդականությունը, արդյունքում՝ նրա տարածական կառուցվածքը, տեղադրությունը բջջում և ակտիվության կարգավորումը։ Այս մեթոդի և փՌՆԹ-երի միջոցով[91] հնարավոր է նաև սպիտակուց մտցնել սինթետիկ ամինաթթուներ և ստանալ նոր հատկություններով սպիտակուցներ[92]։
Կենսաքիմիա[խմբագրել | խմբագրել կոդը]

Սպիտակուցի in vitro անալիզի համար, սպիտակուցը պետք է մաքրված լինի բջջային բաղադրամասերից։ Այս գործընթացը սովորաբար սկսվում է բջջի քայքայումով և այսպես կոչված բջջային էքստրակտի ստացումով։ Ապա ցենտրիֆուգման և ուլտրացենտրիֆուգման մեթոդներով այս էքստրակտը բաժանվում է ֆրակցիաների, որոնք պարունակում են՝ լուծված սպիտակուցները, մեմբրանային լիպիդները և սպիտակուցները, բջջի օրգանոիդները և նուկլեինաթթուները։
Աղայնացման մեթոդով սպիտակուցների նստեցումը կիրառվում է սպիտակուցային խառնուրդների բաժանման համար, նաև թույլ է տալիս խտացնել սպիտակուցները։ Սեդիմենտացիոն անալիզը (ցենտրիֆուգացումը) թույլ է տալիս ըստ սվեդբերգներով (S) չափվող սեդիմենցիայի հաստատունի արժեքի շերտավորել սպիտակուցային խառնուրդները[93]։ Անհրաժեշտ մոլեկուլային զանվածին, լիցքին, աֆինությանը համապատասխանող սպիտակուցները առանձնացնելու համար հետագայում խառնուրդը բաժանվում է քրոմատոգրաֆիայով[94][95]։ Բացի այդ, սպիտակուցները կարող են բաժանվել իրենց լիցքի հիման վրա՝ էլեկտրաֆոկուսավորման միջոցով[96]։
Սպիտակուցների մաքրման գործընթացը պարզեցնելու նպատակով, հաճախ օգտագործում է գենետիկական ինժեներիան, որը թույլ է տալիս ստեղծել սպիտակուցների ածանցյալներ։
«Նշագրերը» (մարկերները) կարճ ամինաթթվային հաջորդականություններ են, օրինակ՝ հիստիդինի 6 և ավելի մնացորդներից կազմված շղթաներ, որոնք ամրանում են սպիտակուցի ծայրերից մեկին։ Երբ համապատասխան նշագրված սպիտակուցը սինթեզած բջիջների էքստրակտը անցկացնում են նիկելի իոններ պարունակող քրմոատոգրաֆի միջով, հիստիդինը կապվում է նիկելի հետ և ամրանում քրոմատոգրաֆի սյունակին, իսկ լիզատի մյուս բաղադրամասերը առանց որևէ արգելքի անցնում են սյունակով։ Աֆինային քրոմատոգրաֆիայի միջոցով տարբեր սպիտակուցներ առանձնացնելու համար նախագծված են այլ նշագրեր նույնպես[97]։
Սպիտակուցի մաքրության աստիճանը կարելի է որոշել, երբ տարբեր տեսակի գել-էլեկտրոֆորեզների միջոցով հայտնի է սպիտակուցի մոլեկուլային զանգվածը և իզոէլեկտրական կետը, նաև՝ ֆերմենտային ակտիվության չափմամբ, եթե սպիտակուցը ֆերմենտ է։ Մաս սպետկրոմետրիան թույլ է տալիս նույնականացնել առանձնացված սպիտակուցը ըստ մոլեկուլային զանգվածի և հատվածի զանգվածով[98]։
Նմուշում սպիտակուցների քանակի որոշման համար, օգտագործվում են մի շարք մեթոդներ[99]
- բիուրետային մեթոդ
- միկրոբիուրետային մեթոդ
- Բրեդֆորդի մեթոդ
- Լոուրիի մեթոդ
- սպեկտրոֆոտոմետրիկ մեթոդ
Պրոտեոմիկա[խմբագրել | խմբագրել կոդը]
Բջջի սպիտակուցների ընդհանրությունն կոչվում է պրոտեոմ, իսկ պրոտեոմի հետազոտությունը՝ պրոտեոմիկա՝ գենոմիկայի նմանությամբ։ Պրոտեոմիկայի հիմնական էքսպերիմենտալ մեթոդները ներառում են՝
- 2D-էլեկտրոֆորեզը, որը թույլ է տալիս առանձնացնել բազմաբաղադրիչ սպիտակուցային խառնուրդները[100],
- մաս-սպեկտրոմետրիա, որը թույլ է տալիս նույնականացնել սպիտակուցներն՝ ըստ նրանց կազմի մեջ մտնող մեծ թափանցելիություն ունեցող պեպտիդների մոլեկուլային զանգվածի[101];
- սպիտակուցային միկրոչիպեր, որոնք թույլ են տալիս միաժամանակ չափել մեծ քանակով սպիտակուցների պարունակությունը բջջում[102];
- խմորասնկային երկհիբրիդային սքրինինգ (անգլ.՝ Two-hybrid screening), որը թույլ է տալիս ուսումնասիրել սպիտակուց-սպիտակուցային փոխհարաբերությունները[103]
Կենսաբանորեն նշանակալի սպիտակուցների բոլոր փոխհարաբերությունների ամբողջությունն անվանում են ինտերակտ[104]։ Սպիտակուցների կառուցվածքի համակարգային ուսումնասիրությունը, որը ներկայացնում է երրորդային կառուցվածքի բոլոր հնարավոր տեսակները, անվանում են կառուցվածքային գենոմիկա[105]։
Կառուցվածքի կանխագուշակում և մոդելավորում[խմբագրել | խմբագրել կոդը]

Սպիտակուցի տարածական կառուցվածքի կանխագուշակումը համակարգչային տեխնիկայի միջոցով (in silico) թույլ է տալիս կառուցել սպիտակուցների մոդելներ, որոնց կառուցվածքը դեռևս չի որոշվել փորձնականորեն[106]։ Ամենահաջող կանխագուշակման ձևը կոչվում է հոմոլոգ մոդելավորում և հիմնվում է գոյություն ունեցող կաղապարային կառույցի վրա, որը ամինաթթվային հաջորդականությամբ նման է մոդելավորվող սպիտակուցին[107]։ Սպիտակուցների տարածական կառուցվածքի կանխագուշակման մեթոդները լայնորեն կիրառվում են սպիտակուցների գենային ինժեներիայի զարգացման ուղղության մեջ․ մեթոդների միջոցով ստացվում են սպիտակուցի նոր երրորդային կառույցներ[108]։ Ավելի բարդ խնդիր է միջմոլեկուլային փոխհարաբերությունների և սպիտակուց-սպիտակուց փոխհարաբերությունների կանխագուշակումը[109]։
Ֆոլդինգը և միջմոլեկուլային փոխազդեցությունները կարող են մոդելավորվել մոլեկուլային մեխանիկայի և հատկապես մոլեկուլային դինամիկայի ու Մոնտե Կառլոյի մեթոդի միջոցով, որոնք ավելի ու ավելի շատ են կիրառում զուգահեռ և ցրված հաշվարկման առավելությունները (օրինակ՝ Folding@home նախագիծը[110])։ Փոքր α-պարույրավոր սպիտակուցների դոմենների ֆոլդինգը, ինչպիսին, օրինակ, վիլինն է[111] կամ ՄԻԱՎ-ի սպիտակուցներից մեկը[112], հաջողությամբ մոդելավորվել է in silico: Մոլեկուլային դինամիկան քվանտային մեխանիկայի հետ միավորող հիբրիդային մեթոդների օգնությամբ ուսումնասիրվել է տեսողական ռոդոպսին գունանյութի էլեկտրոնային վիճակը[113]։
Տես նաև[խմբագրել | խմբագրել կոդը]
Նշումներ[խմբագրել | խմբագրել կոդը]
- ↑ Քիմիական տեսակետից բոլոր սպիտակուցները պոլիպեպտիդներ են։ Սակայն կարճ, մինչև 30 ամինաթթվային մնացորդներ պարունակող պոլիպեպտիդները, հատկապես, երբ արհեստական են սինթեզվել, սպիտակուցներ չեն անվանվում
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Perutz M. F., Rossmann M. G., Cullis A. F., Muirhead H., Will G., North A. C. Structure of haemoglobin: a three-dimensional Fourier synthesis at 5.5-A. resolution, obtained by X-ray analysis // Nature. — 1960. — В. 4711. — Т. 185. — С. 416-422. — PMID 18990801.
- ↑ Kendrew J. C., Bodo G., Dintzis H. M., Parrish R. G., Wyckoff H., Phillips D. C. A three-dimensional model of the myoglobin molecule obtained by x-ray analysis // Nature. — 1958. — В. 4610. — Т. 181. — С. 662-666. — PMID 13517261.
- ↑ 3,0 3,1 3,2 Ю. А. Овчинников Биоорганическая химия. — Москва: Просвещение, 1987. — С. 24-26.
- ↑ Henry Leicester Berzelius, Jöns Jacob // Dictionary of Scientific Biography 2. — New York: Charles Scribner’s Sons, 1980. — С. 90-97. — ISBN 0-684-10114-9
- ↑ Данилевский А.Я. Биолого-химические сообщения о белковых веществах (материалы для химической конституции и биогенеза их). — Физиологический сборник. — 1888. — Т. 1. — С. 289.
- ↑ Цветков Л. А. § 38. Белки // Органическая химия. Учебник для 10 класса. — 20-е изд. — М.: Просвещение, 1981. — С. 184-193. — 1 210 000 экз.
- ↑ Белки // Химическая энциклопедия. — Москва: Советская энциклопедия, 1988.
- ↑ 8,0 8,1 N. H. Barton, D. E. G. Briggs, J. A. Eisen Evolution. — Cold Spring Harbor Laboratory Press, 2007. — С. 38. — ISBN 978-0-87969-684-9
- ↑ «Нобелевская лекция Ф. Сэнгера» (PDF). Արխիվացված (PDF) օրիգինալից 2013 թ․ հունվարի 5-ին. Վերցված է 2013 թ․ հունվարի 3-ին.
- ↑ Sanger F., Tuppy H. The amino-acid sequence in the phenylalanyl chain of insulin. 2. The investigation of peptides from enzymic hydrolysates // Biochem J. — 1951. — В. 4. — Т. 49. — С. 481-490. — PMID 14886311.
- ↑ Sanger F., Thompson E. O. The amino-acid sequence in the glycyl chain of insulin. II. The investigation of peptides from enzymic hydrolysates // Biochem J. — 1953. — В. 3. — Т. 53. — С. 366-374. — PMID 13032079.
- ↑ Овчинников Ю.А., Браунштейн А.Е., Егоров Ц.А., Поляновский О.Л., Алданова Н.А., Фейгина М.Ю., Липкин В.М., Абдулаев Н.Г., Гришин Е.В., Киселев А.П., Модянов Н.Н., Носиков В.В. Полная первичная структура аспартат-аминотрансферазы // Докл. АН СССР. — 1972. — Т. 207. — С. 728-731.
- ↑ Филиппович Ю.Б. Белки и их роль в процессах жизнедеятельности // Книга для чтения по органической химии. Пособие для учащихся. — М.: Просвещение, 1975. — С. 216-234.
- ↑ «Protein Data Bank». Rutgers and UCSD. Արխիվացված է օրիգինալից 2012 թ․ դեկտեմբերի 27-ին. Վերցված է 2012 թ․ դեկտեմբերի 26–ին-ին.
- ↑ Yahav T., Maimon T., Grossman E., Dahan I., Medalia O. Cryo-electron tomography: gaining insight into cellular processes by structural approaches // Curr Opin Struct Biol. — 2011. — В. 5. — Т. 21. — С. 670-677. — PMID 21813274.
- ↑ Fulton A., Isaacs W. Titin, a huge, elastic sarcomeric protein with a probable role in morphogenesis // Bioessays. — 1991. — В. 4. — Т. 13. — С. 157-161. — PMID 1859393.
- ↑ 17,0 17,1 17,2 17,3 Х.-Д. Якубке, Х. Ешкайт Глава 3.5 Физико-химические свойства // Аминокислоты, пептиды, белки. — Москва: Мир, 1985. — С. 356-363.
- ↑ EC 3.4.23.1 - pepsin A Пепсин А в информационной системе BRENDA
- ↑ 19,0 19,1 А. Н. Несмеянов, Н. А. Несмеянов. «Начала органической химии. Книга вторая». էջ 221. Արխիվացված օրիգինալից 2012 թ․ դեկտեմբերի 27-ին. Վերցված է 2012 թ․ դեկտեմբերի 26-ին.
- ↑ Singer S. J. The structure and insertion of integral proteins in membranes // Annu Rev Cell Biol. — 1990. — Т. 6. — С. 247-296. — PMID 2275815.
- ↑ Страйер Л. Биохимия в 3 томах. — Москва: Мир, 1984.
- ↑ 22,0 22,1 Ленинджер А. Основы биохимии в 3 томах. — Москва: Мир, 1985.
- ↑ Koonin E. V., Tatusov R. L., Galperin M. Y. Beyond complete genomes: from sequence to structure and function // Curr Opin Struct Biol.. — 1998. — В. 3. — Т. 8. — С. 355-363. — PMID 9666332.
- ↑ David Whitford Proteins: Structure and Function. — Wiley, 2005. — С. 41. — P. 542. — ISBN 978-0471498940
- ↑ 25,0 25,1 25,2 25,3 David Whitford Proteins: Structure and Function. — Wiley, 2005. — С. 45. — P. 542. — ISBN 978-0471498940
- ↑ 26,0 26,1 Финкельштейн А. В., Птицын О. Б. Лекция 15 // Физика белка. — Москва: КДУ, 2005. — С. 189-205.
- ↑ А. Н. Несмеянов, Н. А. Несмеянов. «Начала органической химии. Книга первая». էջ 331. Արխիվացված օրիգինալից 2012 թ․ դեկտեմբերի 27-ին. Վերցված է 2012 թ․ դեկտեմբերի 26-ին.
- ↑ Шрёдингер Э. Что такое жизнь с точки зрения физики? = пер. с англ. А.А. Малиновского. — Москва: РИМИС, 2009. — С. 176. — ISBN 978-5-9650-0057-9
- ↑ Волькенштейн М.В. Биофизика. — Москва: Наука, 1988.
- ↑ Huber R. Conformational flexibility in protein molecules // Nature. — 1979. — В. 5723. — Т. 280. — С. 538-539. — PMID 460436.
- ↑ Richards F. M. Areas, volumes, packing and protein structure // Annu Rev Biophys Bioeng. — 1977. — Т. 6. — С. 151-176. — PMID 326146.
- ↑ Привалов П.Л. Стабильность белков и гидрофобные взаимодействия // Биофизика. — 1987. — В. 5. — Т. 32. — С. 742-760. — PMID 3318936.
- ↑ Морозов В. Н., Морозова Т. Я. Механические свойства глобулярных белков // Молекулярная биология. — 1983. — В. 3. — Т. 17. — С. 577-586. — PMID 6877232.
- ↑ Doster W., Cusack S., Petry W. Dynamical transition of myoglobin revealed by inelastic neutron scattering // Nature. — 1989. — В. 6209. — Т. 337. — С. 754-756. — PMID 2918910.
- ↑ Parak F., Frolov E. N., Mössbauer R. L., Goldanskii V. I. Dynamics of metmyoglobin crystals investigated by nuclear gamma resonance absorption // J Mol Biol. — 1981. — В. 4. — Т. 145. — С. 825-833. — PMID 7265223.
- ↑ Шайтан К.В., Рубин А.Б. Стохастическая динамика и электронно-конформационные взаимодействия в белках // Биофизика. — 1985. — В. 3. — Т. 30. — С. 517-526. — PMID 3896324.
- ↑ 37,0 37,1 37,2 Спирин А. С. Глава II. Информационная РНК и генетический код // Молекулярная биология. Структура рибосомы и биосинтез белка. — Москва: Высшая школа, 1986. — С. 9-16.
- ↑ Benjamin Lewin Genes VIII. — Upper Saddle River, NJ: Pearson Prentice Hall, 2004. — ISBN 0131439812
- ↑ Dobson C. M. The nature and significance of protein folding // Mechanisms of Protein Folding / Pain R. H.. — 2nd. — New York, NY: Oxford University Press, 2000.
- ↑ Stack D., Neville C., Doyle S. Nonribosomal peptide synthesis in Aspergillus fumigatus and other fungi // Microbiology. — 2007. — В. Pt 5. — Т. 153. — С. 1297-1306. — PMID 17464044.(չաշխատող հղում)
- ↑ Welker M., von Döhren H. Cyanobacterial peptides - nature's own combinatorial biosynthesis // FEMS Microbiol Rev. — 2006. — В. 4. — Т. 30. — С. 530-563. — PMID 16774586.
- ↑ Wilken J., Kent S. B. Chemical protein synthesis // Curr Opin Biotechnol. — 1998. — В. 4. — Т. 9. — С. 412-426. — PMID 9720266.
- ↑ Dawson P. E., Kent S. B. Synthesis of native proteins by chemical ligation // Annu Rev Biochem. — 2000. — Т. 69. — С. 923-960. — PMID 10966479.
- ↑ Jones D. T. Protein secondary structure prediction based on position-specific scoring matrices // J Mol Biol. — 1999. — В. 2. — Т. 292. — С. 195-202. — PMID 10493868.
- ↑ Jensen O. N. Interpreting the protein language using proteomics // Nat Rev Mol Cell Biol. — 2006. — В. 6. — Т. 7. — С. 391-403. — PMID 16723975.
- ↑ Demartino G. N., Gillette T. G. Proteasomes: machines for all reasons // Cell. — 2007. — В. 4. — Т. 129. — С. 659-662. — PMID 17512401.
- ↑ Walsh G., Jefferis R. Post-translational modifications in the context of therapeutic proteins // Nat Biotechnol. — 2006. — В. 10. — Т. 24. — С. 1241-1252. — PMID 17033665.
- ↑ Rosenbaum, J. (2000). «Cytoskeleton: functions for tubulin modifications at last». Curr Biol. 10: 801–803. doi:10.1016/S0960-9822(00)00767-3. PMID 11084355.
- ↑ Bronner C., Chataigneau T., Schini-Kerth V. B., Landry Y. The "Epigenetic Code Replication Machinery", ECREM: a promising drugable target of the epigenetic cell memory // Curr Med Chem. — 2007. — В. 25. — Т. 14. — С. 2629-2641. — PMID 17979715.
- ↑ Alberts B., Johnson A., Lewis J., et al. Chapter 12. Intracellular Compartments and Protein Sorting // Molecular Biology of the Cell. 4th edition. — New York: Garland Science, 2002.
- ↑ Hegde R. S., Bernstein H. D. The surprising complexity of signal sequences // Trends Biochem Sci. — 2006. — В. 10. — Т. 31. — С. 563-571. — PMID 16919958.
- ↑ Saraogi I., Shan S. O. Molecular mechanism of co-translational protein targeting by the signal recognition particle // Traffic. — В. 5. — Т. 12. — С. 535-542.
- ↑ Alberti S. Molecular mechanisms of spatial protein quality control // Prion. — 2012. — В. 5. — Т. 6. — С. 437-442. — — PMID 23051707.
- ↑ 54,0 54,1 Shintani T., Klionsky D. J. Autophagy in health and disease: a double-edged sword // Science. — 2004. — В. 5698. — Т. 306. — С. 990-995. — PMID 15528435.
- ↑ Anfinsen C. B. Principles that Govern the Folding of Protein Chains // Science. — 1973. — В. 4096. — Т. 181. — С. 223-230. — PMID 4124164. Нобелевская лекция. Автор, совместно с Стэнфордом Муром и Уильямом Стейном, получил Нобелевскую премию по химии за «изучение рибонуклеазы, в особенности взаимоотношений между аминокислотной последовательностью фермента и его биологически активной конформацией».
- ↑ Ellis R. J., van der Vies S. M. Molecular chaperones // Annu Rev Biochem. — 1991. — Т. 60. — С. 321-347. — — PMID 1679318.
- ↑ Sun Y., MacRae T. H. The small heat shock proteins and their role in human disease // FEBS J. — 2005. — В. 11. — Т. 272. — С. 2613-2627. — PMID 15943797.
- ↑ Union of Biochemistry and Molecular Biology (NC-IUBMB). «Nomenclature Committee of the International Union of Biochemistry and Molecular Biology (NC-IUBMB)». Արխիվացված օրիգինալից 2013 թ․ հունվարի 5-ին. Վերցված է 2012 թ․ դեկտեմբերի 29-ին.
- ↑ 59,0 59,1 Lodish H, Berk A, Matsudaira P., Kaiser C. A., Krieger M., Scott M. P., Zipursky S. L., Darnell J. Chapter 3 // Molecular cell biology. — 5th. — New York: W.H. Freeman and CO, 2004. — С. 66-72. — ISBN 0-7167-4366-3
- ↑ 60,0 60,1 Сорокин А. В., Ким Е. Р., Овчинников Л. П. Протеасомная система деградации и процессинга белков // Успехи биологической химии. — 2009. — Т. 49. — С. 3-76. Архивировано из первоисточника 7 Հոկտեմբերի 2013.
- ↑ 61,0 61,1 61,2 Farrugia G., Balzan R. Oxidative stress and programmed cell death in yeast // Front Oncol. — 2012. — В. 64. — Т. 2. — — PMID 22737670.
- ↑ Kaganovich D., Kopito R., Frydman J. Misfolded proteins partition between two distinct quality control compartments // Nature. — 2008. — В. 7208. — Т. 454. — С. 1088-1095. — — PMID 18756251.
- ↑ Yannay-Cohen N., Razin E. Translation and transcription: the dual functionality of LysRS in mast cells // Mol Cells. — 2006. — В. 2. — Т. 22. — С. 127-132. — PMID 17085962.
- ↑ «База данных номенклатуры ферментов ENZYME». Արխիվացված օրիգինալից 2013 թ․ ապրիլի 28-ին. Վերցված է 2013 թ․ ապրիլի 25-ին.
- ↑ Bairoch A. The ENZYME database in 2000 // Nucleic Acids Res. — 2000. — В. 1. — Т. 28. — С. 304-305. — PMID 10592255.
- ↑ Radzicka A., Wolfenden R. A proficient enzyme // Science. — 1995. — В. 5194. — Т. 267. — С. 90-93. — PMID 7809611.
- ↑ «The Catalytic Site Atlas at The European Bioinformatics Institute». Արխիվացված է օրիգինալից 2013 թ․ օգոստոսի 3-ին. Վերցված է 2015 թ․ հուլիսի 11-ին.
- ↑ «Номенклатура ферментов на сайте Международного союза биохимии и молекулярной биологии». Արխիվացված օրիգինալից 2013 թ․ ապրիլի 28-ին. Վերցված է 2013 թ․ ապրիլի 25-ին.
- ↑ Erickson H. P. Evolution of the cytoskeleton // Bioessays. — 2007. — В. 7. — Т. 29. — С. 668-677. — PMID 17563102.
- ↑ Wolberg A. S. Thrombin generation and fibrin clot structure // Blood Rev. — 2007. — В. 3. — Т. 21. — С. 131-142. — PMID 17208341.
- ↑ Я. Кольман, К.-Г. Рем Наглядная биохимия. — Москва: Мир, 2000. — С. 308-309.
- ↑ vertebrates have potent phagocytic and microbicidal abilities // Nat Immunol. — 2006. — В. 10. — Т. 7. — С. 1116-1124. — PMID 16980980.
- ↑ Hinnebusch A. G. Translational regulation of GCN4 and the general amino acid control of yeast // Annu Rev Microbiol. — 2005. — Т. 59. — С. 407-450. — PMID 16153175.
- ↑ Повещенко А. Ф., Абрамов В. В., Козлов В. В. Цитокины - факторы нейроэндокринной регуляции // Успехи физиологических наук. — 2007. — В. 3. — Т. 38. — С. 40-46.
- ↑ Wittenberg JB. On optima: the case of myoglobin-facilitated oxygen diffusion. Gene. 2007 Aug 15. 398(1-2):156-161.
- ↑ Driessen AJ, Nouwen N. Protein Translocation Across the Bacterial Cytoplasmic Membrane. Annu Rev Biochem. 2007 Dec 13 [Epub ahead of print]
- ↑ Drory O, Nelson N. (2006). «The emerging structure of vacuolar ATPases». Physiology (Bethesda). 21: 317–325. PMID 16990452.
- ↑ Eliot M. Hermana and Brian A. Larkins Protein Storage Bodies and Vacuoles // The Plant Cell. — 1999. — Т. 11. — С. 601-613.
- ↑ Dupré DJ, Hébert TE. Biosynthesis and trafficking of seven transmembrane receptor signalling complexes. Cell Signal. 2006;18(10):1549-1559
- ↑ Karp G. Cell and Molecular Biology: Concepts and Experiments, Fourth ed, pp. 346-358. John Wiley and Sons, Hoboken, NJ. 2005.
- ↑ Schroer, Trina A. Dynactin. Annual Review of Cell and Developmental Biology. 2004 20, 759-779. PMID 15473859
- ↑ Voet D, Voet JG. Biochemistry Vol 1 3rd ed., Hoboken, NJ (2004).
- ↑ Brosnan J. (2003). «Interorgan amino acid transport and its regulation». J Nutr. 133 (6 Suppl 1): 2068S–72S. PMID 12771367.
- ↑ David Whitford Proteins: Structure and Function. — Wiley, 2005. — С. 313. — P. 542. — ISBN 978-0471498940
- ↑ Stepanenko OV, Verkhusha VV, Kuznetsova IM, Uversky VN, Turoverov KK (2008). «Fluorescent proteins as biomarkers and biosensors: throwing color lights on molecular and cellular processes». Current Protein & Peptide Science. 9 (4): 338–69. doi:10.2174/138920308785132668. PMC 2904242. PMID 18691124.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Yuste R (2005). «Fluorescence microscopy today». Nature Methods. 2 (12): 902–904. doi:10.1038/nmeth1205-902. PMID 16299474.
- ↑ Margolin W (2000). «Green fluorescent protein as a reporter for macromolecular localization in bacterial cells». Methods (San Diego, Calif.). 20 (1): 62–72. doi:10.1006/meth.1999.0906. PMID 10610805.
- ↑ Walker JH, Wilson K (2000). Principles and Techniques of Practical Biochemistry. Cambridge, UK: Cambridge University Press. էջեր 287–89. ISBN 0-521-65873-X.
- ↑ Остерман Л. А. Методы исследования белков и нуклеиновых кислот: Электрофорез и ультрацентрифугирование (практическое пособие). — М.: «Наука», 1981. — С. 240-263. — 288 с.
- ↑ Mayhew TM, Lucocq JM (2008). «Developments in cell biology for quantitative immunoelectron microscopy based on thin sections: a review». Histochemistry and Cell Biology. 130 (2): 299–313. doi:10.1007/s00418-008-0451-6. PMC 2491712. PMID 18553098.
- ↑ Hohsaka T, Sisido M (2002). «Incorporation of non-natural amino acids into proteins». Current Opinion in Chemical Biology. 6 (6): 809–15. doi:10.1016/S1367-5931(02)00376-9. PMID 12470735.
- ↑ Cedrone F, Ménez A, Quéméneur E (2000). «Tailoring new enzyme functions by rational redesign». Current Opinion in Structural Biology. 10 (4): 405–10. doi:10.1016/S0959-440X(00)00106-8. PMID 10981626.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Colea J. L., Hansenb J. C. «Analytical Ultracentrifugation as a Contemporary Biomolecular Research Tool» // J. Biomol. Techn. V 10. 1999. P. 163-176
- ↑ Murray RF, Harper HW, Granner DK, Mayes PA, Rodwell VW (2006). Harper's Illustrated Biochemistry. New York: Lange Medical Books/McGraw-Hill. ISBN 0-07-146197-3.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Остерман Л. А. Хроматография белков и нуклеиновых кислот. — Москва, 1985.
- ↑ Hey J, Posch A, Cohen A, Liu N, Harbers A (2008). «Fractionation of complex protein mixtures by liquid-phase isoelectric focusing». Methods in Molecular Biology. Methods in Molecular Biology™. 424: 225–39. doi:10.1007/978-1-60327-064-9_19. ISBN 978-1-58829-722-8. PMID 18369866.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Terpe K (2003). «Overview of tag protein fusions: from molecular and biochemical fundamentals to commercial systems». Applied Microbiology and Biotechnology. 60 (5): 523–33. doi:10.1007/s00253-002-1158-6. PMID 12536251.
- ↑ Н. А. Понькин. Что в имени твоём, масс-спектрометрия? Արխիվացված 2016-03-04 Wayback Machine сайт Всероссийского масс-спектрометрического общества
- ↑ Editor: John M. Walker The Protein Protocols Handbook. — 3. — Springer. — С. 3-69. — 1985 с. — (Springer Protocols Handbooks). — ISBN 978-1-60327-474-6
- ↑ Görg A, Weiss W, Dunn MJ (2004). «Current two-dimensional electrophoresis technology for proteomics». Proteomics. 4 (12): 3665–85. doi:10.1002/pmic.200401031. PMID 15543535.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Conrotto P, Souchelnytskyi S. Proteomic approaches in biological and medical sciences: principles and applications. // Exp Oncol.. — В. 3. — Т. 30. — С. 171-80. — PMID 18806738.
- ↑ Joos T, Bachmann J (2009). «Protein microarrays: potentials and limitations». Frontiers in Bioscience. 14 (14): 4376–85. doi:10.2741/3534. PMID 19273356.
- ↑ Koegl M, Uetz P (2007). «Improving yeast two-hybrid screening systems». Briefings in Functional Genomics & Proteomics. 6 (4): 302–12. doi:10.1093/bfgp/elm035. PMID 18218650. Արխիվացված է օրիգինալից 2013 թ․ ապրիլի 15-ին. Վերցված է 2016 թ․ հունվարի 24-ին.
- ↑ Plewczyński D, Ginalski K (2009). «The interactome: predicting the protein–protein interactions in cells». Cellular & Molecular Biology Letters. 14 (1): 1–22. doi:10.2478/s11658-008-0024-7. PMID 18839074.
- ↑ Zhang C, Kim SH (2003). «Overview of structural genomics: from structure to function». Current Opinion in Chemical Biology. 7 (1): 28–32. doi:10.1016/S1367-5931(02)00015-7. PMID 12547423.
- ↑ Zhang Y (2008). «Progress and challenges in protein structure prediction». Current Opinions in Structural Biology. 18 (3): 342–48. doi:10.1016/j.sbi.2008.02.004. PMC 2680823. PMID 18436442.
- ↑ Xiang Z (2006). «Advances in homology protein structure modeling». Current Protein and Peptide Science. 7 (3): 217–27. doi:10.2174/138920306777452312. PMC 1839925. PMID 16787261.
- ↑ Kuhlman B, Dantas G, Ireton GC, Varani G, Stoddard BL, Baker D (2003). «Design of a novel globular protein fold with atomic-level accuracy». Science. 302 (5649): 1364–68. Bibcode:2003Sci...302.1364K. doi:10.1126/science.1089427. PMID 14631033.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Ritchie DW (2008). «Recent progress and future directions in protein–protein docking». Current Protein and Peptide Science. 9 (1): 1–15. doi:10.2174/138920308783565741. PMID 18336319.
- ↑ Scheraga HA, Khalili M, Liwo A (2007). «Protein-folding dynamics: overview of molecular simulation techniques». Annual Review of Physical Chemistry. 58: 57–83. Bibcode:2007ARPC...58...57S. doi:10.1146/annurev.physchem.58.032806.104614. PMID 17034338.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Zagrovic B, Snow CD, Shirts MR, Pande VS (2002). «Simulation of folding of a small alpha-helical protein in atomistic detail using worldwide-distributed computing». Journal of Molecular Biology. 323 (5): 927–37. doi:10.1016/S0022-2836(02)00997-X. PMID 12417204.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Herges T, Wenzel W (2005). «In silico folding of a three helix protein and characterization of its free-energy landscape in an all-atom force field». Physical Review Letters. 94 (1): 018101. Bibcode:2005PhRvL..94a8101H. doi:10.1103/PhysRevLett.94.018101. PMID 15698135.
- ↑ Hoffmann M, Wanko M, Strodel P, König PH, Frauenheim T, Schulten K, Thiel W, Tajkhorshid E, Elstner M (2006). «Color tuning in rhodopsins: the mechanism for the spectral shift between bacteriorhodopsin and sensory rhodopsin II». Journal of the American Chemical Society. 128 (33): 10808–18. doi:10.1021/ja062082i. PMID 16910676.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link)
Գրականություն[խմբագրել | խմբագրել կոդը]
- Альбертс Б., Брей Д., Льюис Дж. и др. Молекулярная биология клетки. В 3 томах. — М.: Мир, 1994. — ISBN 5-03-001986-3
- Ленинджер А. Основы биохимии. В 3 томах. — М.: Мир, 1985.
- Страйер Л. Биохимия. В 3 томах. — М.: Мир, 1984.
Արտաքին հղումներ[խմբագրել | խմբագրել կոդը]
- An Introduction to Proteins
- PDB - Սպիտակուցների տվյալների բանկ (Protein Data Bank) Արխիվացված 2008-08-28 Wayback Machine (անգլ.)
- Սպիտակուցների ֆոլդինգի մասին հոդվածներ Արխիվացված 2008-09-16 Wayback Machine (ռուս.)
- Գիտահանրամատչելի ֆիլմ՝ «Սպիտակուց» (ռուս.)
- Պրոտեինները որպես սպորտային հավելում
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Սպիտակուցներ» հոդվածին։ |
| ||||||||||||||||
| Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի օրվա հոդված: |
|
|
Այս հոդվածը ներառված է Հայերեն Վիքիպեդիայի ընտրյալ հոդվածների ցանկում |
|
|
Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի՝ 2016 թվականի Տարվա հոդված |


