Կարբոնաթթուներ



Կարբոնաթթուներ՝ մոլեկուլում պարունակում են կարբօքսիլային խումբ՝ -COOH: Այս խմբի կառուցվածքային բանաձևը և կարբօքսիլ անունը ցույց է տալիս, որ այն կազմված է կարբոնիլային՝ >C=O և օքսի՝ OH, խմբերից։ Սակայն >C=O խմբի յուրահատուկ կետոնային կամ ալդեհիդային բնույթը կարբօքսիլի մոտ ոչ մի բանով չի արտահայտվում։ Կարբօքսիլի մեջ պարունակվող թթվածնի ատոմները լիովին միատեսակ են։ Դա հաստատվում է կարբոնաթթուների ֆիզիկական հատկությունների և նրանց ռենտգենյան ճառագայթների ուսումնասիրությամբ։
Թթվի հիմնայնությունը որոշվում է նրա մոլեկուլում գտնվող կարբօքսիլային խմբերի թվով՝ քացախաթթուն CH3-COOH միահիմն թթու է, թրթնջակաթթուն՝ HOOC-COOH երկհիմն թթու։
Անվանակարգ[խմբագրել | խմբագրել կոդը]
Ըստ կանոնական անվանակարգի՝ թթուների անվանումն ածանցվում է՝ համապատասխան ածխաջրածնի անվանն ավելացնելով «ա» հոդակապն ու «թթու» բառը՝ աթթու վերջամասնիկը, օրինակ՝ HCOOH-մեթանաթթու (մեթան + աթթու)։ Տեղակալիչի դիրքը կարդալու համար ընտրվում է կարբօքսիլային խումբ պարունակող ամենաերկար ածխածնային շղթան, որը համարակալվուլում են այն կողմից որին մոտ է կարբօքսիլային խումբը։
| Միջազգային անվանում | IUPAC անվանում | Բանաձև | Թթվային մնացորդի անվանումը |
|---|---|---|---|
| Մրջնաթթու | Մեթանաթթու | HCOOH | ֆորմիատ |
| Քացախաթթու | Էթանաթթու | CH3COOH | ացետատ |
| Պրոպիոնաթթու | Պրոպանաթթու | C2H5COOH | պրոպիոնատ |
| Կարագաթթու | Բութանաթթու | C3H7COOH | Բութիրատ |
| Վալերիանաթթու | պենտանաթթու | C4H9COOH | վալերիատ |
| Կապրոնաթթու | Հեքսանաթթու | C5H11COOH | կապրատ |
| Էնանտաթթու | Հեպտանաթթու | C6H13COOH | էնանտոատ |
| Կապրիլաթթու | Օկտանաթթու | C7H15COOH | կապրիլատ |
| Պելարգոնաթթու | Նոնանաթթու | C8H17COOH | պելարգոատ |
| Կապրինաթթու | Դեկանաթթու | C9H19COOH | կապրիատի |
| Ունդեցիլանաթթու | Ունդեկանաթթու | C10H21COOH | ունդեկանոատ |
| Լաուրինաթթու | Դոդեկանաթթու | C11H23COOH | լաուրատ |
| - | Տրիդեկանաթթու | C12H25COOH | տրիդեկանոատ |
| Միրիստինաթթու | Տետրադեկանաթթու | C13H27COOH | միրիստիատ |
| - | Պենտադեկանաթթու | C14H29COOH | պենտադեկանոատ |
| Պալմիտինաթթու | Հեքսադեկանաթթու | C15H31COOH | պալմիտատ |
| Մարգարինաթթու | Հեպտադեկանաթթու | C16H33COOH | մարգարատ |
| Ստեարինաթթու | Օկտադեկանաթթու | C17H35COOH | ստերատ |
| - | Նոնադեկանաթթու | C18H37COOH | նոնադեկանոատ |
| Արախինաթթու | C19H39COOH | արախատ | |
| - | Գենեյկոզանաթթու | C20H41COOH | գենեկոզանոատ |
| Բեհենաթթու | Դոկազանաթթու | C21H43COOH | բեգենատ |
| Միջազգային անվանում | IUPAC անվանում | Բանաձև | Թթվային մնացորդի անվանումը |
|---|---|---|---|
| Մրջնաթթու | Էթադիենաթթու | HOOCCOOH | օքսալատ |
| Մալոնաթթու | Պրոպանիդիոնաթթու | HOOССH2COOH | մալոնատ |
| Սաթաթթու | Բութադիոնաթթու | HOOC(СH2)2COOH | սուկցիտ |
| Գլուտարաթթու | Պենտանդիոնաթթու | HOOC(СH2)3COOH | գլուտարատ |
| Ադիպինաթթու | Հեքսադիոնաթթու | HOOC(СH2)4COOH | ադիպինատ |
| Պիմելինաթթու | Հեպտադիոնաթթու | HOOC(СH2)5COOH | պիմելինատ |
| Խցանաթթու | Օկտադիոնաթթո | HOOC(СH2)6COOH | սուբերատ |
| Ազելաինաթթու | Նոնադիոնաթթու | HOOC(СH2)7COOH | ազելաինատ |
| Սերացինաթթու | Դեկանդիոնաթթու | HOOC(СH2)8COOH | սեբացիանատ |
| - | Ունդեկանդիոնաթթու | HOOC(СH2)9COOH | |
| - | Դոդեկանդիոնաթթու | HOOC(СH2)10COOH | |
| Տրիդեկանդիոնաթթու | HOOC(СH2)11COOH | ||
| - | Տետրադեկանդիոնաթթու | HOOC(СH2)12COOH | |
| - | Պենտադեկանդիոնաթթու | HOOC(СH2)13COOH | |
| Հեքսադեկանդիոնաթթու | HOOC(СH2)14COOH | ||
| - | Հեպտադեկանդիոնաթթու | HOOC(СH2)15COOH | |
| - | Օկտադեկանդիոնաթթու | HOOC(СH2)16COOH | |
| - | Նոնադեկանդիոնաթթու | HOOC(СH2)17COOH | |
| - | - | HOOC(СH2)18COOH | |
| Հենեյկոզանդիոնաթթու ? | HOOC(СH2)19COOH |
Դասակարգում[խմբագրել | խմբագրել կոդը]

Կախված կարբօքսիլային խմբի միացած ռադիկալի բնույթից տարբերվում են՝
- սահմանային,
- ոչ սահմանային,
- արոմատիկ և այլ կարբոնաթթուներ։
Ըստ -COOH խմբի քանակի տարբերվում են
- միահիմն (քացախաթթու),
- երկհիմն (թրթնջուկաթթու),
- եռահիմն
- բազմահիմն թթուներ (կիտրոնաթթու)։
Բնության մեջ[խմբագրել | խմբագրել կոդը]
Մի շարք կարբոնաթթուների շատ մեծ տարածում ունեն բնության մեջ։
Միահիմն կարբոնաթթուների ներկայացուցիչներ[խմբագրել | խմբագրել կոդը]
Մրջնաթթուն պարունակվում է մրջյունների խայթիչ արտաթորանքներում, եղինջում և եղևնու փշատերևում։ Մրջնաթթուն օգտագործվում է գործվածքների ներկման, թանկարժեք կաշիների ստացման համար, օգտագործվում է որպես վերականգնիչ։ Մրջնաթթվի եթերները կիրառվում են որպես լուծիչներ և հոտավետ նյութեր, օրինակ՝ մրջնաթթվի ամիլեթերը։ Վալերիանաթթու պարունակվում է կատվախոտի արմատներում։ Իզովալերիանաթթուն ստանում են կատվախոտի արմատներից՝ ջրային գոլորշու հետ թորելով (նաև սինթետիկ եղանակներով)։ Օգտագործվում է դեղամիջոցներ՝ վալիդոլ, բրոմիզովալ և այլն պատրաստելու համար։ Նրա իզոամիլային եթերը՝ «խնձորի էսենցիա» օգտագործվում է սննդի արդյունաբերությունում։ Քացախաթթուն իր անվանումը ստացել է հունարեն՝ oine - գինի, և anthos - ծաղիկ բառերից։ Կարագաթթու կիրառում են որոշ հոտավետ նյութերի արտադրության համար։ Քացախաթթուն ամենալայն կիռառությամբ կարբոնաթթուն է։ Այն թույլ թթու է, ինչը հնարավոր է դարձնում քացախի օգտագործումը՝ իբրև սննդի համեմունք և պահածոների պատրաստման միջոց։ Քացախաթթվի աղերը՝ ացետատները, ուն են զանազան կիրառություններ։ Օրինակ՝ երկաթի և ալյումինի ացետատներն օգտագործվում են գործվածքները ներկելիս, նատրիումի ացետատն օգտագործում են բժշկության մեջ՝ արյան դիալիզում։ Քացախաթթուն մեծ քանակներով օգտագործվում է ացետատային մանրաթել, չայրվող կինոժապավեններ, պոլիվինիլացետատային պլաստմասաներ, դեղանյութեր, ներկանյութեր, հոտավետ նյութեր և լուծիչներ ստանալու համար։ Քացախաթթվի մի քանի ածանցյալներ գյուղատնտեսությունում կիրառվում են մոլախոտերի դեմ պայքարելու համար։ Ստեարինաթթուն և պալմիտինաթթուն գլիցերին և էսթերների ձևով մտնում են կենդանական և բուսական ճարպերի բաղադրության մեջ։ Այս թթուների նատրիումական աղերը՝ պալմիտատները և ստեարատները, ջրում լուծվում են, օժտված են լվացող հատկությամբ և կազմում են սովորական պինդ օճառի հիմնական մասը։ Օլեինաթթուն մտնում է ճարպերի բաղադրության մեջ։
Երկհիմն կարբոնաթթուների ներկայացուցիչներ[խմբագրել | խմբագրել կոդը]
- Թրթնջակաթթու - (НООС-СООН), տարածված է բնության մեջ։ Պարունակում է թրթնջուկում, ինչպես նաև խավրծիլում։ Թրթնջկաթթուն և նրա օքսալատները, կիրառվում են գործվածքների վրայից ժանգագծերը հեռացնելու համար։ Օքսալատներից, օրինակ գլիցինը կիրառում են նյութափոխանակության խանգարումների դեպքում։
- Մալոնաթթու - (НООС-(СН2)-СООН) իր անունը ստացել է լատին․՝ malum - խնձոր բառից։
- Ֆումարաթթու (լատին․՝ fumus - ծուխ), հայտնաբերվել է Fumaria officinalis (ծխաբույս) բույսում և շատ սնկերի մեջ։
- Մալեինաթթու, իր անունը ստացել է խնձորաթթվի լատին․՝ acidum malicum անունից։
- Գլուտարաթթու - (НООС-(СН2)3-СООН) ստացվել է գլուտամինաթթվի սինթեզից։ Անունը ստացել է լատին․՝ gluten - սոսինձ բառից, հայտնաբերվել է ցորենի հասկում։
Ստացում[խմբագրել | խմբագրել կոդը]
Հայտնի են կարբոնաթթուների ստացման մի շարք ընդհանուր եղանակներ։ Առաջնային ալկոհոլների և ալդեհիդների օքսիդացում։
Կարբոնաթթուների ստացման լաբարատոր եղանակները[խմբագրել | խմբագրել կոդը]
Օքսիդացման եղանակ[խմբագրել | խմբագրել կոդը]
- Կարբոնաթթուների ստացման հիմանակն եղանակը համապատասխան ալդեհիդի օքսիդացումն է։
- Սպիրտների օքսիդացումից։ Ուժեղ օքսիդիչի առկայությամբ սպիրտների օքսիդացումից կարելի է ստանալ թթուներ[1].
- Ալկիններ օքսիդացումով Ti (III) միացությունների հետ.
- Ալկենների օքսիդատիվ քայքայումով, ռեակցիան ընթանում է երկու փուլով.
Ալկիլբենզոլի և այլ ալկիլների օքսիդացումով.
Հիդրոլիզ[խմբագրել | խմբագրել կոդը]
- Նիտրիլների հիդրոլիզով.
- Բարդ եթերների հիդրոլիզով.
- Նիտրիլների և ամիդների հիդրոլիզով.
Մեթիլյոդիդը կալիումի ցիանիդով մշակելիս առաջանում է մեթիլցիանիդ (հեղուկ, որը եռում է 81,5 °C-ում)։ Նոսր անօրգանական թթուների հետ տաքացնելիս մեթիլցիանիդը, իրեն միացնում է ջուր և ժեղքվում ամոնիակի ու քացախաթթվի։ Ալկիլցիանիդները հիդրոլիզի ժամանակ փոխարկվում են նույն թվով ածխածնի ատոմներ ունեցող թթուների, ուստի նրանց անվանում են թթուների նիտրիլներ՝ մեթիլցիանիդ կամ ացետոնիտրիլ, էթիլցիանիդ կամ պրոպիոնաթթվի նիտրիլ։ Այս ռեակցիան կարող է ապացույցը հանդիսանալ թթուների կառուցվածքի համար։
Կարբօքսիլացում[խմբագրել | խմբագրել կոդը]
- Մետաղօրգանական միացությունների կարբօքսիլացում.
- Լիթիումի դիզոպրոպիլամիդի օգնությամբ.
Արոմատիկ թթուների սինթեզ[խմբագրել | խմբագրել կոդը]
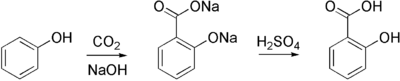
- Կոլբե-Շմիտի ռեակցիաայի վրա են հիմնված ֆենոլից սալիցիլաթթվի, մ-֊ամինաֆենոլից պ-ամինասալիցիլաթթվի (ՊԱՍԹ), ß-օքսինավթոլից ß-օքսինավթոնաթթվի և այլ նյութերի արդյունաբերական ստացման եղանակները։
- Ֆրիդել-Կրաֆտսի ռեակցիայով։
- Ֆոն-Ռիխտերի ռեակցիայով.
Այլ եղանակներ[խմբագրել | խմբագրել կոդը]
- Արնդտա-Էյստերտի ռեակցիայով.
Արդյունաբերական եղանակ[խմբագրել | խմբագրել կոդը]
- Պարաֆինների օքսիդացումով։
- Օքսիսինթեզով.
ա) առաջին փուլում ստանում են ալդեհիդ, օքսիդացնելով համապատասխան թթուները։
բ) ստանում են սպիրտ, իսկ հետո սպիրտների օգնությամբ հալում 250-350 °C-ում։
գ)
Չհագեցած թթուների ստացումը[խմբագրել | խմբագրել կոդը]
- Կարբոքսիլային խմբի թթուները օլեֆում.
- Հիմնված է սահմանային թթուների վրա և հանգեցնում է չհագեցածի.
Ֆիզիկական հատկություններ[խմբագրել | խմբագրել կոդը]

Կարբոնաթթուների ֆիզիկական և քիմիական հատկությունները պայմանավորված են մոլեկուլում առկա կարբօքսիլային խմբի էլեկտրոնային կառուցվածքով։
Կարբոքսիլային խումբը ներառում է երկու ֆունկցիոնալ խումբ՝
- կարբոնիլ
- կարբօքսիլ
որոնք փոխադարձաբար ազդում են միմյանց վրա։ Այդ ազդեցությունը փոխանցվում sp²-հիբրիդային վիճակում գտնվող ատոմներին O-C-O համակարգով։
Կարբոնիլային խմբի ածխածնի ատոմը sp² հիբրիդային վիճակում է և թթվածնի հետ առաջացնում է կրկնակի կապ, որի -կապի էլեկտրոնային զույգը շեղված է դեպի առավել էլեկտրաբացասական թթվածնի ատոմը, ինչի շնորհիվ կարբոնիլային ածխածինը ձեռք է բերում մասնակի դրական լիցք։ Լիցքերի հավասարակշռման միտումով մասնակի դրական լիցքով կարբոնիլային ածխածինը դեպի իրեն ձգում հիդրօքսիլային խմբի թթվածնի էլեկտրոնային ամպը, այդ թթվածինն էլ իր հերթին դեպի իրեն է ձգում O-H կապի էլեկտրոնային զույգը։ Դրա հետևանքով այդ կապը դառնում է ավելի բևեռային՝ պայմանավորելով OH խմբի ջրածնի ատոմը շարժունակությունը՝ կարբոնաթթուների թթվային հատկությունները։ Կարբօքսիլային խմբի ջրածնի և թթվածնի ատոմներն ընդունակ են առաջացնելու միջմոլեկուլային ջրածնային կապեր, ինչն էլ մեծ չափով պայմանավորում է կարբոնաթթուների ֆիզիկական հատկությունները։
Ասոցման հետևանքով կարբոնաթթուներն օժտված են եռման և հալման բարձր ջերմաստիճաններով։ Սովարական պայմաններում կարբոնաթթուները հեղուկներ են կամ պինդ նյութեր։ Նոնանաթթվից սկսած՝ ջրում չլուծվող պինդ նյութեր են։ Մաքուր անջուր քացախաթթուն մինչև 16,8 °C սառեցնելիս փոխարկվում է թափանցիկ բյուրեղների և նմանվում սառույցի։
Կարբոնաթթուների լուծելիությունը ջրում նույնպես պայմանավորված է լուծիչի մոլեկուլների հետ ծագող միջմոլեկուլային ջրածնային կապերով։
Հոմոլագիական շարքի ցածր անդամները ջրի հետ անսահմանափակ խառնվում են, մոլեկուլային զանգվածի մեծացման հետ լուծելիությունը փոքրանում է։ Բարձր անդամները ջրում չլուծվող պինդ նյութեր են։
Կառուցվածք[խմբագրել | խմբագրել կոդը]
Կարբօքսիլային խումբը հարթ, C=O կրկնակի կապով, տարբեր թթուներում կազմում է 0,118-0,126 նմ, կապերը, C-O - 0,121-0,137 նմ։ Կարբոնիլային խմբի ածխածնի ատոմը sp2 հիբրիդային վիճակում է և թթվածնի[2] հետ առաջացնում է կրկնակի կապ, տարբեր թթուներում O-C-O անկյունը կազմում է 118-122,5°:
Կարբօքսիլային խմբի ջրածնի և թթվածնի ատոմներն ընդունակ են առաջացնելու միջմոլեկուլային ջրածնային կապեր, ինչն էլ մեծ չափով պայմանավորված է կարբոնաթթուների ֆիզիկական հատկություններով։
Ջրածնային կապի երկարությունը դիմերներում 0,26 նմ է։

Ուժ[խմբագրել | խմբագրել կոդը]
Կարբոնաթթուները թույլ թթուներ են, մեծ թվով ալիֆատիկ թթուների pKa կազմում է 4,8։ Կարբոնաթթուներում դիսոցացման աստիճանը կախված է լուծիչի բնույթից։ Հոմոլոգիական շարքի ցածր անդամները ջրի հետ անսահմանափակ խառնվում են, մոլեկուլային զանգվածի մեծացման հետ լուծելիությունը փոքրանում է։ Բարձր անդամները ջրում չլուծվող պինդ նյութեր են։
Ջրում գտնվող մեծածավալ կարբոնաթթուների pKa արժեքը 25 °C ջերմաստիճանում
| Ֆորմուլան | pKa | Ֆորմուլան | pKa |
|---|---|---|---|
| СF3COOH | 0,23 | СCl3COOH | 0,64 |
| CHCl2COOH | 1,26 | CH2NO2COOH | 1,48 |
| CF3SO2CH2COOH | 1,88 | CH3SO2CH2COOH | 2,36 |
| NCCH2COOH | 2,47 | CH2FCOOH | 2,59 |
| CH2ClCOOH | 2,86 | CH2BrCOOH | 2,90 |
| CH2ICOOH | 3,18 | CH2OHCOOH | 3,83 |
| C6H5CH2CH2COOH | 4,66 | CH3С≡С-СOOH | 1,84 |
| CH≡C-COOH | 2,62 | CH2CHCOOH | 4,65 |
| տրանս-CH3CH=CH-COOH | 4,68 | տրանս-C6H5CH=CH-COOH | 4,44 |
| օ-CH3OC6H4COOH | 4,08 | մ-CH3OC6H4COOH | 4,10 |
| ց-CH3OC6H4COOH | 4,50 | (CH3)3C6H4COOH | 4,20 |
| ց-(CH3)3C6H4COOH | 4,38 | ց-FC6H4COOH | 4,15 |
| ց-ClC6H4COOH | 4,00 | HCOOH | 3,75 |
| CH3COOH | 4,74 | CH3CH2COOH | 4,87 |
| CH3CH2CH2COOH | 4,81 | CH3CH(CH3)COOH | 4,84 |
| (CH3)3CCOOH | 5,03 | C6H5COOH | 4,2 |
| օ-CH3C6H4COOH | 3,91 | մ-CH3C6H4COOH | 4,25 |
| ց-CH3C6H4COOH | 4,37 | օ-O2NC6H4COOH | 2,17 |
| մ-O2NC6H4COOH | 3,46 | ց-O2NC6H4COOH | 3,43 |
| C6F5COOH | 1,75 | 2,4,6-(O2N)3C6H2COOH | 0,65 |
Կարբոնաթթուների մնացորդներ[խմբագրել | խմբագրել կոդը]
| Թթվային մնացորդներ | Անվանում | ||
|---|---|---|---|
| ացիլ խումբ | անվանում | ացիլատ խումբ | |
| Н-CO¯ | Ֆորմիլ | H-COO¯ | Ֆորմիատ |
| CH3-CO¯ | Ացետիլ | CH3-COO¯ | Ացետատ |
| СН3СН2-СО¯ | Պրոպիոնիլ | СН3СН2-СОO¯ | Պրոպիոնատ |
| СН3СН2CH2-СО¯ | Բութիրիլ | СН3СН2CH2-СОO¯ | Բութիրատ |
| С3Н7-СО¯ | Իզոբութրիլ | С3Н7-СОO¯ | իզոբութիլատ |
| СН3(СН2)3-СО¯ | Վալերիլ | СН3(СН2)3-СОO¯ | Վալերատ |
| С6H5-СО¯ | Բենզոիլ | С6H5-СОO¯ | Բենզոատ |
Քիմիական հատկություններ[խմբագրել | խմբագրել կոդը]

- Ջրածնային լուծույթում կարբոնաթթուները դիսոցվում են՝ առաջացնելով H+ իոններ.
Կարբոնաթթուները թույլ թթուներ են։ Ըստ դիսոցման աստիճանի՝ միայն մրջնաթթուն է միջին ուժի թթու։ Հոմոլոգիական շարքում մոլեկուլային զանգվածի մեծացման հետ թթվի ուժը փոքրանում է։ Պատճառն ալկիլ խմբերի էլեկտրադոնոր հատկություններն են։
- Կարբոնաթթուներն օժտված են թթուներին բնորոշ բոլոր հատկություններով. փոխազդում են ակտիվ մետաղների, հիմքերի, հիմնային օքսիդների, աղերի հետ՝ առաջացնելով համապատասխան կարբոնաթթվի աղը։
- Մետաղների հետ կարբոնաթթուների փոխազդեցությունն ավելի դանդաղ է ընթանում, քան աղաթթվի կամ նոսր ծծմբական թթվի հետ.
- Հիմքերի և հիմնային օքսիդների հետ կարբոնաթթուների փոխազդեցությունից առաջանում են աղ և ջուր.
Այս ռեակցիայի իոնական հավասարումն է.
- Աղերի հետփոխազդելիս կարբոնաթթուները արտամղում են ավելի թույլ և ցնդող թթուներ.
- Կարբոնաթթուներն օժտված են նաև որոշ յուրահատկություններով, օրինակ՝ փոխազդում են սպիրտների հետ՝ առաջացնելով էսթերներ.
- Կարբօքսիլային խումբն էլեկտրոնակցեպտոր է, առաջացնում է C-H կապի լրացուցիչ բևեռացում իրեն հարևան (α) դիրքում և մեծացնում α-ջրածնային ատոմի շարժունակությունը տեղակալման ռեակցիաներում.
Թթվի մոլեկուլում քլորի ատոմի հայտնվելն անհետևանք չի մնում։ Քլորի ազդեցության տակ թթվի դիսոցման աստիճանը մեծանում է։
- Որքան մեծ է α-դիրք մտած էլեկտրաբացասական տարրի ատոմների թիվը, այնքան ուժեղ է թթուն, օրինակ՝ եռքլորքացախաթթուն ավելի ուժեղ է, քան երկքլորքացախաթթուն, որն իր հերթին ավելի ուժեղ է, քան քլորքացախաթթուն։
- Որքան մեծ է թթվի α-դիրք մտած տարրի էլեկտրաբացասականությունը, այնքան մեծ է թթվի ուժը, օրինակ՝ ֆտորքացախաթթուն ավելի ուժեղ է, քան քլորքացախաթթուն։
- Միահիմն կարբոնաթթուներից մեկ մոլեկուլ ջուր պոկելիս ստացվում է այդ թթվի անհիդրիդը։

Ամիդների և նիտրիլների ստացում[խմբագրել | խմբագրել կոդը]
Կարբոնաթթուների ամոնիումի աղերը տաքացնելիս վերածվում են ամիդների.
Ամիդները տաքացնելով P2O5 հետ, անջատվում է ջուր և առաջանում է նիտրիլթթու
Կիրառություն[խմբագրել | խմբագրել կոդը]
Կարբոնաթթուներ հանդիսանում են միացություններ օրգանական սինթեզի արգասիքների ստացման համար, մասնավորապես կետոնների, հալոգենահիդրատների, վինիլային եթերների, հալոգենաթթուների։ Կարբոնաթթուների աղերը և ալկալիական մետաղները օգտագործում են որպես օճառ, էմուլգատոր, քսուկներ։ Թթվի եսթերները օգտագործում են որպես սննդային հավելումներ, լուծիչներ։
Մրջնաթթուն հանդիսանում է ուժեղ վերականգնիչ և ունի ուժեղ մարէասպան ազդեցություն։ Այդ հատկության շնորհիվ մեծ կիրառություն ունի բժշկության մեջ, որպես պահպանող և ախտահանող միջոց։ Ինչպես նաև կիրառում են կաշվի մշակման համար։ Մեծ կիրառություն ունեն մրջնաթթվի եթերները, հատկապես՝ մեթիլֆորմիատ, էթիլֆորմիատ և իզոամիլֆորմիատ[3]։
Քացախաթթու՝ սննդային և քիմիական արտադրությունում։ Լաքերի, լատեքսի, ացետատային մանրաթելի, դեղանյութերի արտադրությունում[4]։
Կարագաթթու էսթերները կիրառվում են օծանելիքի և սննդի արդյունաբերության մեջ՝ որպես հոտավետ նյութեր, ինչպես նաև լաքերի պլաստիֆիկատորներ։ Կենսաբանական գործոններում ունի դրական նշանակություն, հատկապես կիրառում են կարագաթթվի աղերը[5]։
Ստեարինաթթու՝ C17H35COOH օգտագործում են օրգանական սինթեզում և վերլուծական քիմիայում (պղտորաչափական եղանակով որոշում են Ca, Mg), տեխնիկական ստեարինաթթուն որպես դիսպերգատոր և վուլկանիզատոր (ռետինի արտադրությունում)։ Ստեարատները (Na, Li, Ca, Pb) մտնում են պլաստիկ քսուքների, իսկ ստեարինաթթուն և նրա էսթերները՝ օծանելիքի բաղադրության մեջ[6]։
Տես նաև[խմբագրել | խմբագրել կոդը]
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Реутов.О.А. и др. Органическая хиմия. - մ.: Биноմ. Лаборатория знаний, 2004. - Т. 3. - С. 169-269. - 544 с. - 3 000 экз. - ISBN 5-94774-112-1.
- ↑ Шабаров Ю.С. Органическая химия. - Лань, 2011. - С. 346-347. - 848 с.
- ↑ Вергунова Н. Г. Муравьиная кислота // Химическая энциклопедия / Редкол: Кнунянц И. Л. (гл. ред.) и др. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди-Полимерные. — С. 148-149.
- ↑ Присяжнюк З. П. Уксусная кислота // Химическая энциклопедия / Редкол.: Зефиров Н. С. (гл. ред.) и др. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан-Ятрохимия. — С. 32-33.
- ↑ Попова Р.Я. Масляная кислота // Химическая энциклопедия / Редкол.: Кнунянц И. Л. (гл. ред.) и др. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа-Меди. — С. 652.
- ↑ Дрозд Г. И. Стеариновая кислота // Химическая энциклопедия / Редкол.: Зефиров Н. С. (гл. ред.) и др. — М.: Большая Российская энциклопедия, 1995. — Т. 4: Полимерные-Трипсин. — С. 421.
Գրականություն[խմբագրել | խմբագրել կոդը]
- Օրգանական քիմիայի դասընթաց, Բ. Ա. Պավլով և Ա. Պ. Տերենտև
- Общая органическая химия т. 4 под ред. Д. Бартона и Д. Оллиса. М.: Химия. 1983
- Сайкс П. Механизмы реакций в органической химии. М.: Химия. 1991
- Адамс М. Карбоновые кислоты в органике. М.: Химия. 1990
- Дж. Роберт, М.Касерио "Основы органической химии" т. 1 Издание 2-е, дополненное. 1978
- Горбов А. И., Рубцов П. П. Кислоты органические // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). - СПб., 1890-1907.
Արտաքին հղումներ[խմբագրել | խմբագրել կոդը]
- Կարբոնաթթուն(ռուս.) XuMuK կայքում
- Esperienze in laboratorio - Gli acidi carbossilici
- freeware for calculations, data analysis, simulation, and distribution diagram generation
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Կարբոնաթթուներ» հոդվածին։ |
| ||||||
| Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի օրվա հոդված: |

![{\displaystyle {\mathsf {RCHO+[O]\longrightarrow \ RCOOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ef2eac97dcbeda79c5fe2fcf3a19d168e8bafca)
![{\displaystyle {\mathsf {RCH_{2}OH+[O]\longrightarrow \ RCOOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/30a60265c40a8d845d11bbd8a7e53f88364bddcd)
![{\displaystyle {\mathsf {RCCH{\xrightarrow[{Tl(NO_{3})_{3}}]{}}RCOOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1ac2280fc40c3e3b47daf81dcf51cd4d98d0c04c)
![{\displaystyle {\mathsf {R^{1}CH{=}CHR^{2}{\xrightarrow[{KMnO_{4},NaIO_{4}}]{}}R^{1}COOH+R^{2}COOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e35bae943c45d31f8b6415bd842d865d2a41807e)
![{\displaystyle {\mathsf {C_{6}H_{5}CH_{3}{\xrightarrow[{KMnO_{4}}]{}}C_{6}H_{5}COOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/81a018578126e21d42052befaa1d70967be0e7cb)






![{\displaystyle {\mathsf {RR'C{=}PPh_{3}{\xrightarrow[{CO_{2}}]{}}RR'CHCOOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c6cc1c84908057dc78e0b1f80f16fd708a3d7778)


![{\displaystyle {\mathsf {RCH_{2}OH{\xrightarrow[{NaOH}]{}}RCOOH+2H_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b6ae452f04c270f86dd28784aa81e7df32c037f)


![{\displaystyle {\mathsf {CH_{2}{=}CHCH_{3}+Cl_{2}{\xrightarrow[{}]{450C,-HCl}}CH_{2}{=}CHCH_{2}Cl{\xrightarrow[{}]{+KCN,-KCl}}CH_{2}{-}CHCH_{2}CN{\xrightarrow[{}]{+H_{2}O,-NH_{3}}}CH_{2}CHCH_{2}COOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b087782754a5cba83889b1160ac44c1d766be6d3)













