Թրթնջակաթթու
| Թրթնջակաթթու | |
|---|---|
 | |
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | թրթնջակաթթու |
| Ավանդական անվանում | Էթանդիթթու, օքսալաթթու |
| Քիմիական բանաձև | C₂H₂O₄ |
| Ֆիզիկական հատկություններ | |
| Ագրեգատային վիճակ | բյուրեղային |
| Մոլային զանգված | 1,5E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 1,9 ± 0,01 գ/սմ³[2] գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | 189,5 °C °C |
| Եռման ջերմաստիճան | 365 °C °C |
| Տրոհման ջերմաստիճան | 100-130 °C °C |
| Այրման ջերմաստիճան | 166 °C |
| Գոյացան էնթալպիա | −817,38 կՋ/մոլ կՋ/մոլ |
| Սուբլիմացիայի էնթալպիա | 90,58 կՋ/մոլ |
| Գոլորշու ճնշում | 0,001 ± 0,001 mm Hg[2] |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | 10 գ/100գ (20 °C); 25 գ/100գ (44,5 °C); 120 գ/100գ (100 °C) գ/100 մլ |
| pKa | 1,25; 4,14 |
| Կառուցվածք | |
| Բյուրեղային կառուցվածք | ասեղնաձև |
| Դիպոլ մոմենտ | 0 Կլ·մ |
| Դասակարգում | |
| CAS համար | 144-62-7 |
| PubChem | 971, 3819775, 18676629 |
| EINECS համար | 205-634-3 |
| SMILES | C(=O)(C(=O)O)O |
| ЕС | 205-634-3 |
| RTECS | RO2450000 |
| ChEBI | 946 |
| Թունավորություն | |
| ՄԲ50 | 0,2 մգ/լ |
| IDLH | 500 ± 100 mg/m³[2] |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
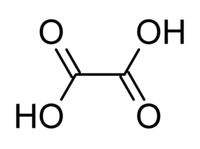
Թրթնջկաթթու (Էթանդիթթու կամ օքսալաթթու)՝ HOOC-COOH, հագեցած երկհիմն պարզ օրգանական թթու։ Թրթնջկաթթուն որպես հոմոլոգ շարքի առաջին ներկայացուցիչ, մրջնաթթվի նման, իր կառուցվածքով և քիմիական հատկություններով տարբերվում է մնացած թթուներից։
Կարբոնաթթուների բոլոր դասի ներկայացուցիչները տեղակայված են կարբօքսիլային խմբով, իսկ թրթնջկաթթվի սահմանում այն չի տարածվում։ Թրթնջկաթթուն կարելի է դիտել որպես իրար հետ կապված երկու կարբօքսիլային խմբեր։ Թրթնջկաթթուն առաջին անգամ սինթեզել է գերմանացի քիմիկոս Ֆրիդրիխ Վյոլերը 1824 թվականին։
Ստացում
[խմբագրել | խմբագրել կոդը]Թրթնջկաթթվի աղերն ստացվում են մրջնաթթվի աղերը 400 °C ում տաքացնելիս, ազատ վիճակում՝ աղերը թթուներով մշակելիս։ Թրթնջկաթթվի ստացման համար մշակված է նոր եղանակ՝ ածխածնի երկօքսիդից և ջրածնից։ Թրթնջկաթթուն բյուրեղանում է երկու մոլեկուլ ջրի հետ C2H2O4•2H2O. այն կարելի է ստանալ նաև հիդրոսկոպիկ բյուրեղների ձևով։
Թրթնջկաթթուն առաջանում է օրգանական շատ նյութերի օքսիդացման ժամանակ։ Նրա ստացման հիմնական եղանակը կայանում է փայտանյութի տաշեղները ալկալիներով մշակելու և առաջացած վերջանյութերը միաժամանակ օդի թթվածնով օքսիդացնելու մեջ։
Թրթնջկաթթվի ստացման առավել հայտնի եղանակներից է CO-ի և նատրիումի ֆորմիատի փոխազդեցությունը.
Ֆիզիկական հատկություններ
[խմբագրել | խմբագրել կոդը]Ասեղնաձև բյուրեղներ են, հալման ջերմաստիճանը՝ 189,5 °C, խտությունը՝ 1653 կգ/մ3 (18,5 °C-ում)։ Բյուրեղանում է երկու մոլեկուլ ջրի հետ՝ HOOC—COOH·H2O, անգույն բյուրեղներ են, հալման ջերմաստիճանը՝ 101,5 °C: 100 մ ջրում, 15 °C-ում լուծվում է 9,5 գրամ թրթնջկաթթու։ Առաջացնում է թթու և չեզոք աղեր, էսթերներ, ամիդներ են։ Բավականին ուժեղ թթու է. նրա էլեկտրոլիտիկ դիսոցման հաստատունը մոտավորապես 2000 անգամ ավելի մեծ է քացախաթթվի դիսոցման հաստատունից։
Քիմիական հատկություններ
[խմբագրել | խմբագրել կոդը]Արագ տաքացնելիս թրթնջկաթթուն քայքայվում է.
Եթե տաքացումը կատարվի ծծմբական թթվի ներկայությամբ, ապա ռեակցիային մասնակցող նյութերը կհանդիսանան միայն ածխաթթու գազը, ածխածնի օքսիդը և ջուրը.
Թրթնջկաթթվի բնորոշ հատկությունն այն է, որ նա հեշտությամբ օքսիդանում է, որի դեպքում առաջանում է ածխաթթու գազ և ջուր։
Լաբորատորիայում թրթնջկաթթուն հաճախ օգտագործում են քլորաջրածնի և յոդաջրածնի ստացման համար։
Ինչպես նաև թրթնջկաթթուն կիրառում են քլորի դիօքսիդի լաբորատոր սինթեզում.
Կիրառություն
[խմբագրել | խմբագրել կոդը]Տարածված է բնության մեջ, նրա թթու կալիումական աղը՝ HCOO-COOK, գտնվում է թրթնջուկի և թթվառվույտի մեջ, թրթնջակաթթվական կալցիումը՝ (COO)2Ca շատ բույսերում։
Թրթնջկաթթու տարածված է բույսերում, գլխավորապես կալցիումի աղի ձևով։ Աննշան քանակի թրթնջկաթթու կա կենդանիների և մարդու օրգանիզմում։ Թրթնջկաթթուն և նրա աղերը կիրառվում են վերլուծական քիմիայում որպես վերականգնիչներ, ինչպես նաև արհեստական ներկերի արտադրության մեջ։
Թունավորություն
[խմբագրել | խմբագրել կոդը]Թրթնջկաթթուն և նրա աղերը թունավոր են, ՍԹԿ ջրամբարի ջրերում 0,2 մգ/լ է։
Գրականություն
[խմբագրել | խմբագրել կոդը]- Օրգանական քիմիայի դասընթաց, Բ. Ա. Պավլով, Ա. Պ. Տերենտև
- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9
- Тутурин Н. Н., Щавелевая кислота // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
- Арциховский В. М., Щавелевая кислота в растениях // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
Արտաքին հղումներ
[խմբագրել | խմբագրել կոդը]- NIOSH Guide to Chemical Hazards (CDC)
- «Oxalic acid». ChemicalLand21.com. Արխիվացված է օրիգինալից 2012 թ․ հունվարի 30-ին. Վերցված է 2015 թ․ փետրվարի 17-ին.
- Table: Oxalic acid content of selected vegetables (USDA) Արխիվացված 2005-10-24 Wayback Machine
- Alternative link: Table: Oxalic Acid Content of Selected Vegetables (USDA)
- About rhubarb poisoning (The Rhubarb Compendium) Արխիվացված 2008-10-16 Wayback Machine
- Oxalosis & Hyperoxaluria Foundation (OHF) The Oxalate Content of Food 2008 (PDF) Արխիվացված 2011-09-02 Wayback Machine
Ծանոթագրություններ
[խմբագրել | խմբագրել կոդը]| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Թրթնջակաթթու» հոդվածին։ |
| ||||||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 4, էջ 227)։ |

![{\displaystyle {\mathsf {NaOH+CO\ {\xrightarrow[{}]{}}\ HCOONa{\xrightarrow[{-H_{2}}]{}}\ NaOOC{\text{-}}COONa\ {\xrightarrow[{}]{H^{+}}}\ HOOC{\text{-}}COOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4d84166b08d70e53e9b1d0973055d04009867983)



