Ամոնիակ
| Ամոնիակ | |
|---|---|
 | |
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | ամոնիակ |
| Քիմիական բանաձև | NH₃ |
| Ֆիզիկական հատկություններ | |
| Մոլային զանգված | 2,8E−26 կիլոգրամ գ/մոլ |
| Մոլյար կոնցենտրացիա cM | 17.0306 մոլ/լ |
| Խտություն | 0.0007723 գ/սմ³ գ/սմ³ |
| Իոնիզացման էներգիա | 10,18 ± 0,01 Էլեկտրոն-վոլտ[1] և 1,6E−18 ջոուլ[2] կՋ/մոլ |
| Հալման ջերմաստիճան | −77,74 °C[3][2] °C |
| Եռման ջերմաստիճան | −33,4 °C[3] °C |
| Ինքնաբռնկման ջերմաստիճան | 651 ± 1 °C[4] |
| Կրիտիկական ճնշում | 132.25 °C մթն. |
| Գոյացան էնթալպիա | −45,94 կՋ/մոլ կՋ/մոլ |
| Գոլորշու ճնշում | 8,5 ± 0,1 մթնոլորտ[1] |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | խառնուրդ գ/100 մլ |
| pKa | 9,21 ± 0,01[5] |
| Դիպոլ մոմենտ | 4,9E−30 Կլ·մ[2] |
| Դասակարգում | |
| CAS համար | 7664-41-7 |
| PubChem | 222 |
| EINECS համար | 231-635-3 |
| SMILES | N |
| ЕС | 231-635-3 |
| RTECS | BO0875000 |
| ChEBI | 217 |
| IDLH | 210 ± 10 mg/m³[1] և 300 ± 1 parts per million[1] |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Ամոնիակ, քիմիական բանաձև՝ NH3, մոլեկուլի առաջացմանը մասնակցում են ազոտի երեք չզույգված էլեկտրոնները՝ առաջացնելով երեք բևեռային կովալենտային կապեր։ Ամոնիակը հայտնի է որպես չորրորդ աստիճանի վտանգավորության գազ ըստ ԳՕՍՏ-ի 12.1.007[6]
Ամոնիակի մոլեկուլի կառուցվածքը
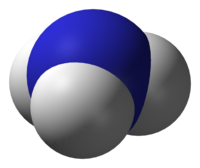
[խմբագրել | խմբագրել կոդը]Ամոնիակի մոլեկուլն ունի բրգաձև կառուցվածք. գագաթին գտնվում է ազոտի ատոմը, իսկ հիմքի երեք անկյուններում՝ ջրածնի ատոմները։ Վալենտային կապով իրար հետ միացած ատոմների միջև կազմված անկյունները՝ <HNH, հավասար են 107°: Քանի որ կապերը բևեռային են, և մոլեկուլի մի կողմում գտնվում է ազոտի ատոմը (ա) (լիցքավորված է բացասականորեն), իսկ մյուս կողմում՝ ջրածնի ատոմները (լիցքավորված են դրականորեն), ամոնիակի մոլեկուլն ամբողջությամբ վերցրած բևեռային մոլեկուլ է՝ դիպոլ (բ)։ Մոլեկուլի այսպիսի կառուցվածքով են պայմանավորված ամոնիակի ֆիզիկական և քիմիական հատկությունները։
Ամոնիակի ստացումը
[խմբագրել | խմբագրել կոդը]Լաբորատոր պայմաններում ամոնիակ ստանալու համար տաքացնում են ամոնիումի քլորիդի և կալցիումի հիդրօքսիդի պինդ խառնուրդը.
- 2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑ + 2H2O
Անջատվող գազային ամոնիակը հավաքում են շրջված փորձանոթի մեջ։
Ամոնիակի ֆիզիկական հատկությունները
[խմբագրել | խմբագրել կոդը]Ամոնիակը բնորոշ սուր հոտով անգույն գազ է, որը 1,7 անգամ թեթև է օդից։ Ջրում ամենաշատ լուծվող գազն է. 1 լիտր ջրում լուծվում է 700 լ ամոնիակ։ Սառեցնելիս և ճնշումը մեծացնելիս ամոնիակը հեշտ հեղուկանում է, իսկ գոլորշիանալիս շրջապատից խլում է մեծ քանակությամբ ջերմություն և այդ պատճառով օգտագործվում է սառնարանային կայանքներում։ Ամոնիակի հոտը զգացվում է նույնիսկ 37 մգ/մ³[7] կոնցենտրացիայի դեպքում։ Ամոնիակը հետությամբ միանում է թթուների հետ՝ առաջացնելով ամոնիումի աղեր։
Օրինակ՝
- NH3 + HCl = NH4Cl
Ինչո ՞վ է պայմանավորված երկու չեզոք մոլեկուլի միացումն իրար հետ։ Ի ՞նչ քիմիական կապ է գոյանում դրանց միջև։ Քննարկենք ամոնիումի իոնի՝ NH4-ի առաջացումը։ Ամոնիակի մոլեկուլում առկա ազոտի չօգտագործված էլեկտրոնային զույգի և էլեկտրոնից զրկված ջրածնի իոնի H+, միջև առաջանում է դարձյալ կովալենտային կապ, այսինքն՝ ընդհանրացված էլեկտրոնային զույգ։ Միայն թե այդ զույգը տրամադրում է մեկ տարր, տվյալ դեպքում՝ ազոտը, իսկ ջրածնի կատիոնը ապահովում է ազատ բջիջ (օրբիտալ), այսինքն՝ ազատ տարածք իր միջուկի շուրջը։ Էլեկտրոնային զույգ տրամադրողը՝ ամոնիակը, կոչվում է դոնոր, իսկ դատարկ օրբիտալը՝ ջրածնի իոնը՝ ակցեպտոր։ Ամոնիումի իոնում առկա է չորս կովալենտային կապ, որոնցից երեքը գոյացել է փոփոխական (յուրաքանչյուր տարրից մեկական էլեկտրոնի մասնակցությամբ), իսկ չորրորդը՝ դոնորակցեպտորային մեխանիզմով։ Սակայն բոլոր կապերն էլ իրար համարժեք են՝ ունեն նույն էներգիան և երկարությունը։
Ամոնիակի քիմիական հատկությունները
[խմբագրել | խմբագրել կոդը]Դոնորակցեպտորային կապը նույն կովալենտային կապն է, տարբերվում է միայն, ինչպես արդեն նշվեց, առաջացման ձևով։ Կովալենտային կապի այդ տեսակը հանդիպում է բազմաթիվ միացություններում։ Ամոնիումի քլորիդում ի հայտ է գալիս նաև իոնական կապ ամոնիումի (NH4+) և քլորիդ (Cl-) իոնների միջև (ջրածնի և քլորիդի միջև եղած կովալենտային կապի փոխարեն).
- NH3 + HCl → [NH]+Cl-
Ամոնիակի ջրային լուծույթը կոչվում է ամոնիակաջուր, որում ամոնիակի մոլեկուլները կապված են ջրի մոլեկուլների հետ, մասնավորապես դիպոլ-դիպոլ փոխազդեցությամբ։ Շնորհիվ ազոտի չբաժանված էլեկտրոնային զույգի՝ ամոնիակը ջրի մոլեկուլից ջրածնի մեկ ատոմ միացնում է իրեն դոնորակցեպտորային մեխանիզմով, և այդ պատճառով լուծույթում առաջանում են հիդրօքսիդային իոններ.
- NH3 + H2O→NH4+ + OH-
Ամոնիակաջուրը հաճախ անվանում են ամոնիումի հիդրօքսիդի լուծույթ, թեև չի հաջողվում լուծույթից առանձնացնել NH4OH հիդրօքսիդը։ Սակայն դրա ջրային լուծույթը ցուցաբերում է թույլ հիմնային հատկություններ։ Ամոնիակն օդում չի այրվում, սակայն այրվում է թթվածնի մթնոլորտում թույլ դեղնականաչավուն բոցով։
- 4NH3 + 3O2 = 2N2 + 6H2O
Ամոնիումի աղերը ստացվում են ամոնիակի և թթուների փոխազդեցությունից։ Դրանք օգտագործվում են հիմնականում որպես պարապտանյութեր։
- NH3 + H3PO4 = NH4H2PO4
- NH3 + HNO3 = NH4NO3
Ամոնիումի աղերը ջրում լավ լուծվող, որպես կանոն՝ սպիտակ բյուրեղային նյութեր են։ Բոլորն էլ ջերմակայուն են, տաքացնելիս քայքայվում են, ընդ որում՝ մեծ մասը ցնդում է, որովհոտև քայքայման հետևանքով գոյանում են գազեր։
- NH4Cl→NH3↑ + NHCl↑
Ամոնիումի աղերը հայտնաբերում են ալկալու միջոցով։ Չոր աղերի կամ դրանց ջրային լուծույթների վրա ալկալու լուծույթով ազդելիս առաջանում է ամոնիակին բնորոշ սուր հոտով գազ, որից լակմուսի խոնավ թուղթը կապտում է։
Օրինակ՝

- (NH4)2SO4 + 2NaOH = Na2SO4 + 2NH3↑ + 2H2O
- NH4+ + OH- = NH3 + H2O
Ամոնիակը փոխազդում է նաև մետաղների հետ։ Օրինակ՝ Cu, Fe, Hg:
- Հեղուկ ամոնիակի ջրային հատկությունները
| E° (V, ամոնիակ) | E° (V, ջուր) | |
|---|---|---|
| Li+ + e− ⇌ Li | −2.24 | −3.04 |
| K+ + e− ⇌ K | −1.98 | −2.93 |
| Na+ + e− ⇌ Na | −1.85 | −2.71 |
| Zn2+ + 2e− ⇌ Zn | −0.53 | −0.76 |
| NH4+ + e− ⇌ ½ H2 + NH3 | 0.00 | — |
| Cu2+ + 2e− ⇌ Cu | +0.43 | +0.34 |
| Ag+ + e− ⇌ Ag | +0.83 | +0.80 |

Ամոնիակի արտադրությունը
[խմբագրել | խմբագրել կոդը]Արդյունաբերությունում ամոնիակը ստանում են ազոտի և ջրածնի միացման, այսպես կոչված, սինթեզի եղանակով։ Այն դժվար իրագործելի քիմիական ռեակցիայի ամենաբարենպաստ պայմանները մշակել է գերմանացի քիմիկոս Ֆրիդրիխ Հաբերը։
- N2 + 3H2 → 2NH3 + Q
Ամոնիակի մեկ տոննա արտադրությունը Ռուսաստանում շրջակա միջավայր է արտանետվում 1200 նմ3, իսկ Եվրոպայում՝ 900 նմ3[8]։ [9][10][11][12]
Դարձելի ռեակցիաներ
[խմբագրել | խմբագրել կոդը]
Դուք նկատել եք, որ որոշ ռեակցիաների հավասարումներում հավասարման նշանի փոխարեն երբեմն դնում են հակադիր սլաքներ։ Սա նշանակում է, որ ռեակցիան դարձելի է, այսինքն՝ ընթանում է միաժամանակ երկու ուղղությամբ։ Դրա արդյունքը լինում է այն, որ ելանյութերը լրիվ չեն վերածվում վերջանյութերի։ Այն ռեակցիաները, որոնք ընթանում են հակադիր ուղղություններով, և ելանյութերն ամբողջությամբ չեն վերածվում վերջանյութերի, կոչվում են դարձելի ռեակցիաներ։
Դարձելի ռեակցիաների հավասարակշռությունը
[խմբագրել | խմբագրել կոդը]Դժվար չէ հասկանալ, որ այդպիսի ռեակցիաներում վաղ թե ուշ հաստատվում է հավասարակշռություն։ Այդ պահից սկսած՝ ինչ արագությամբ ելանյութերը փոխարկվում են վերջանյութերի (V1), նույն արագությամբ է վերջիններս վերածվում են ելանյութերի (V2)։ Ստեղծվում է շարժուն հավասարակշռություն, ուղիղ և հակադարձ ռեակցիաներն ընթանում են նույն արագությամբ՝ V1=V2։ Ամոնիակի ստացման նշված ռեակցիայում հավասարակշռություն է ստանում այն ժամանակ, երբ ազոտի ու ջրածնի ընդամենը 20-30 %-ն է վերածվում ամոնիակի։ Ռեակցիան իրականացնում են 400 °C ջերմաստիճանում՝ բարձր ճնշման տակ, կատալիզատորի առկայությամբ։ Որպես կատալիզատոր ծառայում է սպունգանման մետաղական երկաթը։ Սինթեզի աշտարակից դուրս է գալիս գազային խառնուրդ, որը բաղկացած է ամոնիակից և չփոխազդած ազոտից և ջրածնից։ Այդ խառնուրդից ամոնիակն անջատում են սառցենման ճանապարհով (ամոնիակը վերածվում է հեղուկի), իսկ ազոտն ու ջրածինը կրկին մղում են սինթեզի աշտարակ՝ ավելացնելով ելանյութերի նոր բաժիններ։ Այդպիսի տեխնոլոգիական գործընթացը, որի ժամանակ չփոխազդած ելանյութերն անջատում են վերջանյութերի խառնուրդից և նորից վերադարձնում փոխազդման ապարատ, կոչվում է շրջապտուտային գործընթաց։ Այդ ձևով հաջողվում է ազոտի և ջրածնի 95%-ը, ի վերջո, փոխարկել ամոնիակի։ Ամոնիակն աշխարհում ամենից շատ արտադրվող նյութերից մեկն է։
Գրականություն
[խմբագրել | խմբագրել կոդը]- 9-10-րդ դասարանների քիմիայի դասագրքեր
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.
- Ельницкий А. П., Василевская Е. И., Шарапа Е. И., Шиманович И. Е. Химия. — Мн.: Народная асвета, 2007.
Ծանոթագրություններ
[խմբագրել | խմբագրել կոդը]- ↑ 1,0 1,1 1,2 1,3 1,4 http://www.cdc.gov/niosh/npg/npgd0028.html
- ↑ 2,0 2,1 2,2 2,3 2,4 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 3,0 3,1 3,2 3,3 http://gestis.itrust.de/nxt/gateway.dll/gestis_de/001100.xml?f=templates$fn=default.htm$3.0
- ↑ http://www.cdc.gov/niosh/ipcsneng/neng0414.html
- ↑ Hall H. K. Correlation of the Base Strengths of Amines 1 // J. Am. Chem. Soc. / P. J. Stang — ACS, 1957. — Vol. 79, Iss. 20. — P. 5441—5444. — ISSN 0002-7863; 1520-5126; 1943-2984 — doi:10.1021/JA01577A030
- ↑ ГОСТ 6221-90. Аммиак жидкий технический. Технические условия
- ↑ http://www.rhbz.info/rhbz3.1.5.4.html Արխիվացված 2011-12-30 Wayback Machine Учебное пособие по РХБЗ. Характеристика аварийно химически опасных веществ
- ↑ ФАКТОРЫ КОНКУРЕНТНОСТИ НА РЫНКЕ АММИАЧНО-НИТРАТНЫХ УДОБРЕНИЙ
- ↑ АММИАЧНЫЕ УСТАНОВКИ НА РОССИЙСКИХ ПРЕДПРИЯТИЯХ
- ↑ ПРОИЗВОДИТЕЛИ АММИАКА И КАРБАМИДА В РОССИИ (Часть I)
- ↑ ПРОИЗВОДИТЕЛИ АММИАКА И КАРБАМИДА В РОССИИ (Часть II)
- ↑ ПРОИЗВОДИТЕЛИ АММИАКА И КАРБАМИДА В РОССИИ (Часть III)
Արտաքին հղումներ
[խմբագրել | խմբագրել կոդը]| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Ամոնիակ» հոդվածին։ |
| ||||||||||||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 1, էջ 325)։ |
