Ատոմ
 | |
| Ենթադաս | chemical entity?[1] և բաղադրյալ մասնիկ |
|---|---|
| Դյուի տասնորդական դասակարգում | 539.7 |
Ատոմ, քիմիական տարրի հատկություններ ունեցող փոքրագույն մասնիկ։ Ցանկացած պինդ մարմին, հեղուկ, գազ կամ պլազմա կազմված է չեզոք կամ իոնացված ատոմներից։ Ատոմները շատ փոքր են. սովորաբար մոտ 100 պիկոմետր (մեկ մետրի տասը միլիարդերորդը)։
Փոքր չափերի պատճառով ատոմների վարքագծի վերաբերյալ դասական ֆիզիկայի կանխատեսումները նկատելիորեն սխալ են, ինչը պայմանավորված է քվանտային էֆեկտներով։ Ֆիզիկայի զարգմացման ընթացքում ատոմային մոդելները հիմնվել են քվանտային սկզբունքների վրա՝ ատոմի վարքագիծն ավելի լավ կանխատեսելու և բացատրելու համար։
Ցանկացած ատոմ կազմված է մեկ միջուկից և մեկ կամ ավելի էլեկտրոններից։ Միջուկը կառուցված է մեկ կամ ավել պրոտոններից և սովորաբար գրեթե նույն քանակությամբ նեյտրոններից։ Պրոտոններն ու նեյտրոնները կոչվում են նուկլոնները։ Ատոմի զանգվածի ավելի քան 99.94%-ը միջուկն է։ Պրոտոններն ունեն դրական, էլեկտրոնները՝ բացասական, իսկ նեյտրոնները՝ չեզոք էլեկտրական լիցք։ Եթե ատոմում էլեկտրոնների և պրոտոնների թիվը հավասար է, ուրեմն այն էլեկտրականապես չեզոք է։ Եթե ատոմում պրոտոնների համեմատ կան ավել կամ պակաս էլեկտրոններ, ուրեմն այն համապատասխանաբար բացասական կամ դրական լիցք ունի և կոչվում է իոն։
Ատոմում էլեկտրոնները միջուկի հետ կապված են էլեկտրամագնիսական ուժի միջոցով։ Պրոտոնները և նեյտրոնները միջուկում կապված են միջուկային ուժերով, որոնք սովորաբար ավելի ուժեղ են էլեկտրամագնիսական ուժերից և չեզոքացնում են դրական լիցք ունեցող պրոտոնների միջև եղած վանող ուժերին։ Որոշակի պայմաններում վանող էլեկտրամագնիսական ուժը կարող է միջուկային ուժերից ուժեղ դառնալ, ինչի հետևանքով միջուկից կարող են նուկլոններ հեռանալ (այս միջուկային տրոհման արդյունքում առաջանում է այլ քիմիական տարր)։
Ատոմում պրոտոնների քանակով է պայմանավորված թե ինչ քիմիական տարրի ատոմ է այն. օրինակ՝ պղնձի բոլոր ատոմները ունեն 29 պրոտոն, իսկ նեյտրոնների թվով պայմանավորված է թե քիմիական տարիի որ իզոտոպից է ատոմը։ Էլեկտրոնների քանակը ազդեցություն ունի ատոմի էլեկտրամագնիսական հատկությունների վրա։ Քիմիական կապերի միջոցով ատոմները կարող են քիմիական միացություններ կազմել, ինչպես օրինակ մոլեկուլները։
Ատոմային տեսության պատմություն
[խմբագրել | խմբագրել կոդը]Ատոմները փիլիսոփայությունում
[խմբագրել | խմբագրել կոդը]Այն միտքը, որ նյութը կազմած է դիսկրետ միավորներից հանդիպում է բազմաթիվ անտիկ մշակույթներում, ինչպես օրինակ՝ Հնդկաստանում և Հունաստանում։ «Ատոմ» անվանումը տրվել է հին հույն փիլիսոփաների կողմից։ Սակայն, այս գաղափաները հիմնված էին փիլիսոփայական և աստվածաբանական հիմնավորումների վրա, ոչ թե ապացույցների և փորձերի։ Այդ պատճառով ատոմի կառուցվածքի և վարքագծի մասին նրանց պատկերացումները սխալ էին։ Նրանք նաև չէին կարող ապացուցել իրենց վարկածը, այսպիսով ատոմիզմը նյութի բնույթի վերաբերյալ բազմաթիվ տեսություններից մեկն էր։ Միայն 19-րդ դարում ատոմի գաղափարը ընդունվեց գիտնականների կողմից, երբ քիմիայում արվեցին այնպիսի հայտնագորցություններ, որոնք միայն կարող էին բացատրվել ատոմի գոյությամբ։
Ապացույցի վրա հիմնված առաջին տեսություն
[խմբագրել | խմբագրել կոդը]
1800-ական թվականների սկզբին Ջոն Դալթոնը ատոմի գաղափարի միջոցով է բացատրել այն, որ տարրերը միշտ փոխազդում են փոքր ամբողջ թվերի հարաբերությամբ։՚ Օրինակ՝ գոյություն ունի երկու անագի օքսիդ. մեկը՝ 88.1% անագ, 11.9% թթվածին, երկրորդը՝ 78.7% անագ, 21.3% թթվածին (համապատասխանաբար անագի օքսիդ(II) և անագի օքսիդ(IV))։ Սա նշանակում է, որ 100 գրամ անագը միայն կարող է միանալ 13.5 կամ 27 գրամ թթվածնի հետ։ 13.5-ը և 27-ը կազմում եմ 1:2 հարաբերություն։ Այս փաստից ելնելով Դալթոնը եզրակացրեց, որ տարրերը փոխազդում են դիսկրետ միավորների (այլ կերպ ասած՝ ատոմների) ամբողջ թվի բազմապատիկներով։ Անագի օքսիդի պարագայում մեկ անագի ատոմը կարող է միանալ կամ մեկ, կամ երկու թթվածնի ատոմի հետ[2]։
Դալթոնը նաև հավատում էր, որ ատոմի տեսությունը կարող է բացատրել, թե ինչու է ջուրը տարբեր գազեր տարբեր հարաբերությամբ կլանում։ Օրինակ՝ նա գտավ, որ ջուրը ածխաթթու գազ շատ ավելի լավ է կլանում, քան ազոտ[3]։ Դալթոնը կարծում էր, որ սա կապված է գազերի համապատասխան մասնիկների զանգվածների և դասավորության տարբերությունների հետ (ածխաթթու գազի մոլեկուլը (CO2) շատ ավելի մեծ և ծանր է ազոտի մոլեկուլից (N2))։
Բրոունյան շարժում
[խմբագրել | խմբագրել կոդը]1827 թվականին բուսաբան Ռոբերտ Բրոունը ջրի մեջ ծաղկափոշու շարժը մանրադիտակով ուսումնասիրելիս հայտնաբերեց, որ նրանք շարժվում են անկոնոն և անդադար, այս երևույթը այժմ կոչվում է «Բրոունյան շարժում»։ Ենթադրվում էր, որ սրա պատճառը ջրի մոլեկուլների շարժն է։ 1905 թվականին Ալբերտ Այնշտայնը ապացուցեց այս մոլեկուլների և նրանց շարժման գոյությունը՝ բրոունյան շարժման առաջին վիճակագրական վերլուծությամբ[4][5][6]։ Ֆրանսիացի ֆիզիկոս Ժան Բատիստ Պերրենը օգտագործել է Այնշտայնի աշխատանքները՝ ատոմների զանգվածն ու չափերը փորձնականորեն որոշելու համար[7]։
Էլեկտրոնի հայտնաբերում
[խմբագրել | խմբագրել կոդը]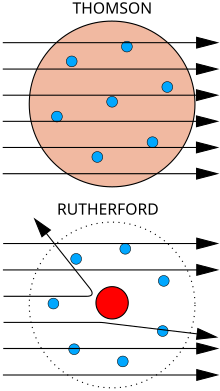
Վերևում։ Ակնկալվող արդյունք: Ալֆա մասնիկները անցնում են ատոմի պուդինգային մոդելի միջով աննշան շեղմամբ։
Ներքևում: Դիտարկված արդյունք: Մասնիկների փոքր մասը շեղվել է դրական լիցքավորված միջուկի պատճառով։
Ֆիզիկոս Ջոզեֆ Ջոն Թոմսոնը հաշվել է կաթոդային ճառագայթների զանգվածը՝ ցույց տալով, որ դրանք կազմված են մասնիկներից, բայց որոնք մոտ 1800 անգամ ավելի թեթև են, քան ամենաթեթև ատոմը՝ ջրածինը։ Հետևաբար՝, դրանք ատոմները չեն, բայց մասնիկ են։ Սա առաջին հայտնաբերված ներատոմային մասնիկն էր, որը սկզբում Թոմսոնը անվանեց «կորպուսկուլ», սակայն հետագայում անվանվել է «էլեկտրոն»։ Ջորջ Սթոնին ցույց է տվել, որ սրանք նույն այն մասնիկներն են, որոնք անջատվում են ֆոտոէլեկտրական և ռադիոակտիվ նյութերից[8]։ Արագորեն հայտնաբերվեց, որ դրանք մետաղական լարերում էլեկտրական հոսանք կրող մասնիկներն են, որոնք նաև կրում են ատոմում բացասական էլեկտրական լիցքը։ Այս աշխատանքի համար 1906 թվականին Թոմսոնը ստացավ Ֆիզիկայի Նոբելյան մրցանակ։ Այսպիսով, նա վերացրեց այն տեսակետը թե ատոմները նույթի անբաժանելի, վերջնական մասնիկներն են[9]։ Թոմսոնը սխալմամբ կարծում էր, որ տարրերի ատոմները կազմված են մի քանի բացասականապես լիցքավորված էլեկտրոններից, որոնք մտնում են համասեռ բաշխված դրական էլեկտրական լիցք ունեցող ոլորտի մեջ (սա հայտնի է Թոմսոնի ատոմի մոդել անվամբ)։
Միջուկի հայտնաբերում
[խմբագրել | խմբագրել կոդը]Պարզվեց, որ ատոմի թոմսոնյան մոդելը անբավարար է բազմաթիվ երևույթներ բացատրելու համար։ Դրանով չհաջողվեց բացատրել ատոմների կողմից ալֆա–մասնիկների ցրման երևույթը հաստատող անգլիացի ֆիզիկոս Էռնեստ Ռեզերֆորդի և նրա աշխատակիցների՝ Հանս Գեյգերի և Էրնեստ Մարսդեի, 1911 թվականին կատարած փորձերի արդյունքները։ Անցնելով նյութի միջով, ալֆա–մասնիկներն ընդհարվում են ատոմների հետ։ Յուրաքանչյուր ընդհարման ժամանակ ալֆա–մասնիկը, անցնելով ատոմի էլեկտրական դաշտով, փոխում է շարժման ուղղությունը՝ ցրվում է։ Այդ շեղումները հիմնականում շատ փոքր են։ Ուստի և նյութի բարակ շերտով ալֆա–մասնիկների փունջը անցնելիս տեղի էր ունենում փնջի շատ փոքր ցրում։ Սակայն մասնիկներից մի քանիսը շեղվում էին 90°–ից ավելի անկյունով։ Այս երևույթը չէր բացատրվում Թոմսոնի մոդելով, որովհետև «հոծ» ատոմի էլեկտրական դաշտը չէր կարող մեծ անկյունով շեղել զանգվածեղ և արագաշարժ ալֆա–մասնիկը։ Ռեզերֆորդը առաջարկեց ատոմի սկզբունքորեն նոր մոդել, որն իր կառուցվածքով հիշեցնում է Արեգակնային համակարգը և ստացավ մոլորակային մոդել անունը։ Ըստ այդ մոդելի՝ ատոմի կենտրոնում գտնվում է դրական լիցք ունեցող միջուկը, որի չափերը (~10−14 մ) շատ փոքր են ատոմի չափերից (~10−10 մ), իսկ զանգվածը գրեթե հավասար է ատոմի զանգվածին։ Միջուկի շուրջը պտտվում են էլեկտրոնները (ինչպես մոլորակները Արեգակի շուրջը)։ Չլիցքավորված (չեզոք) ատոմում էլեկտրոնների թիվը այնպիսին է, որ նրանց գումարային բացասական լիցքը չեզոքացնում է միջուկի դրական լիցքը։ Ի տարբերություն մոլորակային համակարգում գործող ձգողականության ուժի, ատոմում գործում են էլեկտրական (կուլոնյան) ուժեր[10][11][12]։
Իզոտոպների հայտնաբերում
[խմբագրել | խմբագրել կոդը]1913 թվականին ռադիոակտիվ նյութերի հետ փորձարկումներ անելիս ռադիոքիմիկոս Ֆրեդերիկ Սոդդիը հայտնաբերեց, որ պարբերական համակարգի յուրաքանչյուր դիրքի համար կան ավելի քան մեկ տեսակի ատոմներ[13]։ Իզոտոպ անվանումը տվել է Մարգարետ Թոդ։ Ջ. Ջ. Թոմսոնը իոնացված գազերի վերաբերյալ իր աշխատանքի ընթացքում ատոմների տեսակները առանձնացնելու եղանակ է ստեղծել, ինչը հետագայում հանգեցրեց կայուն իզոտոպների հայտնաբերմանը[14]։
Բորի մոդել
[խմբագրել | խմբագրել կոդը]
1913 թվականին ֆիզիկոս Նիլս Բորը առաջ քաշեց մոդել, ըստ որի՝ էլեկտրոնները ատոմում կարող են շարժվել միայն որոշակի ուղեծրերով և չճկառագայթել, սակայն մի ուղեծրից մյուսին անցնել կարող են միայն դիսկրետ քանակությամբ էներգիա կլանելով կամ ճառագայթելով[15]։ Այս մոդելը բացատրեց էլեկտրոնների ուղեծրերի կայությունը (դասական էլեկտրադինամիկայի տեսանկյունից Ռեզերֆորդի մոդելում էլեկտրոնը, որը պտտվում էր միջուկի շուրջը պետք է անընդհատ ճառագայթեր և շատ արագ կորցնելով էներգիան՝ ընկներ միջուկի վրա) և այն, որ էլեկտրոնները էլեկտրամագնիսական ճառագայթումը կլանում կամ արձագում են դիսկրետ սպեկտրային չափով[16]։
Նույն թվականին արված Հենրի Մոսելեիի փորձերով նույնպես ապացուցվում էր Նիլս Բորի տեսությունը։ Այս արդյունքները կատարելագործեցին Էռնեստ Ռեզերֆորդի և Անտոնիո Վան դե Դոր Բրոքի մոդելը, ըստ որի՝ ատոմի միջուկի լիցքը հավասար է պարբերական համակարգում իր համարին։ Մինչև այս փորձերը ատոմական համարը ֆիզիկական կամ փորձարարական մեծություն չէր։ Այն, որ ատոմային համարը համապատասխանում է ատոմի միջուկի լիցքին, ընդունվում է նաև ատոմի ժամանակակից մոդելի կողմից[17]։
Քիմիական կապերի բացատրություն
[խմբագրել | խմբագրել կոդը]1916 թվականին Գիլբերտ Նյուտոն Լյուիսը բացատրել է ատոմների միջև քիմիական կապերը որպես իրենց բաղադրիչ էլեկտրոնների փոխազդեցություն[18]։ Քանի որ տարրերի քիմիական հատկությունները պարբերական օրենքի համաձայն կրկնվում են[19], 1919 թվականին ամերիկացի քիմիկոս Իրվինգ Լենգմյուրը ենթադրեց, որ սա կարող է բացատրվել, եթե ատոմում էլեկտրոնները կապված կամ խմբավորված են ինչ-որ ձևով։ Նա կարծում էր, որ միջուկի շուրջը էլեկտրոնների խմբերը զբաղեցնում են էլեկտրոնային շերտեր[20]։
Քվանտային ֆիզիկայի հետագա զարգացումներ
[խմբագրել | խմբագրել կոդը]1922 թվականի Շտեռն-Գեռլախի փորձը լրացուցիչ ապացույցներ տրամադրեց ատոմի քվանտային բնույթի համար։ Արծաթի ատոմների փունջը, անցնելով խիստ անհամասեռ մագնիսական դաշտով, ճեղքվում էր և էկրանի վրա առաջացնում շերտեր, որոնք վկայում էին մագնիսական մոմենտի պրոյեկցիայի քվանտացումը։ Դասական տեսության համաձայն, էկրանի վրա պետք է առաջանար մեկ հաստ շերտ, սակայն իրականում առաջանում էին սիմետրիկ դասավորված 2 նեղ շերտեր[21]։
1924 թվականին Լուի դը Բրոյլը առաջարկեց, որ բոլոր մասնիկները որոշ չափով վարվում են ալիքների նման։ 1926 թվականին Էրվին Շրյոդինգեր օգտագործեց այս միտքը՝ ատոմի մաթեմատիկական մոդել ստեղծելու համար, որը էլեկտրոններին նկարագում էր որպես եռաչափ ալիքի ձևերի, ոչ թե կետային մասնիկի տեսքով։ Այս մոդելի հետևանքն այն էր, որ տրված պահին մասնիկի դիրքի և իմպուլսի համար մաթեմատիկորեն անհնար է ստանալ ճշգրիտ արժեքներ։ Այլ կերպ ասած, որքան ավելի մեծ ճշգրտությամբ հնարավոր է իմանալ հատկություններից որևէ մեկը, այնքան սակավ ճշգրտությամբ է հնարավոր չափել, վերահսկել կամ իմանալ մյուս հատկությունը[22]։ Սա հայտնի է անորոշությունների սկզբունք անվամբ, որը ձևակերպել է Վերներ Հայզենբերգը 1926 թվականին։ Այս մոդելի օգնությամբ բացատրվեցին դիտումների ընթացքում նկատրված ատոմի վարքագծեր, որոնք նախկին մոդելը չէր կարող բացատրել, ինչպես օրինակ՝ ջրածնից մեծ ատոմներում որոշակի կառուցվածքային և սպեկտրյալ նմանությունները[23][24]։
Նեյտրոնի հայտնաբերում
[խմբագրել | խմբագրել կոդը]Մասս-սպեկտրաչափության զարգացումը հնարավորություն տվեց մեծ ճշտությամբ չափել ատոմի զանգվածը։ Քիմիկոս Ֆրենսիս Ուիլյամ Աստոնը այս սարքի օգնությամբ ցույց է տվել, որ իզոտոպները տարբեր զանգված ունեն։ Իզոտոմների ատոմային զանգվածը տարբերվում է ջրածնի ատոմի ծանգվածի ամբողջ բազմապատիկների քանակով[25]։ 1932 թվականին ֆիզիկոս Ջեյմս Չադվիկը նեյտրոնի հայտնաբերմաբ բացատրեց այս երևույթը։ Նեյտրոնը չեզոք լիցք ունեցող մասնիկ է, որի զանգվածը գրեթե հավասար է պրոտոնի զանգվածին։ Իզոտոպները նույն նույն քանակությամբ պրոտոն, բայց տարբեր քանակությամբ նեյտրոն ունեցող տարրեր են[26]։
Տրոհում, բարձր էներգիայի ֆիզիկա և կոնդենսացված նյութ
[խմբագրել | խմբագրել կոդը]1938 թվականին գերմանացի քիմիկոս Օտտո Հահնը՝ Ռեզերֆորդի ուսանողներից մեկը, տրանսուրան տարր ստանալու նպատակով ուրանի ատոմները ռմբակոծեց նեյտրոններով։ Սակայն նա դրա փոխարեն ստացավ բարիում[27][28]։ Մեկ տարի անց Լիզա Մեյտները և իր ազգական Օտտո Ֆրիշը հաստատեցին, որ Հահնի արդյունքները առաջին փորձարարական միջուկային տրոհումն էր[29][30]։ 1944 թվականին Հահն ստացավ Քիմիայի Նոբելյան մրցանակ։ Չնայած Հահնի ջանքերին, Մեյտների և Ֆրիշի ներդրումները չեն ճանաչվել[31]։
1950-ական թվականներին արագացուցիչների և մասնիկների դետեկտորների կատարելագործումը գիտնականներին թույլ տվեց ուսումնասիրել բարձր էներգիաներում ատոմների շարժի հետևանքները[32]։ Պարզվեց, որ նեյտրոններն ու պրոտոնները հադրոններ են, և կազմված են ավելի փոքր մասնիկներից, որոնք կոչվում են քվարկներ։ Ձևավորվել է ստանդարտ մոդելը, որը մինչև այժմ բարեհաջող բացատրել է միջուկի հատկությունները[33]։
Կառուցվածք
[խմբագրել | խմբագրել կոդը]Ներատոմային մասնիկներ
[խմբագրել | խմբագրել կոդը]Չնայած «ատոմ» բառը սկզբնապես տրվել է անբաժանելի մասնիկի, ժամանակակից գիտությանը հայտնի է, որ ատոմը բաղկացած է բազմաթիվ ներատոմային մասնիկներից։ Ատոմը կազմված է էլեկտրոնից, պրոտոնից և նեյտրոնից (երեքն էլ ֆերմիոն են)։ Սակայն, ջրածին-1-ի ատոմը նեյտրոն չունի, իսկ հիդրոնը՝ էլեկտրոն չունի։
Էլեկտրոնը ունի բացարձակ արժեքով պրոտոնի լիցքին հավասար բացասական էլեկտրական լիցք, զանգվածը՝ 9.11×10−31 կգ, որը մոտավորապես հավասար է պրոտոնի զանգվածի 1/1836-ին[34][35][36] Էլեկտրոնները պատկանում են լեպտոնների ընտանիքի առաջին սերնդին[37], և համարվում են տարրական մասնիկներ, քանի որ ներքին կառուցվածք չունեն[38]։ Իմպուլսի մոմենտը (սպին) Պլանկի հաստատունի միավորով՝ ħ-ով, արտահայտած՝ 12։ Պաուլիի սկզբունքի համաձայն ոչ մի երկու էլեկտրոն չեն կարող նույն քվանտային վիճակում գտնվել, քանի որ այն ֆերմիոն է[37]։ Մնացած տարրական մասնիկների նման էլեկտրոնները նույնպես ցուցաբերում են և՛ մասնիկի, և՛ ալիքի հատկություններ. նրանք կարող են բախվել այլ մասնիկների հետ և կարող են լույսի նման դիֆրակցիայի են ենթակվում։ Էլեկտրոնների ալիքային հատկությունները ավելի հեշտ է դիտել, քան այլ մասնիկներինը, ինչպես օրինակ՝ նեյտրոններինը և պրոտոններինը, քանի որ էլեկտրոնները ունեն ավելի փոքր զանգված, հետևաբար՝ ավելի երկար Դը Բրոյլի ալիք։
Պրոտոնները ունեն դրական էլեկտրական լիցք և 1.6726×10−27 կգ զանգված։ Ատոմում պրոտոնների քանակը կոչվում է ատոմական համար։ Էռնեստ Ռեզերֆորդը (1919) նկատել է, որ ազտորը ալֆա-մասնիկներով ռմբակոծելիս ջրածնի միջուկ է անջատվում։ 1920 թվականին նա ընդունեց, որ ջրածնի միջուկը ատոմում առանձին մասնիկ է և այն կոչեց պրոտոն։
Նեյտրոնները էլեկտրական լիցք չունեն, հանգստի զանգվածը էլեկտրոնի զանգվածից 1,839 անգամ մեծ է[39] կամ հավասար է 1.6929×10−27 կգ-ի։ Այն ատոմի մաս կազմող մասնիկներից ամենածանրն է։ Նեյտրոնները և պրոտոնները (միասին կոչվում են նուկլոններ) համեմատելի չափեր ունեն, չնայած այս մասնիկների «մակերևույթը» հստակ սահմանված չէ[40]։ Նեյտրոնը 1932 թվականին հայտնաբերել է անգլիացի ֆիզիկոս Ջեյմս Չադվիկը։
Ֆիզիկայի ստանդարտ մոդելում էլեկտրոնները տարրական մասնիկներ են առանց ներքին կառուցվածքի։ Սակայն, պրոտոնը և նեյտրոնը կազմված են այլ տարրական մասնիկներից՝ քվարկներից։ Ատոմներում կան երկու տեսակի քվարկներ՝ երկուսն էլ կոտորակային էլեկտրական լիցքով։ Պրոտոնը կազմված է երկու u-քվարկից (յուրաքանչյուրը +23 լիցքով) և մեկ d-քվարկից (−13 լիցքով)։ Նեյտրոնը կազմված է երկու d-քվարկից և մեկ u-քվարկից։ Այս տարբերությամբ է պայմանավորված պրոտոնի և նեյտրոնի ծանգվածի և լիցքի տարբերությունը[41][42]։
Քվարկներին միջև գործում է ուժեղ փոխազդեցություն, որի համար որպես փոխանակային մասնիկ (կամ տրամաչափային բոզոն) հանդես է գալիս գլյուոնը։ Իսկ պրոտոնները և նեյտրոնները միասին պահվում են միջուկային ուժերի միջոցով, որոնք իրականում ուժեղ փոխազդեցութունների արդյունք են[41][42]։
Միջուկ
[խմբագրել | խմբագրել կոդը]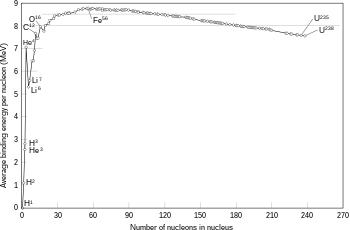
Պրոտոնները և նեյտրոնները միասին կազում են ատոմի միջուկը։ Միջուկի շառավիղը մոտավորապես հավասար է 1.07 3√A fm-ի, որտեղ A-ն միջուկում նուկլոնների ընդհանուր քանակն է[43]։ Սա ատոմի շառավղից շատ փոքր է, որը 105 fm-ի կարգի թիվ է։ Նուկլոնները միասին կապվում են կարճ տարածությունների վրա ազդեղ միջուկային ուժերով։ 2.5 fm-ի ավելի մոտ տարածություններում այս ուժերը գերազանցում են դրական լիցք ունեցող պրոտոնների վանողական ուժին (Կուլոնի օրենք)[44]։
Նույն քիմիական տարրի ատոմները ունեն նույն թվով պրոտոնները, այս թիվը հայտնի է ատոմական համար անվամբ։ Նույն տարի ատոմում նեյտրոնների քանակը կարող է տարբերվել՝ կախված տարրի իզոտոպից։ Պրոտոնների համեմատ նեյտրոնների թվով է պայմանավորված միջուկի կայությունը[45]։
Պրոտոնը, էլեկտրոնը և նեյտրոնը համարվում են ֆերմիոն։ Ֆերմիոնները ենթարկվում են Պաուլիի սկզբունքին, որն արգելում է նույնական ֆերմիոնների, օրինակ՝ պրոտոնների, նույն պահին նույն քվանատային վիճակում գտնվելը։ Այսպիսով, միջուկում յուրաքանչյուր պրոտոն պետք է մնացած պրոտոններից տարբեր քվանտային վիճակում գտնվի, նույնը վերաբերում է նաև բոլոր նեյտրոններին և էլեկտրոնային ամպի էլեկտրոններին։ Սակայն, պչոտոնը և նեյտրոնը կարող են նույն քվանտային վիճակում գտնվել[46]։
Ցածր ատոմային համար ունեցող ատոմների դեպքում՝ պրոտոններից ավելի շատ նեյտրոն ունեցող միջուկները ձգտում են զբաղեցնել ավելի ցածր էներգետիկ մակարդակ՝ ենթարկվելով ռադիոակտիվ տրոհման՝ մինչև նեյտրոն-պրոտոն հարաբերությունը մոտենա մեկի։ Սակայն, բարձ ատոմային համար ունեցող ատոմների դեպքում նեյտրոնների ավելի մեծ համամասնություն է հարկավոր պրոտոնների վաղությանը հակազդելու համար։ Այսպիսով՝ Z = 20 (կալցիում) ատոմային համարից բարձր կայուն ատոմների դեպքում պրոտոնների և նեյտրոնների քանակաը հավասար չէ, և Z-ի աճին զուգահեռ մեծանում է նաև նեյտրոն-պրոտոն հարաբերությունը[46]։ Ամենաբարձր պրոտոն-նեյտրոն հարաբերությամբ իզոտոպը կապար-208-ն է (մոտ 1.5)։
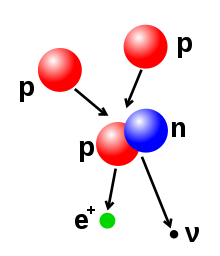
Ատոմի միջուկում պրոտոնների և նեյտրոնների քանակը հնարավոր է փոխել, սակայն ուժեղ փոխազդեցության պատճառով այս գործընթացը պահանջում է մեծ էներգիա։ Ջերմամիջուկային ռեակցիա տեղի է ունենում, երբ մի քանի ատոմային մասնիկներ միանում են՝ կազմելով ավելի ծանր միջուկ։ Օրինակ՝ արևի միջուկում կուլոնային արգելքը՝ փոխադարձ վանողության ուժը, հաղթահարելու և մեկ միջուկ կազմելու համար պրոտոններին անհրաժեշտ է 3-10 կէՎ էներգիա[47]։ Միջուկի ճեղքումը սրա հակառակ գործընթացն է. սովորաբար ռադիոակտիվ տրոհման միջոցով միջուկը բաժանվում է՝ կազմելով ավելի փոքր միջուկներ։ Միջուկը նաև կարող է ձևափոխվել մեծ էներգիա ունեցող մասնիկներով կամ պրոտոններով եմբակոծելու միջոցով։ Եթե այս փոփոխության ընթացքում փոխվում է միջուկում պրոտոնների քանակը, առաջանում է այլ քիմիական տարրի ատոմ[48][49]։
Եթե միաձուլման ռեակցիայից հետո առաջացած միջուկի զանգվածը ավել փոքր է, քան նախնական մասնիկների զանգվածների գումարը, ուրեմն այդ արժեքների տարբերությունը արտանետվում է այլ էներգիայի տեսքով (ինչպես օրինակ՝ գամմա ճառագայթները կամ բետա-մասնիկների կինետիկ էներգիան), համաձայն Ալբերտ Այնշտայնի զանգվածի և էներգիայի համարժեքության բանաձևի՝ E = mc2, որտեղ m-ը զանգվածների տարբերությունն է, c-ն՝ լույսի արագությունը, իսկ E-ն՝ առաջացած էներգիան։ Այս տարբերությունները կապի էներգիայի մաս է կազմում, և չվերականգնվող էներգիա է, ինչը ստիպում է ձուլվող մասնիկներին միասին մնալ[50]։
Եթե ռեակցիայի ընթացքում ստեղծվող միջուկը ունի երկաթից և նիկելից (ընդհանուր առմամբ 60 նուկլոբ) փոքր ատոմային համար, ուրեմն սա սովորաբար էքսոթերմիկ գործընթաց է, որը արտադրում է ավելի շատ էներգիա, քան անհրաժեշտ է միջուկի միացման համար[51]։ Այսպիսի գործընթացներն են աստղերի ինքնաբավ ռեակցիաների աղբյուր հանդիսանում։ Ավելի ծանր միջուկի դեպքում` 26-ից բարձր ատոմային համար և 60 բարձր ատոմային զանգված, սա էնդոթերմիկ գործընթաց է։ Այս զանգվածեղ միջուկները չեն կարող ենթարկվել այնպիսի էներգիա արտադրող ռեակցիաների, որոնք ունակ են պահպանել աստղի հիդրոստատիկ հավասարակշռություն[46]։
Ծանոթագրություններ
[խմբագրել | խմբագրել կոդը]- ↑ ChEBI — EBI.
- ↑ Andrew G. van Melsen (1952). From Atomos to Atom. Mineola, N.Y.: Dover Publications. ISBN 0-486-49584-1.
- ↑ Dalton, John. "On the Absorption of Gases by Water and Other Liquids", in Memoirs of the Literary and Philosophical Society of Manchester. 1803. Retrieved on August 29, 2007.
- ↑ Einstein, Albert (1905). «Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen» (PDF). Annalen der Physik (German). 322 (8): 549–560. Bibcode:1905AnP...322..549E. doi:10.1002/andp.19053220806. Արխիվացված է օրիգինալից (PDF) 2007 թ․ հուլիսի 18-ին. Վերցված է 2007 թ․ փետրվարի 4-ին.
{{cite journal}}: CS1 սպաս․ չճանաչված լեզու (link) - ↑ Mazo, Robert M. (2002). Brownian Motion: Fluctuations, Dynamics, and Applications. Oxford University Press. էջեր 1–7. ISBN 0-19-851567-7. OCLC 48753074.
- ↑ Lee, Y.K.; Hoon, K. (1995). «Brownian Motion». Imperial College. Արխիվացված է օրիգինալից 2007 թ․ դեկտեմբերի 18-ին. Վերցված է 2007 թ․ դեկտեմբերի 18-ին.
- ↑ Patterson, G. (2007). «Jean Perrin and the triumph of the atomic doctrine». Endeavour. 31 (2): 50–53. doi:10.1016/j.endeavour.2007.05.003. PMID 17602746.
- ↑ Thomson, J. J. (1901 թ․ օգոստոս). «On bodies smaller than atoms». The Popular Science Monthly. Bonnier Corp.: 323–335. Վերցված է 2009 թ․ հունիսի 21-ին.
- ↑ «J.J. Thomson». Nobel Foundation. 1906. Վերցված է 2007 թ․ դեկտեմբերի 20-ին.
- ↑ Խմբագրական կոլեգիա, Հայկական Սովետական Հանրագիտարան, հ. {{{1}}} (խմբ. Վիկտոր Համբարձումյան), Ե., «Հայկական ՍՍՀ Գիտությունների Ակադեմիա Հայկական Սովետական Հանրագիտարանի գլխավոր խմբագրություն», էջ {{{2}}}։
- ↑ Rutherford, E. (1911). «The Scattering of α and β Particles by Matter and the Structure of the Atom» (PDF). Philosophical Magazine. 21 (125): 669–88. doi:10.1080/14786440508637080.
- ↑ «The Gold Foil Experiment». myweb.usf.edu. Արխիվացված է օրիգինալից 2016 թ․ նոյեմբերի 19-ին. Վերցված է 2017 թ․ հուլիսի 24-ին.
- ↑ «Frederick Soddy, The Nobel Prize in Chemistry 1921». Nobel Foundation. Վերցված է 2008 թ․ հունվարի 18-ին.
- ↑ Thomson, Joseph John (1913). «Rays of positive electricity». Proceedings of the Royal Society. A. 89 (607): 1–20. Bibcode:1913RSPSA..89....1T. doi:10.1098/rspa.1913.0057.
- ↑ Stern, David P. (2005 թ․ մայիսի 16). «The Atomic Nucleus and Bohr's Early Model of the Atom». NASA/Goddard Space Flight Center. Արխիվացված է օրիգինալից 2007 թ․ օգոստոսի 20-ին. Վերցված է 2007 թ․ դեկտեմբերի 20-ին.
- ↑ Bohr, Niels (1922 թ․ դեկտեմբերի 11). «Niels Bohr, The Nobel Prize in Physics 1922, Nobel Lecture». Nobel Foundation. Վերցված է 2008 թ․ փետրվարի 16-ին.
- ↑ Pais, Abraham (1986). Inward Bound: Of Matter and Forces in the Physical World. New York: Oxford University Press. էջեր 228–230. ISBN 0-19-851971-0.
- ↑ Lewis, Gilbert N. (1916). «The Atom and the Molecule». Journal of the American Chemical Society. 38 (4): 762–786. doi:10.1021/ja02261a002.
- ↑ Scerri, Eric R. (2007). The periodic table: its story and its significance. Oxford University Press US. էջեր 205–226. ISBN 0-19-530573-6.
- ↑ Langmuir, Irving (1919). «The Arrangement of Electrons in Atoms and Molecules». Journal of the American Chemical Society. 41 (6): 868–934. doi:10.1021/ja02227a002.
- ↑ Scully, Marlan O.; Lamb, Willis E.; Barut, Asim (1987). «On the theory of the Stern-Gerlach apparatus». Foundations of Physics. 17 (6): 575–583. Bibcode:1987FoPh...17..575S. doi:10.1007/BF01882788.
- ↑ TED-Ed (2014 թ․ սեպտեմբերի 16). «What is the Heisenberg Uncertainty Principle? - Chad Orzel» – via YouTube.
- ↑ Brown, Kevin (2007). «The Hydrogen Atom». MathPages. Վերցված է 2007 թ․ դեկտեմբերի 21-ին.
- ↑ Harrison, David M. (2000). «The Development of Quantum Mechanics». University of Toronto. Արխիվացված է օրիգինալից 2007 թ․ դեկտեմբերի 25-ին. Վերցված է 2007 թ․ դեկտեմբերի 21-ին.
- ↑ Aston, Francis W. (1920). «The constitution of atmospheric neon». Philosophical Magazine. 39 (6): 449–55. doi:10.1080/14786440408636058.
- ↑ Chadwick, James (1935 թ․ դեկտեմբերի 12). «Nobel Lecture: The Neutron and Its Properties». Nobel Foundation. Վերցված է 2007 թ․ դեկտեմբերի 21-ին.
- ↑ Bowden, Mary Ellen (1997). «Otto Hahn, Lise Meitner, and Fritz Strassmann». Chemical achievers : the human face of the chemical sciences. Philadelphia, PA: Chemical Heritage Foundation. էջեր 76–80, 125. ISBN 9780941901123.
- ↑ «Otto Hahn, Lise Meitner, and Fritz Strassmann». Chemical Heritage Foundation. Վերցված է 2016 թ․ հոկտեմբերի 27-ին.
- ↑ Meitner, Lise; Frisch, Otto Robert (1939). «Disintegration of uranium by neutrons: a new type of nuclear reaction». Nature. 143 (3615): 239–240. Bibcode:1939Natur.143..239M. doi:10.1038/143239a0.
- ↑ Schroeder, M. «Lise Meitner – Zur 125. Wiederkehr Ihres Geburtstages» (German). Արխիվացված է օրիգինալից 2011 թ․ հուլիսի 19-ին. Վերցված է 2009 թ․ հունիսի 4-ին.
{{cite web}}: CS1 սպաս․ չճանաչված լեզու (link) - ↑ Crawford, E.; Sime, Ruth Lewin; Walker, Mark (1997). «A Nobel tale of postwar injustice». Physics Today. 50 (9): 26–32. Bibcode:1997PhT....50i..26C. doi:10.1063/1.881933.
- ↑ Kullander, Sven (2001 թ․ օգոստոսի 28). «Accelerators and Nobel Laureates». Nobel Foundation. Վերցված է 2008 թ․ հունվարի 31-ին.
- ↑ «The Nobel Prize in Physics 1990». Nobel Foundation. 1990 թ․ հոկտեմբերի 17. Վերցված է 2008 թ․ հունվարի 31-ին.
- ↑ «CODATA value: proton-electron mass ratio». 2006 CODATA recommended values. National Institute of Standards and Technology. Վերցված է 2009 թ․ հուլիսի 18-ին.
- ↑ «JERRY COFF». Վերցված է 2010 թ․ սեպտեմբերի 10-ին.
- ↑ Demtröder, Wolfgang (2002). Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics (1st ed.). Springer. էջեր 39–42. ISBN 3-540-20631-0. OCLC 181435713.
- ↑ 37,0 37,1 Curtis, L.J. (2003). Atomic Structure and Lifetimes: A Conceptual Approach. Cambridge University Press. էջ 74. ISBN 0-521-53635-9.
- ↑ Eichten, E.J.; Peskin, M.E.; Peskin, M. (1983). «New Tests for Quark and Lepton Substructure». Physical Review Letters. 50 (11): 811–814. Bibcode:1983PhRvL..50..811E. doi:10.1103/PhysRevLett.50.811.
- ↑ Woan, Graham (2000). The Cambridge Handbook of Physics. Cambridge University Press. էջ 8. ISBN 0-521-57507-9. OCLC 224032426.
- ↑ MacGregor, Malcolm H. (1992). The Enigmatic Electron. Oxford University Press. էջեր 33–37. ISBN 0-19-521833-7. OCLC 223372888.
- ↑ 41,0 41,1 Particle Data Group (2002). «The Particle Adventure». Lawrence Berkeley Laboratory. Արխիվացված օրիգինալից 4 January 2007-ին. Վերցված է 2007 թ․ հունվարի 3-ին.
- ↑ 42,0 42,1 Schombert, James (2006 թ․ ապրիլի 18). «Elementary Particles». University of Oregon. Արխիվացված է օրիգինալից 2011 թ․ օգոստոսի 30-ին. Վերցված է 2007 թ․ հունվարի 3-ին.
- ↑ Jevremovic, Tatjana (2005). Nuclear Principles in Engineering. Springer. էջ 63. ISBN 0-387-23284-2. OCLC 228384008.
- ↑ Pfeffer, Jeremy I.; Nir, Shlomo (2000). Modern Physics: An Introductory Text. Imperial College Press. էջեր 330–336. ISBN 1-86094-250-4. OCLC 45900880.
- ↑ Wenner, Jennifer M. (2007 թ․ հոկտեմբերի 10). «How Does Radioactive Decay Work?». Carleton College. Վերցված է 2008 թ․ հունվարի 9-ին.
- ↑ 46,0 46,1 46,2 Raymond, David (2006 թ․ ապրիլի 7). «Nuclear Binding Energies». New Mexico Tech. Արխիվացված է օրիգինալից 2002 թ․ դեկտեմբերի 1-ին. Վերցված է 2007 թ․ հունվարի 3-ին.
- ↑ Mihos, Chris (2002 թ․ հուլիսի 23). «Overcoming the Coulomb Barrier». Case Western Reserve University. Վերցված է 2008 թ․ փետրվարի 13-ին.
- ↑ Staff (2007 թ․ մարտի 30). «ABC's of Nuclear Science». Lawrence Berkeley National Laboratory. Արխիվացված է օրիգինալից 2006 թ․ դեկտեմբերի 5-ին. Վերցված է 2007 թ․ հունվարի 3-ին.
- ↑ Makhijani, Arjun; Saleska, Scott (2001 թ․ մարտի 2). «Basics of Nuclear Physics and Fission». Institute for Energy and Environmental Research. Արխիվացված է օրիգինալից 2007 թ․ հունվարի 16-ին. Վերցված է 2007 թ․ հունվարի 3-ին.
- ↑ Shultis, J. Kenneth; Faw, Richard E. (2002). Fundamentals of Nuclear Science and Engineering. CRC Press. էջեր 10–17. ISBN 0-8247-0834-2. OCLC 123346507.
- ↑ Fewell, M. P. (1995). «The atomic nuclide with the highest mean binding energy». American Journal of Physics. 63 (7): 653–658. Bibcode:1995AmJPh..63..653F. doi:10.1119/1.17828.
Աղբյուրներ
[խմբագրել | խմբագրել կոդը]- Manuel, Oliver (2001). Origin of Elements in the Solar System: Implications of Post-1957 Observations. Springer. ISBN 0-306-46562-0. OCLC 228374906.
Գրականություն
[խմբագրել | խմբագրել կոդը]- Dalton, J. (1808). A New System of Chemical Philosophy, Part 1. London and Manchester: S. Russell.
- Gangopadhyaya, Mrinalkanti (1981). Indian Atomism: History and Sources. Atlantic Highlands, New Jersey: Humanities Press. ISBN 0-391-02177-X. OCLC 10916778.
- Harrison, Edward Robert (2003). Masks of the Universe: Changing Ideas on the Nature of the Cosmos. Cambridge University Press. ISBN 0-521-77351-2. OCLC 50441595.
- Iannone, A. Pablo (2001). Dictionary of World Philosophy. Routledge. ISBN 0-415-17995-5. OCLC 44541769.
- King, Richard (1999). Indian philosophy: an introduction to Hindu and Buddhist thought. Edinburgh University Press. ISBN 0-7486-0954-7.
- Levere, Trevor, H. (2001). Transforming Matter – A History of Chemistry for Alchemy to the Buckyball. The Johns Hopkins University Press. ISBN 0-8018-6610-3.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - Liddell, Henry George; Scott, Robert. «A Greek-English Lexicon». Perseus Digital Library.
- Liddell, Henry George; Scott, Robert. «ἄτομος». A Greek-English Lexicon. Perseus Digital Library. Վերցված է 2010 թ․ հունիսի 21-ին.
- McEvilley, Thomas (2002). The shape of ancient thought: comparative studies in Greek and Indian philosophies. Allworth Press. ISBN 1-58115-203-5.
- Moran, Bruce T. (2005). Distilling Knowledge: Alchemy, Chemistry, and the Scientific Revolution. Harvard University Press. ISBN 0-674-01495-2.
- Ponomarev, Leonid Ivanovich (1993). The Quantum Dice. CRC Press. ISBN 0-7503-0251-8. OCLC 26853108.
- Roscoe, Henry Enfield (1895). John Dalton and the Rise of Modern Chemistry. Century science series. New York: Macmillan. Վերցված է 2011 թ․ ապրիլի 3-ին.
- Siegfried, Robert (2002). From Elements to Atoms: A History of Chemical Composition. DIANE. ISBN 0-87169-924-9. OCLC 186607849.
- Teresi, Dick (2003). Lost Discoveries: The Ancient Roots of Modern Science. Simon & Schuster. էջեր 213–214. ISBN 0-7432-4379-X.
- Various (2002). Lide, David R. (ed.). Handbook of Chemistry & Physics (88th ed.). CRC. ISBN 0-8493-0486-5. OCLC 179976746. Արխիվացված օրիգինալից 2008 թ․ մայիսի 23-ին. Վերցված է 2008 թ․ մայիսի 23-ին.
- Wurtz, Charles Adolphe (1881). The Atomic Theory. New York: D. Appleton and company. ISBN 0-559-43636-X.
Արտաքին հղումներ
[խմբագրել | խմբագրել կոդը]- The Feynman Lectures on Physics: Atoms in Motion
- "Quantum Mechanics and the Structure of Atoms" ՅուԹյուբում The actual physics lesson begins 2:20 into the video.
- Freudenrich, Craig C. «How Atoms Work». How Stuff Works. Արխիվացված օրիգինալից հունվարի 8, 2007-ին. Վերցված է 2007 թ․ հունվարի 9-ին.
- «The Atom». Free High School Science Texts: Physics. Wikibooks. Վերցված է 2010 թ․ հուլիսի 10-ին.
- Anonymous (2007). «The atom». Science aid+. Վերցված է 2010 թ․ հուլիսի 10-ին.—a guide to the atom for teens.
- Anonymous (2006 թ․ հունվարի 3). «Atoms and Atomic Structure». BBC. Արխիվացված օրիգինալից հունվարի 2, 2007-ին. Վերցված է 2007 թ․ հունվարի 11-ին.
- Various (2006 թ․ հունվարի 3). «Physics 2000, Table of Contents». University of Colorado. Արխիվացված օրիգինալից հունվարի 14, 2008-ին. Վերցված է 2008 թ․ հունվարի 11-ին.
- Various (2006 թ․ փետրվարի 3). «What does an atom look like?». University of Karlsruhe. Արխիվացված է օրիգինալից 2010 թ․ ապրիլի 17-ին. Վերցված է 2008 թ․ մայիսի 12-ին.
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 1, էջ 657)։ |
