Վիրուսներ
| Վիրուսներ | ||||
|---|---|---|---|---|
| Գիտական դասակարգում | ||||
|
||||
| Լատիներեն անվանում | ||||
| Viruses[նշում 1]
Fischlechner M, Donath E
|
||||
| Կարգեր | ||||
(շուրջ 70 ընտանիքներ չեն մտնում որևէ | ||||
|
|
Վիրուս (լատին․՝ virus՝ թույն), ոչ բջջային կառուցվածք ունեցող հարուցիչ, որը բազմանում է միայն կենդանի բջիջների ներսում։ Վիրուսները վարակում են կյանքի բոլոր բջջային ձևերը՝ կենդանիներից ու բույսերից մինչև բակտերիաներ և արքեաներ։
Վիրուսներն առաջին անգամ նկարագրվել են 1892 թվականին Դմիտրի Իվանովսկու կողմից որպես՝ ծխախոտի բույսերը վարակող ոչ բջջային ախտածիններ։ Ծխախոտի խճանկարի վիրուսը հայտնաբերել է Մարտին Բեյերինկը 1898 թվականին[2]։ Այդ ժամանակից ի վեր հայտնաբերվել և մանրամասն նկարագրվել են շուրջ 5000 տեսակի տարբեր վիրուսներ[3], չնայած այն բանին, որ հայտնի են վիրուսների միլիոնավոր ձևեր[4]։ Վիրուսներ հայտնաբերվել են գրեթե բոլոր էկոհամակարգերում և կենսաձևերից ամենաբազմաքանակն են[5][6]։ Վիրուսների մասին գիտությունը վիրուսաբանությունն է, որը մանրէաբանության (միկրոբիոլոգիա) ենթաճյուղերից է։
Վիրուսները բաղկացած են երկու կամ երեք մասերից (վիրիոններից)։
- բոլոր վիրուսներն ունեն գենետիկական նյութ՝ ԴՆԹ կամ ՌՆԹ։ Սրանք երկար մոլեկուլներ են, որոնք կրում են գենետիկական տեղեկատվությունը,
- բոլոր վիրուսներն ունեն սպիտակուցե կապսիդ, որը պաշտպանում է գեները,
- որոշ վիրուսներ ունեն նաև լիպիդային պատյան, որը շրջապատում է կապսիդը բջջից դուրս գտնվելու ժամանակ։
Վիրուսների ձևերը տարբեր են՝ հասարակ պարուրաձևից և իկոսաեդրից (քսանանիստից) մինչև ավելի բարդ կառույցներ։ Վիրուսի միջին մեծությունը կազմում է բակտերիայի մեծության մոտ 1/100-րդը[7]։ Վիրուսների մեծ մասը շատ փոքր են լուսային մանրադիտակով հայտնաբերվելու համար։
Վիրուսների էվոլյուցիոն ծագումն ամբողջությամբ պարզ չէ։ Հնարավոր է՝ նրանց մի մասը ծագել է բակտերիաներից։ Էվոլյուցիայում վիրուսները խաղում են կարևոր դեր գեների հորիզոնական տեղափոխման մեջ՝ սրանով նպաստելով գենետիկական բազմազանությանը[8]։ Որոշ գիտնականներ վիրուսները համարում են կենդանի ձևեր, քանի որ վերջիններս կրում են գենետիկական նյութ, վերարտադրվում են և բնական ընտրությամբ ենթարկվում էվոլյուցիայի։ Այնուամենայնիվ, վիրուսների մոտ բացակայում են կենդանի օրգանիզմներին բնորոշ որոշ կարևոր հատկանիշներ (ինչպիսին օրինակ բջջային կազմությունն է), որի պատճառով վիրուսներին անվանում են «կյանքի ոչ բջջային ձևեր»։
Վիրուսները տարածվում են բազմաթիվ ճանապարհներով. բույսերի վիրուսները փոխանցվում են բույսից բույս բուսահյութով սնվող միջատների միջոցով (օրինակ՝ լվիճներ), կենդանական վիրուսները փոխանցվում են արնախում միջատների միջոցով։ Այս եղանակով հիվանդությունը փոխանցող օրգանիզմներն անվանվում են վեկտորներ (փոխանցողներ)։ Գրիպի վիրուսները տարածվում են օդակաթիլային եղանակով՝ հազի և փռշտոցի միջոցով։ Ռոտավիրուսները փոխանցվում են երեխաների հետ անմիջական շփման հետևանքով։ ՄԻԱՎ-ը սեռական ճանապարհով և վարակված արյան ներարկմամբ փոխանցվող վիրուսներից է։ Վիրուսի կողմից վարակվող բջիջներն անվանվում են թիրախներ[9]։
Վիրուսային վարակը կենդանիների մոտ առաջացնում է իմունային պատասխան, որը սովորաբար ոչնչացնում է վարակող վիրուսին։ Իմունային պատասխան կարող է առաջանալ նաև պատվաստանյութի նկատմամբ, որով հնարավոր է դառնում առաջացնել արհեստական ձեռքբերովի իմունիտետ տվյալ վիրուսային հարուցչի դեմ։ Սակայն շատ վիրուսներ (ՁԻԱՀ-ի և վիրուսային հեպատիտի), կարողանում են խուսափել իմունային պատասխանից՝ առաջացնելով քրոնիկական վարակներ։ Հակաբիոտիկները ոչ մի ազդեցություն չեն ունենում վիրուսների վրա։ Մշակվել և ստեղծվել են որոշ հակավիրուսային դեղամիջոցներ։
Անվան ծագում[խմբագրել | խմբագրել կոդը]
«Վիրուսը» (լատին․՝ virus) լատիներեն բառ է, որն օգտագործվել է թույները և այլ վնասակար նյութերն անվանելու համար։ Առաջին անգամ օգտագործվել է Անգլիայում 1392 թվականին[10]։ «Վիրուլենտ» բառը ծագել է լատիներեն «virulentus»՝ թունավոր բառից, թվագրվում է 1400 թվականին[11]։ 1728 թվականից մինչև Դմիտրի Իվանովսկու կողմից վիրուսների հայտնաբերումը (1892) «վիրուս» բառը օգտագործվել է միայն «հարուցիչ» իմաստով[10]։ «Վիրուս» բառի հոգնակին հայերենում «վիրուսներ»-ն է, այն դեպքում, երբ լատիներեն բառը հավաքական գոյական է և չունի հոգնակի ձև։ «Վիրալ», «վիրուսային» (անգլ.՝ viral բառերն առաջին անգամ օգտագործվել է 1948 թվականին[12]։ «Վիրիոն» տերմինը (անգլ.՝ virion, հոգնակի՝ վիրիոններ), որը թվագրվում է 1959 թվականին[13], վիրուսի այն մասնիկն է, որը բջջից դուրս գալուց ընդունակ է վարակել նույն տեսակի այլ բջիջներ[14]։ 1981 թվականին հրատարակված «Ընդարձակ Բառարան Անգլիերէնէ Հայերէն»-ում վիրուս բառը թարգմանվում է «թույն», «ատելություն»[15]։ Իսկ «Օտար բառերի բառարանում» բառը թարգմանվում է՝ մարդու, կենդանիների և բույսերի վարակիչ հիվանդությունների հարուցիչներ[16]։
Պատմություն[խմբագրել | խմբագրել կոդը]

Վարակիչ հիվանդությունների ուսումնասիրությունները ցույց տվեցին, որ ոչ բոլոր հիվանդություններն են պայմանավորված բակտերիաներով, նախակենդանիներով և մանրադիտակային սնկերով։ Լուի Պաստյորը այդպես էլ չկարողացավ գտնել կատաղության հարուցիչը՝ ենթադրելով, որ հարուցիչը չափից դուրս փոքր է լուսային մանրադիտակով հայտնաբերվելու համար[17]։ Չարլզ Շամբերլանդը ստեղծեց մի ֆիլտր (Շամբերլանդի ֆիլտր կամ Շամբերլանդ-Պաստյորի ֆիլտր), որի անցքերը բակտերիաներից փոքր էին[18]։ 1892 թվականին ռուս կենսաբան Դմիտրի Իվանովսկին օգտագործեց այս ֆիլտրը ծխախոտի խճանկարի վիրուսի ուսումնասիրությունների համար։ Նա ցույց տվեց, որ վարակված ծխախոտի բույսի տերևներից ստացված հյութը շարունակում է պահպանել իր վարակունակությունը նույնիսկ Շամբերլանդի ֆիլտրով ֆիլտրումից հետո։ Իվանովսկին ենթադրում էր, որ հիվանդության պատճառը բակտերիաների արտադրած թույներն են[19]։
1898 թվականին հոլանդացի միկրոբիոլոգ Մարտին Բեյերինկը կրկնեց Իվանովսկու փորձերը և եզրահանգեց, որ ֆիլտրով անցնող վարակիչ նյութը պարունակում է դեռևս անհայտ հարուցիչներ[20]։ Նա նկատեց, որ այս հարուցիչները բազմանում են միայն բաժանվող բջիջներում, սակայն չբացահայտեց հարուցիչի իսկությունը։ Բեյերինկն այս նյութն անվանեց Contagium vivum fluidum (բառացի թարգմանությամբ՝ լատին․՝ լուծվող կենդանի մանրէ) և նորից գործածության մեջ դրեց վիրուս տերմինը[21]։ Բեյերինկը կարծում էր, որ վիրուսն իր բնույթով հեղուկ է։ Այս տեսությունը մերժեց Ուենդել Ստենլին, ով ապացուցեց, որ վիրուսները մասնիկներ են[21]։ Նույն թվականին Ֆրիդրիխ Լյոֆելը և Պաուլ Ֆրոշը հայտնաբերեցին առաջին կենդանական վիրուսը՝ դաբաղի հարուցիչը (աֆտովիրուս)[22]։
20-րդ դարի սկզբին անգլիացի բակտերիոլոգ Ֆրեդերիկ Թուերթը հայտնաբերեց բակտերիաներին վարակող վիրուսների մի խումբ և անվանեց դրանք «բակտերիոֆագեր» (ֆագեր)[23]։ Ֆրանս-կանադացի միկրոբիոլոգ Ֆելիքս Դ'Էրելը նկարագրեց վիրուսների մի տեսակ, որոնք ագարի վրա ավելացվելու դեպքում ձևավորում են մահացած բակտերիաների շերտ։ Փորձ կատարվեց ֆագերն օգտագործել տիֆի և խոլերայի բուժման համար, բայց դրանց փոխարինելու եկավ պենիցիլինը։ Հաշվելով մահացած բակտերիաների մակերեսը՝ Դ'Էրելը կարողացավ որոշել սկզբնական սուսպենզիայում վիրուսային մասնիկների քանակը[24]։
19-րդ դարի վերջում վիրուսները նկարագրվում էին իրենց վարակունակությամբ, ֆիլտրացիայի ընդունակությամբ և կենդանի թիրախների առկայության անհրաժեշտությամբ։ Վիրուսներն աճեցվում էին միայն կենդանիների և բույսերի մեջ։ 1906 թվականին Ռոսս Հարիսոնը մշակեց վիրուսների ավշային հյուսվածքում աճեցման մեթոդ, իսկ 1913 թվականին այս մեթոդն օգտագործվեց և կիրառվեց որպես պատվաստ՝ վիրուսը ծովախոզուկի եղջերաթաղանթի հյուսվածքի բջիջներում աճեցման նպատակով[25]։ 1928 թվակականին Գ. Բ. Մեյտլանդը և Մ. Կ. Մեյտնլանդը մանրացված հավի երիկամի սուսպենզիայում աճեցրեցին ծաղիկի վիրուսը։ 1950-ականների վերջում այս մեթոդն սկսվեց լայնորեն կիրառվել պոլիովիրուսի և պատվաստների ստեղծման նպատակով[26]։
Հետազոտությունների հաջորդ քայլը 1931 թվականին ամերիկացի ախտաբան Էրնեստ Ուիլյամ Գուդպաստյորի կողմից բեղմնավորված հավի ձվերի մեջ գրիպի վիրուսի աճեցումն էր[27]։
Վիրուսների առաջին նկարներն ստեղծվեցին էլեկտրոնային մանրադիտակի հայտնաբերումից հետո։ Ծխախոտի խճանկարի վիրուսը դարձավ առաջինը, որն առանձնացվեց, բյուրեղացվեց և բաժանվեց սպիտակուցների և ՌՆԹ-ի։ 1967 թվականին վիրուսներն առաջին անգամ արհեստականորեն սինթեզել են Ա. Քորենբերգը և Մ. Կուլայանը (ԱՄՆ)[28]։ 1949 թվականին Ջոն Ֆրանկլին Էնդերսը, Թոմաս Ուելլերը և Ֆրեդերիկ Ռոբինսը պոլիովիրուսը աճեցրեցին մարդու սաղմի կուլտուրայի վրա։ Սա կենդանիների հյուսվածքների վրա վիրուսի աճեցման առաջին փորձն էր։ Այս հետազոտությունների հետևանքով՝ Ջոնաս Սոլկը ստեղծեց պոլիոմիելիտի առաջին արդյունավետ պատվաստը[29]։

20-րդ դարի երկրորդ կեսին վիրուսները դարձան գենետիկական ինժեներիայի հիմնական օբյեկտները, հայտնաբերվեցին ավելի քան 2000 կենդանական, բուսական և բակտերիալ վիրուսներ[30]։ 1957 թվականին հայտնաբերվեցին ձիու արտերիվիրուսները և կովերի վիրուսային լուծի հարուցիչները՝ պեստիվիրուսները։ 1963 թվականին Բարուխ Բլամբերգը հայտնաբերեց հեպատիտ B-ի վիրուսը[31], իսկ 1965 թվականին Հուարդ Թեմինը նկարագրեց առաջին ռետրովիրուսները։ 1970 թվականին Թեմինը և Դեյվիդ Բատիմորը միմյանցից անկախ նկարագրեցին հակառակ տրանսկիպտազը[32]։ 1983 թվականին մի խումբ գիտնականներ Լյուկ Մոնտանյեի գլխավորությամբ Ֆրասնիայի Պաստյորի ինստիտուտից, առաջին անգամ առանձնացրեցին մի ռետրովիրուս, որը այժմ հայտնի է ՄԻԱՎ անվամբ[33].
1887 թվականին Բրյուստը լուսային մանրադիտակով տեսավ կովերի ծաղիկի վիրուսը։ Վերջինս իր չափերով ամենամեծն է, ինչի պատճառով այն ժամանակ կարծել էին, որ հիվանդության այս հարուցիչը վիրուս չէ[34]։ 1935 թվականին ամերիկացի կենսաքիմիկ և վիրուսաբան Ուենդել Մերեդիտ Սթենլին մանրամասն ուսումնասիրեց ծխախոտի խճանկարի վիրուսը և հայտնաբերեց, որ այն առավելապես կազմված է սպիտակուցներից[35]։ Կարճ ժամանակ անց այս վիրուսից առանձնացվեցին սպիտակուցային և նուկլեինաթթվային բաղադրամասերը[36]։ Ծխախոտի խճանկարի վիրուսը առաջին բյուրեղացված վիրուսն է։ Դրա առաջին ռենտգենոգրամը պատրաստել են Բերնալը և Ֆունկուխենը 1930-ական թվականների վերջին։ Այս պատկերների հիման վրա Ռոզալինդ Ֆրանկլինը 1955 թվականին սահմանեց վիրուսի ամբողջական կառուցվածքը[37]։ Նույն ժամանակահատվածում Հայնց Ֆրենկել Կոնրատը և Ռոբլի Ուիլյամսը ցույց տվեցին, որ ծխախոտի խճանկարի վիրուսի ՌՆԹ-ն և թաղանթի սպիտակուցը ֆունկցիոնալ վիրուսում կարող են ինքնահավաքվել։ Հետազոտողները եզրակացրին, որ բոլոր վիրուսները ունեն բջիջներում հավաքման նմանատիպ մեխանիզմներ[38]։
2002 թվականին Նյու Յորքի համալսարանում ստեղծվեց առաջին սինթետիկ վիրուսը (պոլիոմելիտի վիրուս)[39]։
Վիրուսաբանությունը Հայաստանում[խմբագրել | խմբագրել կոդը]
Հայաստանում վիրուսներն ուսումնասիրող գիտական կառույցներն են ՀՀ ԳԱԱ մոլեկուլային կենսաբանության ինստիտուտը և Ա. Բ. Ալեքսանյանի անվան համաճարակաբանության, վիրուսաբանության և բժշկական մակաբուծաբանության գիտահետազոտական ինստիտուտը[40]։ Մոլեկուլային կենսաբանության ինստիտուտում զբաղվում են մարդու համար ոչ վտանգավոր վիրուսների, մասնավորապես կենդանական հիվանդությունների վիրուսների հետազոտմամբ[41]։ Օրինակ՝ մարդու և կենդանիների բջջային կուլտուրանների ուսումնասիրություններով բացահայտվել են կայուն բջիջների առաջացման ժամանակ վիրուսների ընտրողական ազդեցության մեխանիզմները։ Ցույց է տրվել, որ անէուպլոիդ գենոմով բազմակորիզակային բջիջներում վիրուսներն առաջացնում են ապոպտոզ և կարող են ձևափոխել բջիջները՝ առաջացնելով դիպլոիդ պոպուլացիաներ[42][43]։
Համաճարակաբանության, վիրուսաբանության և բժշկական մակաբուծաբանության ԳԻ-ում զբաղվել և զբաղվում են մի շարք վիրուսային հիվանդությունների՝ բնական ծաղկի, վիրուսային A, B, C, E հեպատիտների, արբովիրուսային վարակիչ հիվանդությունների ախտորոշման, կանխարգելման և պայքարի միջոցառումների մշակման հարցերով։
Ծագում[խմբագրել | խմբագրել կոդը]
Վիրուսները հանդիպում են ամենուր, որտեղ կա կյանք և, ամենայն հավանականությամբ, գոյություն են ունեցել և էվոլուցվել՝ առաջին կենդանի բջիջների հետ[44] միաժամանակ։
Վիրուսների ծագման վարկածները միանշանակ չեն. վիրուսները չեն թողնում բրածո մնացորդներ, ժառանգական հարաբերությունները հնարավոր է պարզել միայն մոլեկուլային ֆիլոգենետիկայով։ Վիրուսների էվոլյուցիայի հիմնական մեթոդը մոլեկուլյար կենսաբանական մեթոդն է՝ վիրուսի ԴՆԹ-ի կամ ՌՆԹ-ի համեմատությունը[45]։
Առաջացման տեսություններ[խմբագրել | խմբագրել կոդը]

Վիրուսների ծագման վերաբերյալ գոյություն ունի երեք հիմնական տեսություն՝ ռեգրեսիայի, բջջային ծագման և կոէվոլյուցիայի տեսությունները[46][47]։
Ռեգրեսիայի տեսություն[խմբագրել | խմբագրել կոդը]
Վիրուսները հնարավոր է, որ ժամանակին եղել են մանր բջիջներ, որոնք մակաբուծել են ավելի մեծ բջիջներում։ Ժամանակի ընթացքում, այն գեները, որոնք անմիջականորեն կապված չեն եղել մակաբուծության հետ՝ անհետացել են։ Ռիկետսիա բակտերիան և քլամիդիան վիրուսների պես վերարտադրվում են միայն տիրոջ բջիջներում։ Վիրուսների՝ որպես մակաբույծի զարգացումը պատճառ է դարձել որոշ գեների կորստին և թույլ է տվել նրանց գոյատևել բջջից դուրս։ Այս տեսությունն անվանվում է նաև «դեգեներացիայի տեսություն»[48][49] կամ ռեդուկցիայի վարկած[50]։
Բջջային ծագման տեսություն[խմբագրել | խմբագրել կոդը]
Որոշ վիրուսներ հնարավոր է, որ զարգացել են ԴՆԹ-ի և ՌՆԹ-ի այն հատվածներից, որոնք «ազատվել են» ավելի մեծ կենդանի օրգանիզմի գեներից։ Այսպիսի հատվածներ կարող էին ձևավորվել պլազմիդներից կամ տրանսպոզոններից[51]։ Տրանսպոզոնները (նախկին անվանումը՝ «թռչող գեներ») շարժուն գենետիկական տարրերի օրինակներ են, որոնք հայտնաբերվել են 1950 թվականին Բարբարա Մաք Քլինտոկի կողմից եգիպտացորենի գենոմում[52]։ Այս վարկածն անվանում են նաև «թափառման»[53][54] կամ «փախուստի վարկած»[50]։
Կոէվոլյուցիայի տեսություն[խմբագրել | խմբագրել կոդը]
Այս տեսությունն անվանվում է նաև «սկզբում վիրուսն էր» տեսություն։ Համաձայն այս տեսության՝ վիրուսները կարող էին զարգանալ սպիտակուցների և նուկլեինաթթուների բարդ մոլեկուլներից՝ Երկրի վրա առաջին բջիջների ի հայտ գալուն զուգահեռ. վիրուսները կախված են եղել բջջային կյանքից միլիոնավոր տարիներ։ Վիրիոիդները ՌՆԹ-ի մոլեկուլներ են, որոնք վիրուսներ չեն համարվում, քանի որ չունեն սպիտակուցային կապսիդ։ Չնայած դրան՝ վիրիոիդները օժտված են այնպիսի հատկանիշներով, որոնք բնորոշ են վիրուսներին, դրա համար էլ հաճախ անվանվում են ենթավիրուսային մասնիկներ[55]։ Վիրիոիդները բույսերի տարածված ախտածիններ են[56], նրանք չեն գաղտնագրում սպիտակուցներ, բայց ներխուժում են թիրախ բջջի կենսական պրոցեսների մեջ և վերարտադրվում[57]։ Հեպատիտ D-ի վիրուսն ունի ՌՆԹ գենոմ, սակայն միայնակ չի կարող սինթեզել սպիտակուցային թաղանթի սպիտակուցները։ Վիրուսային մասնիկների ձևավորման համար, այն օգտագործում է հեպատիտ B-ի վիրուսի կապսիդի սպիտակուցները. այս պատճառով հեպատիտ D-ի վիրուսը ընդունակ է բազմանալ միայն այն բջիջներում, որոնք վարակված են հեպատիտ B-ով։ Հեպատիտ D-ի վիրուսը դեֆեկտավոր է[58]։ Սպուտնիկ վիրոֆագը (անգլ.՝ sputnik virophage) նմանապես կախված է Acanthamoeba castellanii նախակենդանիները վարակող միմիվիրուսից[59]։ Դրանք հայտնի են որպես արբանյակ-վիրուսներ, քանի որ կախված են այլ վիրուսի առկայությունից։ Ենթադրում են, որ արբանյակ-վիրուսները վիրուսների և վիրիոնների միջանկյալ օղակն է[60][61]։
Այդքանով հանդերձ՝ Ռեգրեսիայի տեսությունը չի բացատրում, թե ինչու նույնիսկ ամենափոքր բջջային մակաբույծները վիրուսներին չեն նմանվում։ Փախուստի վարկածը չի կարողանում բացատրել կապսիդի և վիրուսի այլ կառույցների ծագումը։ Կոէվոլյուցիայի տեսությունը հակասում է վիրուսի «տեր բջջից կախված ոչ բջջային տարր» բնորոշմանը[50]։
Անցյալում այս երեք տեսությունների շուրջ ծագել են բազմաթիվ վեճեր։ Այժմ վիրուսները համարվում են շատ հին ծագմամբ մասնիկներ, որոնք ծագել են նախքան կյանքի երեք վերնաթագավորությունների առաջացումը[62]։
ՌՆԹ աշխարհի մասին գոյություն ունեցող փաստերը և վիրուսների ու թիրախ բջիջների գենոմի համակարգչային անալիզը թույլ տվեց ավելի լավ հասկանալ տարբեր վիրուսների միջև եղած էվոլյուցիոն կապերը, պարզել ժամանակակից վիրուսների նախնիներին։ Մինչ այժմ վերոնշյալ երեք տեսություններից ոչ մեկն ամբողջությամբ ապացուցված չէ։ Այնուամենայնիվ, հերքվում է այն փաստը, որ բոլոր վիրուսներն ունեցել են միանման ծագում և ընդհանուր նախնի[63]։ Պրիոնները վարակունակ սպիտակուցների մոլեկուլներ են, որոնք չեն պարունակում ԴՆԹ կամ ՌՆԹ[64]։
ՌՆԹ աշխարհ[խմբագրել | խմբագրել կոդը]
ՌՆԹ աշխարհի վարկածը[65] և տիրոջ ու վիրուսային ՌՆԹ-ի ու ԴՆԹ-ի համակարգչային վերլուծությունը թույլ է տալիս ավելի լավ հասկանալ վիրուսների տարբեր խմբերի միջև գոյություն ունեցող էվոլյուցիոն կապերը և օգնում է ժամանակակից վիրուսների նախնիների որոշման հարցում։ Մինչև օրս, սակայն, հայտնի չէ, թե վերոնշյալ երեք վարկածներից, որն է ճիշտը[65]։ Ենթադրվում է, որ քիչ հավանական է բոլոր վիրուսների մեկ ընդհանուր նախնու գոյությունը. ամենայն հավանականությամբ անցյալում վիրուսների որոշակի խմբեր առաջացել են միմյանցից անկախ, քանի որ վիրուսների խմբերը ունեն գենետիկական նյութի կազմակերպման զգալիորեն տարբերվող մեխանիզմներ[66]։
Պրիոններ[խմբագրել | խմբագրել կոդը]

Պրիոնները վարակունակ սպիտակուցի մոլեկուլներ են, որոնք չեն պարունակում ԴՆԹ կամ ՌՆԹ[64]։ Պրիոնները կարող են առաջացնել ոչխարների մարմաջ[67], խոշոր եղջերավոր անասունների սպունգային էնցեֆալոպատիա, եղնիկների քրոնիկական հոգնածություն (անգլ.՝ chronic wasting disease) և այլ հիվանդություններ։ Մարդու պրիոններով պայմանավորված հիվանդություններից է կուրուն, Կրայցֆելդ-Յակոբի հիվանդությունը և Գերստման-Շտրաուսլեր-Շայնկերի ախտանիշը[68]։ Պրիոնները կարող են խթանել սեփական կրկնօրինակների առաջացումը։ Պրիոնի սպիտակուցը կարող է գոյություն ունենալ երկու՝ նորմալ (PrPC) և պրիոնային (PrPSc) իզոձևերով։ Պրիոնային ձևը փոխհարաբերվելով նորմալ ձևի հետ կարող է մասնակցել նրա պրիոնային ձևին անցնելուն։ Չնայած պրիոնները զգալիորեն տարբերվում են վիրուսներից և վիրոիդներից, նրանց հայտնաբերումը թույլ է տալիս ենթադրել, որ վիրուսները կարող էին ձևավորվել ինքնավերարտադրվող մոլեկուլներից[69]։
Միկրոբիոլոգիա[խմբագրել | խմբագրել կոդը]
Վիրուսների կենդանի լինելու խնդիրը[խմբագրել | խմբագրել կոդը]
Վիրուսները բնորոշելիս գիտնականների մի մասն այն սահմանում է որպես կյանքի ձևեր, մյուսները՝ օրգանիզմների հետ փոխհարաբերության մեջ մտնող օրգանական կառույցներ. հստակ մոտեցում դեռ չի ձևավորվել։ Վիրուսները բնորոշվել են որպես «կյանքի սահմանում գտնվող օրգանիզմներ»[22], քանի որ պարունակում են գեներ, բնական ընտրությամբ ենթարկվում էվոլյուցիայի, կարողանում են վերարտադրվել[70]։ Չնայած որ վիրուսներն ունեն ժառանգական նյութ՝ նրանք չունեն բջջային կառուցվածք, որը համարվում է կենդանի աշխարհի հիմնական հատկությունը։ Վիրուսները չունեն սեփական նյութափոխանակություն, նյութերի սինթեզի համար անհրաժեշտ է տեր բջջի առկայությունը։ Սրա պատճառով վիրուսներն ընդունակ չեն բազմանալ բջջից դուրս[71]։ Հատկանշական է, որ ռիկետսիաներն ու քլամիդիաները նույնպես չեն կարող բազմանալ տեր բջջից դուրս, սակայն համարվում են կենդանի օրգանիզմներ[72][73]։ Վիրուսները ժառանգում են մուտացիաներ և ենթարկվում են բնական ընտրության. սա է բյուրեղների աճից վիրուսների բազմացման տարբերությունը։ Բջջում վիրուսային մասնիկների ինքնահավաքումը հավելյալ վկայություն է այն մասին, որ կյանքը կարող էր ծագել ինքնահավաքվող օրգանական մոլեկուլներից[74]։ 2013 թվականին ցույց տրվեց, որ որոշ բակտերիոֆագեր ունեն հարմարման ընդունակ իմունային համակարգ[75], որը կողմ փաստարկ է վիրուսների կենդանի լինելու վարկածի օգտին։
Կառուցվածք[խմբագրել | խմբագրել կոդը]

А. Լիպիդային պատյան չունեցող վիրուս (օրինակ՝ պիկորնավիրուսներ).
B. Լիպիդային պատյանով վիրուս (օրինակ՝ հերպեսվիրուսներ)
Թվերով ներկայացված են (1) կապսիդ, (2) գենոմային նուկլեինաթթու, (3) կապսոմեր, (4) նուկլեոկապսիդ, (5) վիրիոն, (6) լիպիդային պատյան, (7) պատյանի թաղանթային սպիտակուցները
Վիրուսներն ունեն ձևերի և չափերի հսկայական բազմազանություն։ Որպես կանոն, վիրուսներն ավելի փոքր են, քան բակտերիաները։ Վիրուսների մեծ մասը 15–300 նանոմետր է (նանոմետրը միլիմետրի մեկ միլիոներորդ մասն է) սահմաններում։ Որոշ ֆիլովիրուսներ ունեն 1400 նմ երկարություն և 80 նմ տրամագիծ[76]։ Մինչև 2013 թվականը ամենամեծ վիրուսը համարվում էր Pandoravirus-ը որն ուներ 1x0,5 մկմ չափեր։ 2014 թվականի մարտի դրությամբ ամենամեծ վիրուսն է համարվել Սիբիրի հավերժական սառույցներում հայտնաբերված Pithovirus-ը, որն ունի 1,5x0,5 մկմ չափեր[77]։ Վիրիոնների մեծ մասը անհնար է տեսնել լուսային մանրադիտակով, դրա համար օգտագործում են էլեկտրոնային մանրադիտակներ[78]։ Որպեսզի վիրուսը ընդգծվի շրջապատող միջավայրի ֆոնի վրա օգտագործում են հատուկ «ներկեր», որոնք ծանր մետաղների աղեր են, ցրում են մակերևույթի էլեկտրոնները։ Այսպիսի վերամշակումը, սակայն, վատացնում է մանր մասնիկների տեսանելիությունը։ Նեգատիվ «ներկման» ժամանակ «ներկվում» է միայն ֆոնը[79]։
Հասուն վիրուսային մասնիկը՝ վիրիոնը, կազմված է սպիտակուցային պաշտպանիչ թաղանթով՝ կապսիդով պատված նուկլեինաթթվից։ Կապսիդը, իր հերթին, կառուցվում է միանման սպիտակուցային ենթամիավորներից՝ կապսոմերներից[80]։ Վիրուսները կարող են ունենալ նաև լիպիդային պատյան, որը ձևավորվում է տիրոջ բջջաթաղանթից։ Լիպիդային պատյանը ծածկում է կապսիդը և հաճախ անվանվանվում է նաև «սուպերկապսիդ»։ Կապսիդի սպիտակուցները գաղտնագրվում են վիրուսային գենոմի միջոցով և նրանց ձևը ընկած է վիրուսների ձևաբանական դասակարգման հիմքում[81][82]։ Առավել բարդ կառուցվածք ունեցող վիրուսները կարող են գաղտնագրել նաև հատուկ սպիտակուցներ, որոնք օգնում են կապսիդի հավաքմանը։ Սպիտակուցների և նուկլեինաթթուների համակարգերը հայտնի են նուկլեոպրոտեիններ անվամբ. նմանապես՝ կապսիդի և նուկլեինաթթովի համալիրն անվանվում է նուկլեոկապսիդ։ Կապսիդի և վիրիոնի ձևը կարելի է ուսումնասիրել սկանավորող ատոմաուժային մանրադիտակի միջոցով[83][84].
Արքեաներին վարակող որոշ վիրուսներ իրենց ձևով տարբերվում են վիրուսների մյուս խմբերից[85]։
Կապսիդ[խմբագրել | խմբագրել կոդը]


Վիրուսի կապսիդը ըստ ձևի ու տեսքի կարող է լինել պարուրաձև, իկոսաեդրային, երկարացված և բարդ։
Պարուրաձև[խմբագրել | խմբագրել կոդը]
Այս կապսիդը կազմված է մեկ տեսակի կապսոմերից, որը դասավորվելով կենտրոնական առանցքի շուրջը ստեղծում է պարուրաձև խողովակ. խողովակի ներքին խոռոչում կամ խողովակում տեղադրվում է վիրուսի ժառանգական նյութը։ Կապսիդի այսպիսի կառուցվածքը վիրիոնին տալիս է ցուպիկաձև կամ թելաձև տեսք, վիրիոնը կարող է լինել կարճ և խիտ կամ երկար և ճկուն։ Գենետիկական նյութը հիմնականում միապարույր կամ երկպարույր ՌՆԹ-ն է, որոշ դեպքերում՝ միաշղթա ԴՆԹ-ն։ Բացասական լիցքավորված նուկլեինաթթուն փոխազդեցության մեջ է մտնում դրական լիցքավորված սպիտակուցի հետ, այս միջոցով նուկլեինաթթուն ամրանում է խոռոչում։ Պարուրաձև կապսիդի երկարությունը սովորաբար կախված է նուկլեինաթթվի երկարությունից, իսկ տրամագիծը՝ կապսոմերների չափերից և դասավորությունից։ Ծխախոտի խճանկարի վիրուսը պարուրաձև վիրուսի դասական օրինակ է[86]։
Իկոսաեդրային[խմբագրել | խմբագրել կոդը]
Կենդանական վիրուսների մեծ մասը ունեն քսանանիստի (իկոսաէդրի) կամ իկոսաեդրային համաչափություն ունեցող գնդի ձև։ Քսանանիստը սովորաբար շատ հարմար է ստեղծել միանման ենթամիավոներից։ Կապսոմերների նվազագույն քանակը 12-ն է, որոնցից յուրաքանչյուրը կազմված են 5 միանման ենթամիավորներից։ Շատ վիրուսներ, օրինակ՝ ռոտավիրուսն, ունեն ավելի քան 12 կապսոմեր, գնդաձև են, բայց պահպանում են իկոսաէդրային համաչափությունը։ Գագաթներում գտնվող կապսոմերները շրջապատված են այլ 5 կապսոմերներով և անվանվում են «պենտոններ»։ Եռանկյունաձև նիստերի կապսոմերներն ունեն 6 հարևան կապսոմերներ և անվանվում են «հեքսոններ»[87]։ Հեքսոնները տափակ են, իսկ 12 գագաթ ձևավորող պենտոնները կորացած են։ Միևնույն սպիտակուցը կարող է դառնալ և՛ պետոմերների, և՛ հեքսամերների ենթամիավորներ։
Երկարացած[խմբագրել | խմբագրել կոդը]
Երկարացած անվանում են այն քսանանիստային կապսիդներին, որոնք երկարացված են հինգերորդ կարգի սիմետրիայի առանցքի երկայնքով։ Բակտերիոֆագերի գլխիկը սովորաբար ունի այսպիսի կառուցվածք[88]։
Բարդ կապսիդ[խմբագրել | խմբագրել կոդը]
Բարդ վիրուսների կապսիդը ամբողջությամբ պարուրաձև և քսանանիստային չէ։ Այս վիրուսները սովորաբար ունենում են լրացուցիչ արտաքին կառույցներ, ինչպիսին օրինակ՝ սպիտակուցային պոչն է կամ բարդ արտաքին պատեր։ Որոշ բակտերոֆագեր (օրինակ՝ T4 ֆագը) ունի իկոսաէդրային գլխիկից և պարուրաձև պոչից բաղկացած բարդ կապսիդ։ Պոչը գործում է մոլեկուլային ներարկիչի պես, ամրանում է տեր բջջին և նրա մեջ ներարկում ֆագի գենետիկական տեղեկատվությունը[89]։
Պատյան[խմբագրել | խմբագրել կոդը]

Որոշ վիրուսներ ունեն լրացուցիչ պատյան, որը բջջապատյանի ձևափոխությունն է։ Լրացուցիչ երկշերտ լիպիդային այս պատյանն անվանվում է սուպերկապսիդ։ Վիրուսի լիպիդային պատյանում կան տիրոջ և վիրուսի գենոմներով գաղտնագրվող սպիտակուցներ, լիպիդները և ածխաջրերը գաղտնագրվում են միայն տեր բջջի գենոմով։ Լիպիդային պատյան ունեն օրինակ գրիպի վիրուսը և ՄԻԱՎ-ը։ Պատյանավոր վիրուսների մեծամասնության վարակունակությունը պայմանավորված է հենց պատյանով[90]։
Պոքսվիրուսները յուրահատուկ ձևաբանությամբ բարդ կառուցվածք ունեցող վիրուսներ են։ Վիրուսի գենետիկական նյութը սպիտակուցների հետ միացած գտնվում է կենտրոնական սկավառակաձև կառույցում՝ նուկլեոտիդում։ Նուկլեոտիդը շրջապատված է թաղանթով և անհայտ ֆունկցիա ունեցող երկու կողմնային մարմնիկներով։ Վիրուսն ունի մակերեսին մեծ քանակով սպիտակուցներ կրող արտաքին պատյան։ Վիրիոնը պլեյոմորֆ է՝ պայմաններից կախված կարող է փոխել ձևը և չափսերը։ Վիրիոնը կարող է ընդունել էլիպսաձև կամ ճախարակաձև[91] տեսք։ Ամենամեծ նկարագրված վիրուսներից մեկի՝ միմիվիրուսի կապսիդը իկոսաեդրային է՝ 400-500 նմ տրամագծով։ Վիրիոնի մակերեսից դուրս եկող սպիտակուցային թելիկները ունեն 100 նմ երկարություն[92][93]։ 2011 թվականին հետազոտողները Չիլիի մերձափնյա շրջանում հայտնաբերեցին ավելի խոշոր մի վիրուս, որն ստացավ Megavirus chilensis անվանումը։ Այս վիրուսին կարելի է դիտել նույնիսկ սովորական լուսային մանրադիտակով[94]։
Գենոմ[խմբագրել | խմբագրել կոդը]
| Հատկություն | Տեսակ |
|---|---|
| Նուկլեինաթթու |
|
| Ձև |
|
| Շղթաների քանակը |
|
| Բևեռայնություն |
|
Վիրուսների մոտ հանդիպում են գենոմի կազմավորման տարատեսակ ձևեր. այդ առումով նրանք ավելի բազմազան են, քան բույսերը, կենդանիները, արքեաներն ու բակտերիաները։ Գոյություն ունեն վիրուսների միլիոնավոր տեսակներ[4], բայց դրանցից մանրամասն նկարագրվել են միայն մոտ 5000-ը[95]։ Վիրուսի գենետիկական նյութը կարող է կազմված լինել կամ ԴՆԹ-ից կամ ՌՆԹ-ից, ըստ դրա տարբերակում են ԴՆԹ և ՌՆԹ վիրուսներ. մեծամասնությունը կազմում են ՌՆԹ վիրուսները։ Բույսերի վիրուսները սովորաբար պարունակում են միաշղթա ՌՆԹ, իսկ բակտերոֆագերը, որպես կանոն՝ երկշղթա ԴՆԹ[96]։
Վիրուսների գենոմը կարող է լինել օղակաձև ինչպես պոլիոմավիրուսների մոտ կամ գծաձև՝ ինչպես ադենովիրուսների մոտ է։ Գենոմի ձևը կապված չէ նուկլեինաթթվի բնույթից։ Շատ ՌՆԹ և որոշ ԴՆԹ վիրուսների մոտ գենոմը ներկայացված է մի քանի մոլեկուլներից (հատվածներից), որի պատճառով նրանք անվանվում են «հատվածավորված» (սեգմենտավորված)։ ՌՆԹ վիրուսների մոտ յուրաքանչյուր սեգմենտը կոդավորում է միայն մեկ սպիտակուց և սովորաբար փաթեթավորված է մեկ կապսիդում[76]։ Չնայած դրան, վարակ առաջացնելու համար անհրաժեշտ են վիրուսի ոչ բոլոր սեգմենտները։
Վիրուսային գենոմներն անկախ նուկլեինաթթվի բնույթից լինում են կամ միաշղթա, կամ երկշղթա։ Երկշղթա գենոմն ընդգրկում է մի շարք կոմպլեմենտար նուկլեինաթթուների շղթաներ, իսկ միաշղթան՝ միայն մեկ շղթա։ Վիրուսների որոշ ընտանիքների գենոմները մասամբ երկշղթա են, մասամբ՝ միաշղթա (օրինակ՝ հեպադնավիրուսների մոտ)[96]։
ՌՆԹ վիրուսների մեծամասնության և որոշ ԴՆԹ վիրուսների համար որոշում են նաև նուկլեինաթթվի բևեռայնությունը, որը կախված վիրուսային ՌՆԹ-ին կոմպլիմենտար լինելուց կարող է լինել դրական կամ բացասական (դրական շղթա կամ բացասական շղթա)։ Դրական շղթան ունի նուկլեոտիդների նույն հաջոորդականությունը ինչ մՌՆԹ-ն, դրա համար նրա մի մասը կարող է անմիջապես տրանսլացվել։ Բացասական բևեռայնությամբ կոմպլեմենտար է մՌՆԹ-ին. մինչև տրանսլյացիայի սկիզբը անհրաժեշտ է, որ այս շղթայի հիման վրա ՌՆԹ-կախյալ-ՌՆԹ-պոլիմերազի[96] միջոցով սինթեզվի ՌՆԹ-ի դրական շղթան։ ԴՆԹ վիրուսների համար շղթաների անվանումները նման են ՌՆԹ վիրուսների համապատասխան շղթաների անվանումներն։ Որոշ ԴՆԹ և ՌՆԹ վիրուսների գենոմը ունի տարբեր բևեռայնություն՝ տրանսկրիպցիայի կարող է ենթարկվել ցանկացած շղթա։ Այդ վիրուսներից են գեմինիվիրուսները (միաշղթա ԴՆԹ-ով բուսական վիրուսներ) և արենավիրուսները (կենդանական վիրուսներ միաշղթա ՌՆԹ-ով)[97]։
Գենոմի մեծությունը տարբեր տեսակների մոտ տարբեր է։ Ամենափոքր միաշղթա ԴՆԹ-ով օժտված է ցիրկովիրուսը՝ Circoviridae ընտանիքից, որը պարունակում է շուրջ 2000 նուկլեոտիդ։ Ամենամեծ գենոմներից մեկը ունի միմիվիրուսը։ Այն պարունակում է ավելի քան 1,2 միլիոն զույգ ազոտային հիմք և կոդավորում՝ հազարից ավելի սպիտակուցներ[98]։ Որպես կանոն ՌՆԹ վիրուսներն ունեն ավելի փոքր գենոմ, քան ԴՆԹ վիրուսները, գենոմի չափը սահմանափակ է ռեպլիկացիայի ժամանակ սխալների մեծ հավանականության պատճառով[45]։ Ռեպլիկացիայի ժամանակ տեղի ունեցող սխալների մեծ քանակը կվտանգեր վիրուսի գոյությունը։ Այս սահմանափակման հաղթահարման համար շատ ՌՆԹ վիրուսների գենոմներ սեգմենտավորված են։ Ի հակադրություն, ԴՆԹ վիրուսները սովորաբար ունեն մեծ գենոմ՝ սխալների քիչ հավանականության և կրկնապատկմանը մասնակցող ֆերմենտների հաշվին[99]։ Բացառություն են կազմում միայն միաշղթա ԴՆԹ ունեցող վիրուսները, որոնց մոտ մուտացիաների կուտակման արագությունը նույնն է ինչ միաշղթա ՌՆԹ վիրուսների մոտ[100]։
Վիրուսների մոտ գենետիկական փոփոխականությունն ընթանում է տարբեր կերպ։ Դրանցից է օրինակ ԴՆԹ-ի կամ ՌՆԹ-ի շղթաներում նուկլեոտիդների պատահական փոխարինումները։ Այս կետային մուտացիաները մեծ մասամբ «թաքնված» են՝ չեն փոխում այդ գեներով գաղտնագրվող սպիտակուցների կառուցվածքը։ Հազվադեպ մուտացիաները կարող են բերել վիրուսի մոտ նոր հատկությունների ձևավորմանը, ինչպիսին օրինակ հակավիրուսային դեղամիջոցների հանդեպ դիմացկունությունն է[101]։ Հակամարմինների դրեյֆի ժամանակ գենոմում տեղի են ունենում հսկայական փոփոխություններ։ Հակամարմինների դրեյֆի պատճառ կարող է լինել ռեկոմբինացիան կամ ռեասորտիմենտը։ Երբ գրիպի վիրուսը ենթարկվում է հակամարմինների դրեյֆի, հնարավոր է առաջանա համավարակ[102]։ ՌՆԹ վիրուսները շատ հաճախ գոյություն ունեն կվազիձևերով, որը վիրուսի նույն տեսակն է, սակայն գենոմի նուկլեոտիդների հաջորդականությունը տարբեր է։ Այս կվազիձևերը բնական ընտրության հիմնական թիրախն են[103]։
Սեգմենտավորված գենոմը տալիս է էվոլյուցիոն առավելություններ՝ սեգմենտավորված գենոմով վիրուսի տարբեր շտամներ կարող են փոխանակել գեներ և ձևավորել յուրահատուկ հատկություններով օժտված նոր սերունդներ։ Այս երևույթն անվանվում է ռեասորտիմենտ[104]։
Գենետիկական ռեկոմբինացիան մի գործընթաց է, որի ժամանակ տեղի է ունենում նուկլեինաթթվի մոլեկուլի խզում և առաջացած հատվածների միացում՝ այլ հաջորդականությամբ։ Ռեկոմբինացիան կարող է տեղի ունենալ երկու վիրուսի գենոմների միջև, երբ վերջիններս միաժամանակ վարակել են միևնույն բջիջը։ Վիրուսների էվոլյուցիոն ուսումնասիրությունը ցույց է տվել, որ վիրուսների մոտ ռեկոմբինացիան լայնորեն տարածված է[105]։ Ռեկոմբինացիան բնորոշ է և ՌՆԹ և ԴՆԹ վիրուսների համար[106][107]։
Բազմացման ցիկլ[խմբագրել | խմբագրել կոդը]


Վիրուսները բջջային օրգանիզմներ չեն և չեն բազմանում բջջի բաժանմամբ։ Նրանք օգտագործում են տեր բջջի ռեսուրները՝ սեփական կրկնօրինակների ստեղծման և վիրուսի հավաքման նպատակով։
Վիրուսի կյանքի ցիկլը կարելի է բաժանել մի քանի պայմանական (սովորաբար 6) խմբերի։ Դրանք են[108]՝
- ամրացում (ադսորբցիա)
- թափանցում
- ապապատիճավորում (դեկապսիդացիա)
- տրանսկրիպցիա
- նուկլեինաթթուների ռեպլիկացիա և այլ վիրուսային միացությունների սինթեզ
- հավաքում և ելք բջջից
Ամրացում[խմբագրել | խմբագրել կոդը]
Ամրացումը կամ ադսորբցիան վիրուսի կապսիդի սպիտակուցների միացումն է տեր բջջի ռեցեպտորներին։ Այս ամրացումը որոշում է վիրուսի հնարավոր տերերի միջակայքը։ ՄԻԱՎ-ն, օրինակ, վարակում է միայն հատուկ տեսակի լեյկոցիտներ։ Սրա պատճառն այն է, որ ՄԻԱՎ-ի կապսիդի gp120 գլիկոպրոտեինը փոխազդեցության մեջ է մտնում CD4 (քեմոկինային ռեցեպտոր) մոլեկուլների հետ, որը հանդիպում է հիմնականում CD4+ T-լիմֆոցիտների մակերեսի վրա։ Վիրուսի ամրացման տեսակը որոշվում է վիրուսների տիպով, բջիջների բազմազանության խտացումով, իոնների կենտրոնացումով և ջերմաստիճանով։ Ռեցեպտորի հետ միացումը կարող է բերել կապսիդի կամ լիպիդային թաղանթի սպիտակուցների կառուցվածքային և ձևաբանական փոփոխությունների, որին հաջորդում է վիրուսային և բջջային թաղանթների ձուլումը և վիրուսի թափանցումը։
Թափանցում[խմբագրել | խմբագրել կոդը]
Կյանքի ցիկլի հաջորդ փուլում վիրուսը բջիջ է տեղափոխում իր գենետիկական տեղեկատվությունը։ Վիրիոնները բջիջ են թափանցում ռեցեպտոր միջնորդավորված էնդոցիտոզի կամ թաղանթի միաձուլման միջոցով։ Այս պրոցեսը հաճախ անվանվում է վիրուսի մուտք։ Որոշ վիրուսներ բջիջ են տեղափոխում նաև կրկնապատկման համար անհրաժեշտ սեփական սպիտակուցները։ Տարբեր վիրուսներ բջիջ թափանցելու համար օգտագործում են տարբեր մեխանիզմներ, օրինակ՝ պիկորնավիրուսները ՌՆԹ-ն բջիջ են ներմուծում պլազմատիկ թաղանթի միջոցով, օրթոմիքսովիրուսները բջիջ են թափանցում էդոցիտոզի միջոցով, ընկնում լիզոսոմների թթվային միջավայրի մեջ, դեպրոտեինացնում կապսիդը, որից հետո ազատված ՌՆԹ-ն անհրաժեշտ սպիտակուցների հետ հաղթահարում է լիզոսոմային թաղանթը՝ հայտնվելով ցիտոպլազմայում, իսկ որոշ դեպքերում նաև կորիզում։
Վիրուսի՝ կենդանական բջիջներ թափանցելը տարբերվում է բուսական և սնկային բջիջների թափանցումից, վերջիններիս մոտ ցելյուլոզե և խիտինե բջջապատի առկայության պատճառով[109]։ Այս վիրուսները բջիջ կարող են թափանցել միայն բջջապատի վնասման դեպքում։ Այնուամենայնիվ, համարյա բոլոր բույսերի վիրուսները (այդ թվում ծխախոտի խճանկարի վիրուսը) նույնպես կարող են բջջից տեղափոխվել բջիջ հատուկ անցուղիների՝ պլազմոդեսմների միջով, միաշղթա նուկլեոպրոտեինային կոմպլեքսների ձևով[110]։ Բակտերիաները բույսերի պես ունեն ամուր բջջապատ, որը վիրուսը բջիջ թափանցելու համար վնասվում է։ Բայց քանի որ բակտերիաների բջջապատն ավելի բարակ է քան բույսերինը, որոշ վիրուսներ ուղղակի ներմուծում են գենետիկական տեղեկատվությունը բջիջ, իսկ կապսիդը մնում է դրսում[111]։
Դեկապսիդացիա[խմբագրել | խմբագրել կոդը]
Դեկապսիդացիան կապսիդի անջատման և հեռացման գործընթացն է, որը տեղի է ունենում վիրուսի կամ տեր բջջի ֆերմենտների միջոցով։ Այս փուլի վերջում գենոմային նուկլեինաթթուն անջատվում է կապսիդից։
Կրկնապատկում[խմբագրել | խմբագրել կոդը]
Վիրուսների կրկնապատկումը (ռեպլիկացիան) առաջին հերթին վերաբերվում է գենոմի կրկնապատկումը։ Կրկնապատկումն ընդգրկում է վիրուսի մՌՆԹ-ի (մատրիցային կամ ինֆորմացիոն ՌՆԹ), վիրուսային սպիտակուցների սինթեզը, բարդ սպիտակուցների հավաքումը և վիրուսի գենոմի կրկնապատկումը, որը մեկնարկում է վաղ՝ կարգավորիչ գեների ակտիվացումից հետո։ Բարդ վիրուսների մոտ սրան կարող է հաջորդել մՌՆԹ-ի լրացուցիչ սինթեզի գործընթացներ։ Գեների ուշացած ակտիվացումը բերում է կառուցվածքային և վիրիոնային սպիտակուցների սինթեզին։
Հավաքում[խմբագրել | խմբագրել կոդը]
Կրկնապատկմանը հաջորդում են վիրուսի հավաքումը և որոշ սպիտակուցների ձևաբանական փոփոխությունները։ Օրինակ ՄԻԱՎ-ի մոտ, այս փոփոխությունը՝ այսպես կոչված «հասունացումը» ընթանում է վիրուսի բջջից դուրս գալուց հետո[112]։
Ելք[խմբագրել | խմբագրել կոդը]
Վիրուսները կարող են բջջից դուրս բերվել լիզիսից հետո։ Լիզիսը մի գործընթաց է, որի ժամանակ բջիջը մահանում է՝ բջջաթաղանթի և բջջապատի պատռվելու պատճառով։ Այսպես են դուրս գալիս բակտերիաների վիրուսների մեծամասնությունը և որոշ կենդանական վիրուսներ։ Վիրուսների մի մասն ունենում է լիզոգենիկ ցիկլ, որի դեպքում վիրուսի գենոմը տեղագրվում է տիրոջ բջջի քրոմոսոմի որոշակի հատվածներում։ Վիրուսային գենոմը այդ դեպքում անվանվում է «պրովիրուս» (նախավիրուս), իսկ բակտերիոֆագերի մոտ՝ «պրոֆագ»[113]։ Տեր բջջի բաժանման ժամանակ բաժանվում է նաև վիրուսային գենոմը, որը գտնվում է ոչ ակտիվ վիճակում։ Սակայն որոշ դեպքերում պրոֆագը կարող է սկիզբ տալ ակտիվ վիրուսին և տիրոջ բջիջը ենթարկել լիզիսի[114]։
Ակտիվ բազմացող վիրուսը միշտ չի սպանում տեր բջջին։ Թաղանթավոր վիրուսները, այդ թվում ՄԻԱՎ-ը, բջջից դուրս են գալիս բողբոջմամբ։ Բողբոջման ժամանակ վիրուսը թաղանթավորվում է տեր բջջի ձևափոխված բջջաթաղանթի կամ այլ ներքին մեմբրանի հաշվին[115]։ Այս դեպքում բջիջը մնում է կենդանի և շարունակում մասնակցել վիրուսի տարածմանը։
Վիրուսների տարբեր խմբերի կյանքի ցիկլի առանձնահատկություններ[խմբագրել | խմբագրել կոդը]
Վիրուսներում գենետիկական տեղեկատվության և կրկնապատկման տեսակը տարբերվում է տարբեր վիրուսների մոտ։
ԴՆԹ վիրուսներ[խմբագրել | խմբագրել կոդը]

Շատ ԴՆԹ վիրուսների ռեպլիկացիան տեղի է ունենում բջջի կորիզում։ Եթե բջջի վրա կան համապատասխան ռեցեպտորներ, այս վիրուսները բջիջ են մուտք գործում բջջաթաղանթի հետ միաձուլման միջոցով (օրինակ՝ հերպեսվիրուսները) կամ ռեցեպտոր միջնորդավորված էնդոցիտոզով։ ԴՆԹ վիրուսների մեծամասնության ռեպլիկացիան կախված է տեր բջջի ՌՆԹ-ի և ԴՆԹ-ի սինթեզի մեխանիզմներից. եթե էուկարիոտների մոտ վիրուսը ստիպված պետք է ճեղքի բջջի կորիզաթաղանթը, ապա բակտերիաների մոտ ընդամենն անհրաժեշտ է մուտք գործել բջիջ։ Մեծ գենոմներ ունեցող վիրուսները (օրինակ՝ պոքսվիրուսները) կարող են գաղտնագրել այս սպիտակուցների մեծ մասը։ Էուկարիոտների վիրուսի գենոմը պետք է հաղթահարի կորիզաթաղանթը՝ ԴՆԹ և ՌՆԹ սինթեզող ֆերմենտներին հասանելի դառնալու համար, պրոկարիոտների դեպքում այն ուղղակի պետք է թափանցի բջջի ներս[116]։
ՌՆԹ վիրուսներ[խմբագրել | խմբագրել կոդը]
Այս վիրուսների կրկնապատկումը հիմնականում տեղի է ունենում ցիտոպլազմայում։ ՌՆԹ վիրուսները, կախված ռեպլիկացիայի բնույթից, կարելի է բաժանել 4 տարբեր խմբերի։ ՌՆԹ-ի բևեռայնությունից և շղթաների քանակից կախված՝ ռեպլիկացիան ընթանում է տարբեր կերպ։ Բոլոր ՌՆԹ վիրուսները իրենց գենոմի կրկնապատկման համար օգտագործում են սեփական ՌՆԹ պոլիմերազները[117]։
Հակառակ տրանսկրիպտող վիրուսներ[խմբագրել | խմբագրել կոդը]
Այս վիրուսներն ունեն միաշղթա ՌՆԹ (ռետրովիրուսներ, մետավիրուսներ, պսևդովիրուսներ) և երկշղթա ԴՆԹ (կաուլիմովիրուսներ ու հեպադնավիրուսներ)։ ՌՆԹ գենոմներով հակառակ տրանսկրիպտող վիրուսները կրկնապատկման համար օգտագործում են ԴՆԹ միջնորդ, այն դեպքում, երբ ԴՆԹ գենոմներով վիրուսներն օգտագործում են ՌՆԹ միջնորդ[118]։ Երկու դեպքում էլ օգտագործվում է հակառակ տրանսկրիպտազ կամ ՌՆԹ-կախյալ-ԴՆԹ-պոլիմերազ ֆերմենտը։ Ռետրովիրուսները տիրոջ գենոմի մեջ են տեղագրում հակառակ տրանսկրիպցիայի ժամանակ առաջացած ԴՆԹ-ն, վիրուսի այս վիճակն անվանվում է պրովիրուս[119]։ Հակառակ տրանսկրիպտող վիրուսները զգայուն են հակավիրուսային դեղամիջոցների, այդ թվում՝ զիդովուդինի և լամիվուդինի նկատմամբ, որոնք ճնշում են հակառակ տրանսկրիպտազը։

Վարակված բջջի մոտ առաջացող կառուցվածքային և կենսաքիմիական փոփոխությունները շատ բազմազան են[120]։ Այս փոփոխություններն անվանվում են ցիտոպլազմային երևույթներ[121]։ Վիրուսային վարակների մեծ մասը բերում է տեր բջջի մահվան։ Մահվան պատճառ կարող է դառնալ բջջի լիզիսը, բջջաթաղանթի փոփոխությունը և ապոպտոզը[122]։ Բջջի մահվան պատճառ կարող է դառնալ նաև վիրուսային սպիտակուցների կողմից տիրոջ ճնշումը[123]։
Որոշ վիրուսներ չեն առաջացնում որևէ տեսանելի փոփոխություն։ Այդ բջիջներում վիրուսները գտնվում են քնած վիճակում և ակտիվ չեն, բջիջները չեն դրսևորում որևէ ախտանիշ, կենսագործունեությունը նորմալ է[124]։ Նիրհող վիրուսները կարող են առաջացնել քրոնիկական վարակներ, որի ախտանիշները կարող են չդրսևորվել ամիսներ և տարիներ։ Այսպես տեղի է ունենում օրինակ հերպեսի վիրուսի ժամանակ[125][126]։ Որոշ վիրուսներ, օրինակ Էպշտեյն-Բարրի վիրուսը կարող է առաջացնել բջիջների արագ բազմացում, առանց չարորակության դրսևորման[127], այն դեպքում, երբ պապիլոմավիրուսները ունակ են առաջացնելու չարորակ նորագոյացություններ[128]։
Տեր օրգանիզմների բազմազանություն[խմբագրել | խմբագրել կոդը]
Վիրուսները Երկրի վրա ամենաբազմազան կենսաբանական օբյեկտներ են և գերազանցում են մյուս բոլոր օրգանիզմներին միասին վերցրած[129]։ Վիրուսները վարակում են բոլոր բջջային օրգանիզմների ձևերին, այդ թվում՝ կենդանիներին, բույսերին, բակտերիաներին և սնկերին[95]։ Չնայած այս ամենին, վիրուսի յուրաքանչյուր տեսակ ընդունակ է վարակել միայն որոշակի տեր օրգանիզմներ։ Օրինակ բնական ծաղկի վիրուսը կարող է վարակել միայն մարդ բանական տեսակը[130]։ Այս դեպքում խոսում են տեր օրգանիզմների նեղ միջակայքի մասին։ Ի հեճուկս դրա, կատաղության վիրուս կարող է վարակել կաթնասունների շատ տեսակներ՝ ունի տեր օրգանիզմների լայն միջակայք[131]։ Բուսական վիրուսներն անվնաս են կենդանիների, իսկ կենդանիների վիրուսների մեծ մասը՝ մարդկանց համար[132]։ Որոշ բակտերիոֆագերի տերերի միջակայքը սահմանափակվում է բակտերիայի միայն մեկ շտամով, այս հատկությամբ նրանք կարող են կիրառվել շտամների նույնականացման համար[133]։
Դասակարգում[խմբագրել | խմբագրել կոդը]
Կենդանի բնության կարգաբանության մեջ վիրուսները առանձին տաքսոն են։ Նրանք Systema Naturae 2000 դասակարգման համակարգում Bacteria, Archaea և Eukaryota տաքսոնների հետ ներառվում են Biota սկզբնական տաքսոնի մեջ[134]։ 20-րդ դարում առաջարկություններ են եղել համապատասխան տաքսոն ստեղծել նաև ոչ բջջային կյանքի համար (Aphanobionta Novak, 1930[135]; վերնաթագավորություն Acytota Jeffrey, 1971[136]; Acellularia[137]), որը սակայն չի իրականացվել[138]։
Դասակարգման հիմնական դերը նմանությունների հիման վրա վիրուսների խմբավորումն ու անվանակարգումն է։ Վիրուսների դասակարգման առաջին փորձը կատարել են Անդրե Լվոֆը, Ռոբերտ Հորնը և Պոլ Տուրնիերը 1962 թվականին։ Դասակարգումը հիմնված էր Կառլ Լիննեյի կարգաբանության վրա[139]։ Դասակարգումն ընդգրկում էր տիպը, դասը, բաժինը, ընտանիքը, ցեղը և տեսակը։ Վիրուսները դասակարգվում էին իրենց ընդհանուր հատկությունների և գենոմը կազմող նուկլեինաթթվի տեսակի հիման վրա[140]։ Հետագայում ստեղծվեց «Վիրուսների կարգաբանության միջազգային հանձանաժողովը» (ICTV)։ Վիրուսները չեն դասակարգվում տիպերի և դասերի մեջ, իրենց փոքր չափերով գենոմի և մուտացիաների բարձր հաճախականության պատճառով։ Բալտիմորի դասակարգումը օգտագործվում է դասական կարգաբանության հետ՝ լրացնելով վերջինիս։
Վիրուսների դասակարգումը և կարգաբանությունը ներկայումս ապահովում և համալրում է Վիրուսների կարգաբանության միջազգային հանձանաժողովը (անգլ.՝ International Committee on Taxonomy of Viruses, ICTV)։ ICIV-ը ապահովում է նաև The Universal Virus Database ICTVdB տվյալների շտեմարանը։
ICTV դասակարգում[խմբագրել | խմբագրել կոդը]
Վիրուսների կարգաբանության միջազգային հանձնաժողովը մշակել է վիրուսների դասակարգման ժամանակակից համակարգը և համընդհանուր կարգաբանությունը։ ICIV-ին 7-րդ զեկույցում ամրագրել է, որ վիրուսների դասակարգման ամենաստորին տաքսոնը տեսակն է[141][նշում 2]։ Ներկայումս ուսումնասիրված է վիրուսների բազմազանության ընդամենը մի փոքր մասը, մարդու օրգանիզմի վիրուսների ուսումնասիրությունը ցույց է տվել, որ վիրուսային գենոմի հաջորդականությունների շուրջ 20%-ը նախկինում հետազոտված չէ։ Արտաքին միջավայրից, օրինակ՝ ծովային ջրից և օվկիանոսի հատակից վերցրած փորձանմուշների ուսումնասիրությունը ցույց է տվել, որ վիրուսային գենոմի հաջորդականությունների մեծամասնությունը ամբողջությամբ նոր են[142]։
Կարգաբանական հիմնական միավորներն են[143]՝
- Կարգ (-virales)
- Ընտանիք (-viridae)
- Ենթաընտանիք (-virinae)
- Ընտանիք (-viridae)
ICTV-ի 2011 թվականին ընդունված կարգաբանության համաձայն՝ գոյություն ունեն վիրուսների 6 հիմնական կարգեր՝
- Կաուդովիրուսներ, (Caudovirales), (3 ընտանիք),
- Հերպեսվիրուսներ, (Herpesvirales), (3 ընտանիք),
- Մոնոնեգավիրուսներ, (Mononegavirales), (4 ընտանիք),
- Նիդովիրուսներ, (Nidovirales), (4 ընտանիք),
- Պիկորնավիրուսներ, (Picornavirales), (5 ընտանիք),
- Թիմովիրուսներ, (Tymovirales), (4 ընտանիք),
Առաջարկվել է նաև ավելացնել 7-րդ՝ լիգամենվիրուսներ (Ligamenvirales) կարգը։ Այսպիսով, ICIV-ի ժամանակակից դասակարգումը (2012) ներառում է վիրուսների 7 կարգ՝ Caudovirales, Herpesvirales, Ligamenvirales, Mononegavirales, Nidovirales, Picornavirales և Tymovirales[144]։ 8-րդ կարգի գոյությունը դեռևս ենթադրվում է (Megavirales[145])։ Դասակարգումը չի առանձնացնում ենթատեսակները, շտամները և իզոլյատները։
Ընդհանուր հաշվում են վիրուսների 6 կարգ, 87 ընտանիք, 19 ենթաընտանիք, 349 ցեղ և շուրջ 2284 տեսակ. շուրջ 3000 տեսակ էլ դեռևս դասակարգված չեն[146][147][148]։
Բալտիմորի դասակարգում[խմբագրել | խմբագրել կոդը]

Նոբելյան մրցանակի դափնեկիր, կենսաբան Դավիթ Բալտիմորը ստեղծել է վիրուսների դասակարգման սեփական մոդելը[149]։ ICTV դասակարգման համակարգը ժամանակակից վիրուսաբանության մեջ օգտագործվում է բալտիմորյան կարգաբանության հետ զուգահեռ[150][151][152]։ Բալտիմորի դասակարգումը հիմնված է վիրուսների իՌՆԹ-ի (ինֆորմացիոն կամ մատրիցային ՌՆԹ) ձևավորման մեխանիզմների վրա։ Բոլոր վիրուսները իՌՆԹ-ները սինթեզում են սպիտակուցների սինթեզի և ռեպլիկացիայի համար, բայց իՌՆԹ-ի սինթեզը տարբեր վիրուսների մոտ ընթանում է տարբեր կերպ։ Վիրուսային գենոմը կարող է լինել կամ միաշղթա (անգլ.՝ single-stranded (ss)) կամ երկշղթա (անգլ.՝ double-stranded (ds)), պարունակել ՌՆԹ կամ ԴՆԹ և որոշ դեպքերում օգտագործել հակառակ տրանսկրիպտազ (անգլ.՝ everse transcriptase (RT))։ Ավելին, միաշղթա ՌՆԹ վիրուսները կարող են լինել կամ դրական (+), կամ բացասական (-)։
Բալտիմորի դասակարգմամբ վիրուսները բաժանվում են 7 խմբերի[153][154]՝
- I։ Երկշղթա ԴՆԹ վիրուսներ (dsDNA) (օրինակ՝ ադենովիրուսներ, հերպեսվիրուսներ, պոքսվիրուսներ)
- II։ Միաշղթա (+) ԴՆԹ վիրուսներ (+ssDNA) (օրինակ՝ պարվովիրուսներ)
- III։ Երկշղթա ՌՆԹ վիրուսներ (dsRNA) (օրինակ՝ ռեովիրուսներ)
- IV։ Միաշղթա (+) ՌՆԹ վիրուսներ (+ssRNA) (օրինակ՝ պիկորնավիրուսներ, տոգավիրուսներ)
- V։ Միաշղթա (-) ՌՆԹ վիրուսներ (-ssRNA) (օրինակ՝ օրթոմիքսովիրուսներ, ռաբդովիրուսներ)
- VI։ Միաշղթա հակառակ տրանսկրիպտող (-) ՌՆԹ վիրուսներ (ssRNA-RT) (օրինակ՝ ռետրովիրուսներ)
- VII։ Երկշղթա հակառակ տրանսկրիպտող ԴՆԹ վիրուսներ (dsDNA-RT) (օրինակ՝ հեպադնավիրուսներ)[155]։
Վիրուսների հետագա բաժանումը կատարվում է գենոմի կառուցվածքային առանձնահատկությունների, այլ վիրուսների հետ նմանության, լիպիդային պատիճի առկայության, տիրոջ կարգաբանական տեղի հիման վրա և այլ հատկանիշների հիման վրա։
Մարդու վիրուսային հիվանդություններ[խմբագրել | խմբագրել կոդը]

Մարդու տարածված վիրուսային հիվանդություններն են՝ գրիպը, ջրծաղիկը, հերպեսը և այլն։ Շատ հիվանդություններ՝ էբոլան, ՁԻԱՀ-ը, թռչնագրիպը, սուր շնչառական ախտանիշը պայմանավորվում են վիրուսներով։ Վիրուսների՝ հիվանդություն առաջացնելու ընդունակությունը բնութագրվում է նրանց վիրուլենտությամբ։ Որոշ հիվանդությունների պատճառը միայն ենթադրվում է, որ վիրուսային է, օրինակ՝ հավանական կապ կա 6-րդ տիպի հերպեսվիրուսի և այնպիսի նյարդաբանական հիվանդությունների մեջ, ինչպիսիք են՝ ցրված սկլերոզը և քրոնիկական հոգնածության ախտանիշը[156]։ Վեճեր են ընթանում այն բանի շուրջ, որ ձիերի նյարդաբանական հիվանդություններ առաջացնող բարնովիրուսը մարդու մոտ կարող է առաջացնել հոգեկան հիվանդություններ[157]։
Օրգանիզմում հիվանդություն առաջացնելիս՝ վիրուսներն օգտագործում են տարբեր մեխանիզմներ, որը կախված է վիրուսի տեսակից։ Բջջային մակարդակով այդ մեխանիզմները ներառում են լիզիսը, ապա բջջի մահը՝ նեկրոզը։ Բազմաբջիջ օրգանիզմներում մեծ քանակով բջիջների մահից հետո տեղի է ունենում ամբողջ օրգանիզմի մահը։ Ոչ բոլոր վիրուսներն են առաջ բերում հոմեոստազի հավասարակշռության խախտում և հիվանդություն, որոշները օրգանիզմում կարող են գոյություն ունենալ առանց տեսանելի վնասների։ Այսպիսի վիրուսի օրինակ է առաջին տիպի պարզ հերպեսի վիրուսը։ Այս երևույթն անվանում են լատենտություն[158]։ Լատենտ են նաև ինֆեկցիոն մոնոնուկլեոզ առաջացնող Էպշտայն Բարի, ջրծաղիկի, գոտեորքի վիրուսը։ Մարդկանց մեծամասնությունը իրենց կյանքի ընթացքում վարակվել են այս վիրուսներից առնվազն մեկով[159]։ Լատենտ վիրուսները հաճախ կարող են նաև օգտակար լինել, վիրուսների առկայությունն օրինակ, կարող է ձևավորել հակաբակտերիալ իմունիտետ[160]։
Որոշ վիրուսներ կարող են առաջացնել քրոնիկական կամ ամբողջ կյանքում պահպանվող վարակ, որի դեպքում վիրուսները կրկնապատկվում են օրգանիզմում՝ չենթարկվելով տիրոջ իմունային պաշտպանության մեխանիզմներին[161]։ Սա հատուկ է օրինակ հեպատիտ B և հեպատիտ C-ի վիրուսներին։ Քրոնիկական հիվանդները կոչվում են կրողներ[162]։ Եթե պոպուլյացիայում մեծ է կրողների խտությունը, հիվանդությունը դառնում է համաճարակային բնույթի[163]։
Վարակաբանություն[խմբագրել | խմբագրել կոդը]
Վիրուսային վարակաբանությունը բժշկագիտության բաժին է, որն ուսումնասիրում է մարդկանց վիրուսային հիվանդությունների փոխանցումը և կարգավորումը։ Վիրուսի փոխանցումը կարող է տեղի ունենալ ուղղահայաց՝ մորից երեխային և հորիզոնական՝ մարդուց մարդուն։ Ուղղահայաց փոխանցման օրինակ է ՁԻԱՀ-ի և հեպատիտ B-ի փոխանցումը, որի ժամանակ երեխան արդեն վարակված է ծնվում[164]։ Ավելի հազվադեպ հանդիպող օրինակներից է ջրծաղիկի և գոտեորքի վիրուսները, որոնք մեծահասակների համար անվնաս են, բայց կարող են մահացու լինել սաղմի և նորածնի համար[165]։
Պոպուլյացիայում վիրուսի տարածման ամենահանդիպող մեխանիզմը հորիզոնական փոխանցումն է։ Փոխանցումը կարող է տեղի ունենալ՝ սեռական հեղուկների (ՄԻԱՎ), արյան, այդ թվում օգտագործված ներարկիչների (հեպատիտ C), թքի (Էպշտայն Բարրի վիրուս) միջոցով, վարակված ջրի, սննդի կլանման (նորովիրուս), վիրիոններով օդի ներշնչման (գրիպի վիրուս), տիրոջ մաշկը վնասող միջատների (մոծակներ, Դենգե տենդ) միջոցով։ Վարակի փոխանցման արագությունը կախված է պոպուլյացիայի խտությունից, վիրուսի հանդեպ ձևավորված իմունիտետ չունեցող զգայունակ մարդկանց քանակից[166],առողջապահակն վիճակից և եղանակային պայմաններից[167]։
Վարակաբանությունը կիրառվում է վարակի տարածումը կանխելու համար[168]։ Կախված վիրուսի բնույթից ձեռնարկվում են տարբեր կանխարգելիչ միջոցառումներ։ Սկզբում որոշվում է բռնկման պատճառը և նույնականացվում հարուցիչը։ Վիրուսի նույնականացումից հետո վարակը հնարավոր է կանխարգելել պատվաստումների միջոցով։ Եթե պատվաստումներն անհասանելի են, ապա կիրառվում է սանացիա և վարակազերծում։ Շատ հաճախ վարակված մարդկանց մեկուսացնում են հասարակությունից. հայտարարվում է կարանտին[169]։ 2001 թվականի դաբաղի բռնկումը կանխելու պատճառով սպանդի ենթարկվեցին հազարավոր կովեր։ 2007 և 2010 թվականներին Հայաստանում խոզերի աֆրիկյան ժանտախտի բռնկումների հետևանքով սպանդի ենթարկվեցին հազարավոր ընտանի խոզեր[170]։ Կենդանիների և մարդու հիվանդությունների մեծ մասն ունի ինկուբացիոն շրջան, որի ժամանակ վարակի ոչ մի ախտանիշ չի դրսևորվում[171]։ Վիրուսային հիվանդությունների ինկուբացիոն շրջանը կարող է տևել մի քանի օրից մի քանի շաբաթ[172]։ Ինկուբացիոն շրջանին սովորաբար հաջորդում է վարակի փոխանցման շրջանը, երբ վարակված մարդը կամ կենդանին կարող է վարակել այլ մարդկանց և կենդանիներին[172]։ Այս երկու շրջանների տևողության իմացությունը կարևոր է բռնկումների և համաճարակների կառավարման համար[173]։ Եթե բռնկումը բերում է մեծ քանակով կենդանիների և մարդկանց վարակմանը, ապա այն անվանում են համաճարակ («էպիդեմիա»), իսկ եթե բռնկումը տարածվում է ամբողջ տարածաշրջանով, աշխարհամասով կամ ամբողջ աշխարհով՝ համավարակ[174]։
Համաճարակներ և համավարակներ[խմբագրել | խմբագրել կոդը]
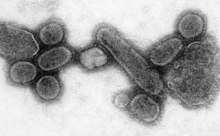
Ամերիկայի բնիկների թվաքանակը շեշտակի նվազել է վարակիչ հիվանդությունների՝ հատկապես ծաղիկի պատճառով, որը Ամերիկա էր բերվել եվրոպացի գաղութարարների կողմից։ Ըստ որոշ գնահատականների, Կոլումբոսի Ամերիկա գալուց հետո, աշխարհամաս բերված հիվանդություններից սպանվել է արմատական բնակչության շուրջ 70%-ը։ Հիվանդությունների պատճառած վնասը օգնել է եվրոպացիներին նվաճել և հպատակեցնել նրանց[175][176][177][178][179][180][181]։
Համավարակը տարերային կամ համաշխարհային մասշտաբներ ընդգրկող համաճարակն է։ 1918-1919 թվականներին շարունակվող Իսպանական գրիպի համաճարակը գրիպի վիրուսի 5-րդ կարգի համավարակ է։ Համավարակի պատճառը ագրեսիվ և բարձր մահացություն ունեցող A գրիպի վիրուսն էր։ Ի տարբերություն գրիպի մյուս բռնկումների, որոնց ժամանակ հիվանդանում էին անչափահասները, ծերերն ու երեխաները, իսպանական գրիպով հիվանդանում էին հասուն ուժեղ իմունիտետով մարդիկ[182]։ Հին գնահատականներով, իսպանական գրիպի ժամանակ մահացավ 40-50 մլն[183], իսկ ժամանակակից տվյալների համաձայն՝ շուրջ 100 միլիոն մարդ, որը կազմում էր այդ ժամանակվա Երկրի բնակչության 5%-ը[184]։
Հետազոտողների մեծամասնությունը կարծում է, որ ՁԻԱՀ-ն առաջացել է Աֆրիկայի հարավում 20-րդ դարում[185]։ Այսօր ՁԻԱՀ-ի համաճարակն ունի համավարակի մասշտաբ[186]։ Առողջության համաշխարհային կազմակերպության և ՄԱԿ-ի ՄԻԱՎ/ՁԻԱՀ-ի միացյալ ծրագրի գնահատականներով 1981 թվականի հունիսի 5-ին գրանցված առաջին դեպքից հետո ՁԻԱՀ-ից մահացել է ավելի քան 25 միլիոն մարդ[187]։ 2007 թվականին գրանցվել է ՁԻԱՀ-ով վարակման 2,7 միլիոն դեպք և շուրջ 2 միլիոն ՁԻԱՀ-ի հետ կապված մահ[188]։
Ֆլավովիրուսների ընտանիքին են պատկանում որոշ մահացու վիրուսային հիվանդությունների հարուցիչներ։ Ֆլավովիրուսները թելանման վիրուսներ են, առաջացնում են հեմոռագիկ տենդ։ Այս վիրուսներին է պատկանում Էբոլա հեմոռագիկ տենդի հարուցիչը և մարբուրգյան վիրուսը։ Մարբուրգյան վիրուսը մամուլի ուշադրության կենտրոնում է հայտնվել 2005 թվականի ապրիլին Անգոլայում ունեցած բռնկման պատճառով։ Այս բռնկումը տևել է 2004-ի հոկտեմբերից մինչև 2005 թվականի սկիզբը և բնորոշվել է որպես երբևէ տեղի ունեցած ամենադաժան հեմոռագիկ տենդի համաճարակ[189]։
Քաղցկեղ[խմբագրել | խմբագրել կոդը]

Վիրուսները կարող են առաջացնել մարդու և այլ տեսակների չարորակ ուռուցքներ, որը սակայն հանդիպում է վարակվածներից քչերի մոտ։ Քաղցկեղային վիրուսները պատկանում են տարբեր ընտանիքներին, ներառում են ՌՆԹ- և ԴՆԹ-վիրուսները. օնկովիրուսների (հնացած տերմին) մեկ ընդհանուր տեսակ գոյություն չունի։ Քաղցկեղի զարգացումը որոշվում է մի շարք գործոններով, որոնցից են տիրոջ իմունային համարգի առանձնահատկությունները[190] և տիրոջ մոտ մուտացիաների առկայությունը[191]։ Մարդու մոտ քաղցկեղ առաջացնող վիրուսներից են մարդու պապիլոմավիրուսի որոշ ներկայացուցիչներ, հեպատիտ B-ի և C-ի, Էպշտայն Բարրի վիրուսները, հերպեսվիրուսը (Մերկելի բջիջների պոլիոմավիրուս)[192]։ Հեպատիտի վիրուսները կարող են առաջացնել քրոնիկական վիրուսային վարակ, որը հանգեցնում է լյարդի քաղցկեղի[193][194]։ Մարդու T-լիմֆոտրոֆ վիրուսով վարակումը կարող է առաջացնել արևադարձային սպաստիպ պարապերեզ և T-լեյկոցիտների լեյկեմիա[195]։ Պապիլոմավիրուսները կարող են առաջացնել արգանդի վզիկի, մաշկի, հետանցքի և առնանդամի քացղկեղ[196]։ Կապոշի սարկոմայի հերպեսվիրուսը առաջացնում է Կապոշի սարկոմա և մարմնի խոռոչի լիմֆոմա, Էպշտայն Բարրի վիրուսը՝ Բերկիտի լիմֆոմա, լիմֆոգրանուլեմատոզ, B-լիմֆոպրոլիֆերացիայի խախտում և քթկոկորդային կարցինոմա[197]։ Մերկելի բջիջների պոլիովիրուսը նման է ավելի քան 50 տարի վիրուսային քաղցկեղի համար մոդելային վիրուսներ օգտագործվող SV40 վիրուսին և մկների պոլիովիրուսներին[198]։
Տիրոջ պաշտպանական մեխանիզմները[խմբագրել | խմբագրել կոդը]
Օրգանիզմի հակավիրուսային պաշտպանության առաջին օղակը բնածին իմունիտետն է։ Այն ներառում է ոչ յուրահատուկ պաշտպանությունն ապահովող բջիջներ և այլ մեխանիզմներ։ Բնածին իմունիտետի բջիջները ճանաչում և ազդում են հարուցչի վրա միանման ձևով անկախ հարուցչի տեսակից։ Ի տարբերություն ձեռքբերովի իմունիտետի, բնածինը չի ապահովում հիվանդության դեմ շարունակական և ապահով պաշտպանություն[199]։
Էուկարիոտների մոտ վիրուսներից բնածին պաշտպանության կարևոր ձևերից է ՌՆԹ ինտերֆերենցիան[200]։ Շատ վիրուսների կրկնապատկման միջանկյալ փուլերից է երկշղթա ՌՆԹ-ի փուլը։ Այսպիսի վիրուսների դեմ պայքարի համար, բջիջն ունի միա- և երկշղթա ՌՆԹ-ն քայքայելու ոչ յուրահատուկ ընդունակություն։ Երբ վիրուսը թափանցում է բջջի ներս և ազատում գենոմային ՌՆԹ-ն, միանում է տիրոջ Dicer սպիտակուցային համալիրը և կտրտում վիրուսային ՌՆԹ-ն մանր հատվածների։ Ակտիվանում է RISC անվանվող ուղին, որը քայքայում է վիրուսային ՌՆԹ-ն՝ արգելակելով վիրուսի հետագա բազմացումը։ Ռոտավիրուսը կարողանում է խուսափել ՌՆԹ ինտերֆերենցիայից, քանի որ այն ցիտոպլազմայում պահպանում է կապսիդը, իսկ նոր ձևավորված ՌՆԹ-ն դուրս է գալիս կապսիդի հատուկ անցուղիներից[201][202]։
Վիրուսին հանդիպելու դեպքում ողնաշարավորների ձեռքբերովի իմունիտետի համակարգը սկսում է ձևավորել յուրահատուկ հակամարմիններ, որոնք միանում են վիրուսին՝ հաճախ դարձնելով նրան անվտանգ։ Այս գործընթացն անվանվում է հումորալ իմունիտետ։ Գոյություն ունի հակամարմինների երկու կարևոր տեսակ՝ IgM) (իմունոգլոբուլին էմ), որը բարձր արդյունավետությամբ ոչնչացնում է վիրուսին, սակայն արտադրվում է միայն մի քանի շաբաթվա ընթացքում։ Երկրորդը՝ ImG արտադրվում է ավելի երկար։ Տիրոջ արյան մեջ IgM-ի առկայությունը խոսում է օրգանիզմում վարակի առկայության, իսկ IgG-ի առկայությունը՝ անցյալում ունեցած վարակի մասին[203]։ Իմունիտետի թեսթավորման համար չափվում է հենց IgG-ի քանակը[204]։ Հակամարմինները կարող են արդյունավետ լինել նույնիսկ այն ժամանակ, երբ վիրուսն արդեն թափանցել է բջջի ներս։ TRIM21 բջջային սպիտակուցը կարող է հակամարմինները միացնել վիրուսի մասնիկների մակերեսին։ Սրան հաջորդում է վիրուսի քայքայումը պրոտեոսոմային համակարգի միջոցով[205]։
Ողնաշարավորների ձեռքբերովի իմունիտետի մյուս համակարգն անվանվում է բջջային իմունիտետ և ընդգրկում է իմունային բջիջներ հանդիսացող T-լիմֆոցիտները։ Օրգանիզմի բջիջները իրենց մակերեսին միշտ կրում են սեփական սպիտակուցների կարճ հատվածներ. եթե այս սպիտակուցների շարքում T-լիմֆոցիտը ճանաչում է կասկածելի վիրուսային ծագում ունեցող սպիտակուց, ապա սկսվում է T-քիլլերների միջոցով այդ բջջի քայքայումը։ Սրան հաջորդում է վիրուսային սպիտակուցի հիման վրա յուրահատուկ T-լիմֆոցիտների արտադրությունը։ Այլ բջիջներ, օրինակ՝ մակրոֆագերը մասնագիտացած են հակածնի ներկայացման մեջ[206]։ Օրգանիզմի կարևոր պաշտպանական մեխանիզմներից է նաև ինտերֆերոնի սինթեզը։ Ինտերֆերոնը հորմոն է, որն արտադրվում է ի պատասխան օրգանիզմում վիրուսի առկայության։ Ինտերֆերոնը համալիր ձևով ազդում է վարակված բջջի և հարևան բջիջների վրա, սպանում դրանց՝ սրանով կանխարգելելով վիրուսի տարածումը[207]։
Իմունային պատասխան առաջանում է ոչ բոլոր բջիջների դեմ։ ՄԻԱՎ-ը կարողանում է շրջանցել իմունային պատասխանը, քանի որ անընդհատ փոխում է վիրիոնի մակերեսի սպիտակուցների ամինաթթվային կազմը։ Այսպիսի դիմացկուն վիրուսները, հեռանում են իմունային համակարգից, մեկուսանում իմունային բջիջներից, արգելակում հակամարմինների ներկայացումը, ցիտոկինների հանդեպ ունեցած դիմացկունության շնորհիվ խուսափում են բնական քիլլերներից, արգելակում բջիջների ապոպտոզը[208]։ Նեյրոտրոպ վիրուսները խուսափում են իմունային պատասխանից տարածվում նյարդային բջիջներում, որտեղ հասանելի չեն իմունային բջիջների համար։
Կանխարգելում և բուժում[խմբագրել | խմբագրել կոդը]
Վիրուսի ոչնչացումը հիմնականում զուգորդվում է տեր բջջի վրա բացասական ազդեցություն ունենալով։ Բանն այն է, որ կրկնապատկվելու համար վիրուսն օգտագործում է տեր բջջի նյութափոխանակության մեխանիզմները։ Վիրուսային հիվանդությունների կանխարգելման ամենաարդյունավետ մոտեցումը պատվաստումն է, որը հիվանդության հանդեպ ձևավորում է իմունիտետ և հակավիրուսային դեղամիջոցների օգտագործումը, որոնց օգտագործումը ընտրողաբար ազդում է վիրուսի կրկնապատկման վրա։
Պատվաստումներ[խմբագրել | խմբագրել կոդը]

Պատվաստումը վիրուսային վարակների կանխարգելման էժան և արդյունավետ եղանակ է։ Պատվաստումները վիրուսային հիվանդությունների կանխարգելման համար օգտագործվել են վիրուսների հայտնաբերումից շատ ավելի վաղ։ Պատվաստումների միջոցով բուժվել են շատ մահացու հիվանդություններ, ինչպիսիք են՝ պոլիոմելիտը, կարմրուկը, խոզուկը և կամրախտը[209]։ Բնական ծաղիկի վարակն այժմ ամբողջությամբ վերացված է[210]։ Պատվաստումների միջոցով կանխարգելվում են մարդու շուրջ տասներեք[211] և շատ այլ կենդանական վիրուսային հիվանդություններ[212]։ Պատվաստումը կարող է կազմված լինել կենդանի-ապաակտիվացված կամ մահացած վիրուսային սպիտակուցներից (հակածիններից)[213]։ Ակտիվ պատվաստումները պարունակում են վիրուսի թուլացված ձևը։ Այն հիվանդություն չի հանգեցնում, սակայն առաջացնում է իմունիտետ։
Այս պատվաստանյութերը կարող են վտանգավոր լինել թուլացած իմունիտետով մարդկանց համար, քանի որ հավանական է հիվանդության զարգացումը[214]։ Կենսատեխնոլոգիայի և գենետիկական ճարտարագիտության մեթոդները օգտագործվել են ենթամիավորների պատվաստանյութերի արտադրման համար։ Այս պատվաստանյութերը ներառում են միայն վիրուսի կապսիդի սպիտակուցները։ Այս տեսակին է պատկանում, օրինակ հեպատիտ B-ի պատվաստանյութը[215]։ Ենթամիավորների պատվաստանյութերը ապահով են ճնշված իմունիտետով հիվանդների համար, քանի որ չեն կարող առաջացնել հիվանդություն[216]։ Դեղին տենդի վիրուսի պատվաստանյութը, որը անվանվել է «17D», ամենայն հավանականությամբ, երբևէ ստեղծված ամենաապահով և արդյունավետ պատվաստանյութն է[217]։
Հակավիրուսային դեղամիջոցներ[խմբագրել | խմբագրել կոդը]


Հակավիրուսային դեղամիջոցները հաճախ նուկլեոզիդին նման նյութեր են, որոնք կրկնապատկման ընթացքում վիրուսները սխալմամբ ընդգրկում են իրենց գենոմում։ Ընդգրկելուց հետո վիրուսի կյանքի ցիկլը կանգ է առնում, քանի որ նոր սինթեզվող վիրուսային ԴՆԹ-ները ոչ ակտիվ են հիդրօքսիլ խմբերի անբավարարության հետևանքով։ Ֆոսֆորի ատոմներին միանալով հիդրօքսիլ խմբերն առաջացնում են ԴՆԹ-ի մոլեկուլի ամուր կմախքը։ Այս պրոցեսը կոչվում է շղթայի տերմինացիա[218]։ Նուկլեոզիդին նման նյութերից է ացիկլովիրը՝ հերպեսի վիրուսի և լամիվուդինը՝ ՄԻԱՎ-ի և հեպատիտ B-ի վիրուսի համար։ Ացիկլովիրը ամենահին և ամենից հաճախ նշանակվող հակավիրուսային դեղամիջոցն է[219]։
Կիրառվող մյուս հակավիրուսային դեղամիջոցները ազդում են վիրուսի կյանքի ցիկլի այլ փուլերի վրա։ ՄԻԱՎ-ի կենսագործունեության համար անհրաժեշտ է ՄԻԱՎ-1 պրոտեազը, որը պրոտեոլիտիկ ֆերմենտ է։ Գոյություն ունեն հատուկ դասի դեղամիջոցներ՝ պրոտեազ ինհիբիտորներ, որոնք ապաակտիվացնում են այս ֆերմենտը։
Հեպատիտ C-ի հարուցիչը ՌՆԹ վիրուս է։ Այս հիվանդությամբ վարակված մարդկանց 80%-ի մոտ հիվանդությունը քրոնիկական է, չբուժվելու դեպքում այն մնում է ամբողջ կյանքի ընթացքում։ Այն այժմ բուժվում է հակավիրուսային դեղամիջոց ռիբավիրինի և ինտերֆերոնի համակցմամբ[220]։ Նմանապես քրոնիկական հեպատիտ B-ի անախտանիշ ձևի բուժման համար մշակվել է լամիվուդինով բուժման եղանակ[221]։
Այլ տեսակների վիրուսներ[խմբագրել | խմբագրել կոդը]
Վիրուսները վարակում են բոլոր բջջային օրգանիզմները։ Այդքանով հանդերձ, յուրաքանչյուր օրգանիզմ ունի յուրահատուկ հարուցիչներ[222]։ Կան վիրուսներ, այսպես կոչված «արբանյակները» (անգլ.՝ satellite), որոնք կրկնապատկվում են միայն այլ վիրուսներով վարակված բջիջներում[59]։
Նախակենդանիների վիրուսներ[խմբագրել | խմբագրել կոդը]
Նախակենդանիների վիրուսներին են պատկանում կենդանիների, բույսերի և սնկերի թագավորություններին չպատկանող միաբջիջ էուկարիոտների վիրուսները[223]։
Նախակենդանիների շատ վիրուսներ ունեն անսովոր մեծ չափսեր։ Օրինակ՝ ամեոբաներից առաջին անգամ առանձնացված Marseillevirus-ի գենոմը ունի 368 կբ մեծություն, իսկ Acanthamoeba նախակենդանուն վարակող Mamavirus-ը չափերով գերազանցում է նույնիսկ միմիվիրուսին (կապսիդն ունի շուրջ 500 նմ տրամագիծ)։ Հսկա վիրուսների թվին է պատկանում նաև լայնորեն տարածված ծովային նախակենդանի Cafeteria roenbergensis-ին վարակող վիրուսը (անգլ.՝ Cafeteria roenbergensis virus, CroV)[224].
Կենդանական վիրուսներ[խմբագրել | խմբագրել կոդը]
Վիրուսները բազմաթիվ խոշոր եղջերավոր անասունների հիվանդությունների հարուցիչներ են. դաբաղը, խոզերի աֆրիկական ժանտախտը և այլ հիվանդություններ պայմանավորված են վիրուսներով[225]։ Չվակցինացված կատուները, շները և ձիերը զգայունակ են տարբեր վիրուսային հիվանդությունների նկատմամբ։ Շների պարվովիրուսը պայմանավորված է փոքր ԴՆԹ վիրուսով և շան ձագերի համար հաճախ մահացու է[226]։ Ինչպես բոլոր անողնաշարավորները, մեղրատու մեղուն նույնպես զգայունակ է շատ վիրուսային հիվանդությունների նկատմամբ[227]։ Սակայն շատ վիրուսներ չեն վնասում տիրոջ օրգանիզմը, չեն առաջացնում հիվանդություններ և ախտանիշներ[2]։
Անողնաշարավորների վիրուսներ[խմբագրել | խմբագրել կոդը]
Անողնաշարավորները կազմում են բոլոր հայտնի կենդանատեսակների շուրջ 80%-ը և նույնպես վարակվում են բազմաթիվ վիրուսներով։ Առավել ուսումնասիրված են միջատների վիրուսները, որոնց մասին տեղեկությունները սակայն նույնպես լիարժեք չեն։ Վերջին ժամանակներում բնութագրված են նաև այլ անողնաշարավորների վիրուսային հիվանդություններ։ Այս վիրուսները մնում են քիչ ուսումնասիրված, քանի դեռ հիվանդությունների վիրուսային բնույթը վերջնականապես չի ուսումնասիրվել և մեկուսացված վիրուսը չի փորձարկվել նույն տեսակի այլ առանձնյակների վրա[228]։
Ներկայումս հայտնի է հոդվածոտանիներին՝ հիմնականում միջատներին վարակող վիրուսների առանձին ընտանիք՝ իրիդովիրուսները (լատին․՝ Iridoviridae անգլ.՝ Invertebrate iridescent viruses-ից՝ «հոդվածոտանիների ծիածանային վիրուսներ», այսպիսի գույն են ստանում վարակված առանձնյակները), որոնք գոյություն ունեն ջրային և խոնավ միջավայրերում։ Իրիդովիրուսները իկոսաեդրային մասնիկներ են 120-180 նմ տրամագծով, պարունակում են ներքին լիպիդային թաղանթ և երկշղթա ԴՆԹ-ից բաղկացած գենոմ՝ 130-210 հազար նուկլեոտիդներից կազմված[229]։
Միջատներին վարակող այլ վիրուսներից են՝ Baculoviridae ընտանիքը, Poxviridae ընտանիքի Entomopoxvirinae ենթաընտանիքը, Parvoviridae ընտանիքի Densovirus ենթաընտանիքը, Rhabdoviridae ընտանիքի որոշ վիրուսներ, Reoviridae, Picornaviridae ընտանիքները[230]։
Սնկերի վիրուսներ[խմբագրել | խմբագրել կոդը]
Սնկերի վիրուսները հայտնի են միկովիրուսներ անվամբ։ Ներկայումս առանձնացված է հիսուներեք ցեղի պատկանող շուրջ 73 տեսակի սնկերի վիրուսներ, որոնք մտնում են 5 դասերի մեջ[231]։ Ենթադրաբար, սնկերի մոտ կան նաև մեծաքանակ անվտանգ վիրուսներ։ Այս վիրուսները 30-45 նմ տրամագիծ ունեցող շրջանաձև մասնիկներ են։ Վիրուսների կապսիդի միակ սպիտակուցը դասավորված է վիրուսային գենոմի՝ երկշղթա ՌՆԹ-ի շուրջը։ Որպես կանոն, միկովիրուսներն անվնաս են։
Որոշ սնկային շտամներ կարող են վարակվել բազմաթիվ վիրուսներով, բայց միկովիրուսների մեծամասնությունը սովորաբար ունի միայն մեկ տեր։ Սնկերի վիրուսների դասակարգմամբ այժմ զբաղվում է Վիրուսների կարգաբանության միջազգային հանձնաժողովի հատուկ հանձնաժողովը[231]։ Ներկայումս վերոնշյալ հանձնաժողովը առանձնացնում է միկովիրուսների 3 ընտանիք, ամենալավ ուսումնասիրված վիրուսները պատկանում են Totiviridae[232] ընտանիքին։
Պենիցիլինային սնկերի հակավիրուսային ակտիվությունը պայմանավորած է միկովիրուսի երկշղթա ՌՆԹ-ի վրա ինտերֆերոնի արգելակող ազդեցությամբ[231]։
Երբ վիրուսը սունկ թափանցելուց հետո դրսևորում է վիրուլենտություն, սնկի պատասխան ռեակցիան կարող է լինել՝ ախտածին տեսակների մոտ վիրուլենտության բարձրացում կամ նվազում, միցելի և պտղամարմնի դեգեներացիա, գույնի փոփոխություն, սպորակրության փոփոխություններ և այլն։ Ոչ կապսիդային վիրուսների ՌՆԹ փոխանցվում է անաստամոզների միջոցով՝ միտոքոնդրիումներից անկախ։
Վիրուսային հիվանդությունները կարող են վնաս հասցնել սնկաբուծությամբ զբաղվող կազմակերպություններին, առաջացնել օրինակ՝ շամպինիոնի պտղամարմնի գորշացում, ձմեռային կոճկասնկի գունավորման փոփոխություն, որը նվազեցնում է վերջիններիս սպառողական արժեքը։ Հիպովիրուլենտություն առաջացնող ախտածին սնկերը կարող են կիրառվել բույսերի հիվանդությունների դեմ պայքարում[233][234]։
Բուսական վիրուսներ[խմբագրել | խմբագրել կոդը]

Գոյություն ունեն բույսերի բազմաթիվ վիրուսներ, որոնք հաճախ առաջացնում են բերքի կորուստ, և այդպիսի վիրուսներին կառավարելը տնտեսապես ձեռնտու չէ։ Բուսական վիրուսները բույսից բույս են տարածվում այլ օրգանիզմների միջոցով, որոնք անվանվում են վեկտորներ։ Վեկտորները սովորաբար միջատներ են, բայց կարող են լինել նաև սնկեր, նեմատոդներ, նախակենդանիներ։ Հիվանդությունը կանխելու նպատակով տնտեսապես ավելի ձեռնտու է ոչնչացնել հիվանդությունը տարածող վեկտորներին և այլընտրանքային տերերին, որոնք սովորաբար մոլախոտեր են[235]։ Բուսական վիրուսները չեն կարող վարակել մարդկանց և այլ կենդանիներին, քանի որ կարող են բազմանալ միայն բուսական բջիջներում[236]։
Բույսերն ունեն շատ ուժեղ և բարդ հակավիրուսային պաշտպանության մեխանիզմներ։ Ամենաարդյունավետ մեխանիզմներից մեկը այսպես կոչված դիմադրության (R) գեներն են։ Յուրաքանչյուր R գեն ապահովում է որոշակի վիրուսի հանդեպ պաշտպանությունը՝ վարակված բջջի շուրջը գտնվող այլ բջիջների մահվամբ, որը կանխում է վարակի հետագա տարածումը։ Մահացած բջիջների այս շերտը շատ հաճախ նկատելի է նույնիսկ անզեն աչքով[237]։ ՌՆԹ ինտերֆերենցիան նույնպես համարվում է բույսերի հակավիրուսային պաշտպանության արդյունավետ եղանակ[238]։ Վարակվելու դեպքում, բույսերը շատ հաճախ արտադրում են բնական մանրէազերծող նյութեր, օրինակ՝ սալիցիլաթթու, ազոտի օքսիդ, ռեակտիվ թթվածնի մոլեկուլներ, որոնք ոչնչացնում են վիրուսներին[239]։
Բուսական վիրուսների մասնիկները կամ վիրուսանման մասնիկները (անգլ.՝ virus-like particle - VLP) կիրառվում են կենսատեխնոլոգիայում և նանոտեխնոլոգիայում։ Շատ բույսերի վիրուսների կապսիդներ պարզ են և դիմացկուն և վարակված բույսերի կողմից կարող են սինթեզվել մեծ քանակությամբ։ Կենսատեխնոլոգիայի միջոցով բուսական վիրուսների մասնիկները կարող են ենթարկվել գենետիկական և քիմիական ձևափոխությունների, պատիճավորել օտարածին նյութերը և միավորվելով ձևավորել վերմոլեկուլային կառույցներ[240]։
Բակտերիաների վիրուսներ[խմբագրել | խմբագրել կոդը]

Բակտերիոֆագերը ամենատարածված և բազմաքանակ վիրուսների խումբն են և ամենահարուստ կենսաձևն են ջրային միջավայրում. օվկիանոսում վիրուսների քանակը մոտ 10 անգամ գերազանցում է բակտերիաների քանակը[241], 1 միլիոն ջրում հասնելով 250 000 000-ի[242]։
Այս վիրուսները վարակում են բակտերիաներին՝ միանալով վերջիններիս բջջաթաղանթի արտաքին ռեցեպտորների հետ և մուտք գործում բջիջ[243]։ Կարճ ժամանակ անց, որը կարող է նույնիսկ տևել մի քանի րոպե, բակտերիալ պոլիմերազը սկսում է տրանսլյացիայի ենթարկել վիրուսային իՌՆԹ-ն և սինթեզել սպիտակուցներ։ T4 բակտերոֆագի դեպքում, վիրուսի ներխուժելուց ընդամենը 12 րոպեում կարող են ձևավորվել ավելի քան երեք հարյուր ֆագեր[244]։
Բակտերիայի վիրուսային պաշտպանության հիմնական մեխանիզմը օտարածին ԴՆԹ-ի հաջորդականությունները քայքայող ֆերմենտների սինթեզն է։ Այս ֆերմենտներն անվանվում են խզող էնդոնուկլեազներ և կտրտում են բակտերիալ բջիջ թափանցած վիրուսային ԴՆԹ-ի հատվածները[245]։ Բակտերիան ունակ է նաև CRISPR հաջորդականությունների միջոցով ճանաչել նախկինում արդեն հանդիպած վիրուսների գենոմի հատվածները և արգելակել վիրուսների կրկնապատկումը ՌՆԹ ինտերֆերենցիայի ձևերից մեկի միջոցով[246][247]։ Այս գենետիկական մեխանիզմը ապահովում է բակտերիայի հակավիրուսային իմունիտետը։
Բակտերիոֆագերը կարող են նաև օգտակար լինել բակտերիաների համար։ Օրինակ, մարդու համար այդքան վտանգավոր դիֆտերիայի հարուցչի թույնը կոդավորող գենը գաղտնագրում է այդ բակտերիան վարակող բակտերիոֆագը[248]։
Արքեաների վիրուսներ[խմբագրել | խմբագրել կոդը]

Շատ վիրուսներ կրկնապատկվում են արքեաներում. սրանք երկպարույր ԴՆԹ վիրուսներ են շատ հաճախ տարօրինակ, չկրնվող ձևով[85][250]։ Այս վիրուսները մանրամասն ուսումնասիրված են ջերմասեր արքեաների մոտ, և հատկապես Sulfolobales ու Thermoproteales կարգերում[251]։ Արքեաների այս վիրուսների դեմ պաշտպանությունը ընդգրկում է ՌՆԹ ինտերֆերենցիան[252][253]
Վիրուսների վիրուսներ[խմբագրել | խմբագրել կոդը]
Միմիվիրուսի ուսումնասիրման ժամանակ պարզվել է, որ վիրուսի վրա հավաքվում են մեկ այլ վիրուսի ոչ մեծ վիրիոններ։ Այս վիրուսներն անվանվել են սպուտնիկներ (անգլ.՝ Sputnik)[254]։ Սպուտնիկներն, ամենայն հավանականությամբ, չեն կարող վարակել միմի- և մամավիրուսների տեր հանդիսացող ամեոբաներին, սակայն կարող են միմի- և մամավիրուսների հետ բազմանալ նրանց մեջ, որի պատճառով սպուտնիկները դասակարգվում են որպես արբանյակ վիրուսներ։ Սպուտնիկները առաջին հայտնի վիրուս արբանյակներն են, պարունակում են երկշղթա ԴՆԹ և բազմանում են էուկարիոտ բջիջների ներսում։ Հետազոտության հեղինակները առաջարկում են սպուտնիկներին դիտարկել ոչ թե որպես արբանյակներ, այլ որպես վիրոֆագեր (վիրուսների վիրուսներ)[255][256][257]։ Այս երկու հասկացությունների տարբերությունը նրանում է, որ վիրուս արբանյակների կրկնապատկման համար պահանջվում է տեր բջջի և տեր վիրուսի առկայությունը, այն դեպքում, երբ վիրոֆագերը վերարտադրվում են միայն տեր վիրուսի կրկնապատկման ապարատի շնորհիվ և միայն վիրուսի մակաբույծներ են[258]։ Վիրոֆագի գենոմում առկա են միմիվիրուսին բնորոշ կարգավորիչ տարրեր, որոնք ճանաչում են վերջինիս տրանսկրիպցիոն ապարատը։ Բացի այդ, սպուտնիկի առկայությունը զգալիորեն նվազեցնում է միմիվիրուսի բազմացումը բջջում. առաջանում են դեֆեկտավոր վիրիոններ, տեր բջջի լիզիսը դանդաղում է[254]։ Չնայած այս ամենին, սպուտնիկների վիրոֆագեր լինելը վերջնականապես ապացուցված չէ։
Հայտնաբերվել է նաև միմիվիրուսի CL շտամի մեկ այլ վիրոֆագ[259]։
Դերը էվոլյուցիայում[խմբագրել | խմբագրել կոդը]

Վիրուսները կարևոր դեր են կատարում տարբեր տեսակների միջև գեների տեղափոխման մեջ, որը մեծացնում է տեսակների գենետիկական բազմազանությունը[260]։ Ենթադրվում է, որ վիրուսները կենտրոնական դեր են ունեցել Երկրի վրա կյանքի վաղ էվոլյուցիայում, երբ բակտերիաները, արքեաներն ու էուկարիոտները դեռևս առանձնացած չէին և երբ ապրում էր ընդհանուր ունիվերսալ վերջին նախնին (անգլ.՝ LUCA)[261]։ Վիրուսները մինչև օրս էլ Երկրի վրա չուսումնասիրված և չբացահայտված գենետիկական բազմազանության հսկայական շտեմարաններից մեկն են[262]։
Վիրուսները գենետիկորեն կապված են Երկրի բուսական (ֆլորա) և կենդանական աշխարհի (ֆաունա) հետ։ Վերջերս կատարված հետազոտությունների համաձայն՝ մարդու գենոմի շուրջ 32%-ը կազմված է վիրուսանման տարրերից, տրանսպոզոններից և նրանց մնացորդներից[263]։ Վիրուսների միջոցով հնարավոր է գեների հորիզոնական տեղափոխությունը (քսենոլոգիա), երբ գենետիկական տեղեկատվությունը փոխանցվում է ոչ թե ծնողներից իրենց ժառանգներին, այլ մեկ առանձնյակից՝ մյուսին (առանձնյակները կարող են նույնիսկ պատկանել տարբեր տեսակների)։ Այսպես օրինակ՝ ենթադրվում է, որ բարձրակարգ պրիմատների մոտ սինցիտին սպիտակուցը կոդավորող գենը կապիկների գենոմ է բերվել ռետրովիուսների միջոցով[264]։
Վիրուսները կենսոլորտում[խմբագրել | խմբագրել կոդը]
Վիրուսները Երկիր մոլորակի վրա ամենաբազմաքանակ օրգանական մատերիայի գոյության ձևն են։ Վիրուսները կարևոր են բազմաթիվ կենդանի օրգանիզմների պոպուլյացիաների քանակի կարգավորման համար։ Շատ հաճախ վիրուսները կենդանիների հետ առաջացնում են սիմբիոզ[265][266]։ Այսպես օրինակ, որոշ թունավոր կրետների թույնը պարունակում է պոլի-ԴՆԹ-վիրուսներ (Polydnavirus, PDV) կոչվող կառույցներ, որոնք ունեն վիրուսային ծագում։
Կենսոլորտում վիրուսների հիմնական դերը կապված է օվկիանոսներում և ծովերում նրանց կատարած գործունեության հետ։
Դերը ջրային էկոհամակարգերում[խմբագրել | խմբագրել կոդը]
Ծովային ջրի մեկ թեյի գդալը պարունակում է մոտ մեկ միլիոն վիրուս[267]։ Սրանց մեծամասնությունը բակտերիոֆագեր են, որոնք անվնաս են կենդանիների և բույսերի համար և կարևոր են էկոհամակարգում քաղցրահամ և աղի ջրերի կարգավորման համար[268]։ Այս վիրուսները վարակում են և ոչնչացնում ծովային ջրերում առկա բակտերիաների գաղութները. այս մեխանիզմն շատ կարևոր է ջրային միջավայրում ածխածնի շրջապտույտի մեջ։ Մահացած բակտերիալ բջիջներից դուրս բերված օրգանական մոլեկուլները նպաստում են նոր բակտերիաների և ջրիմուռների աճին[269]։ Վիրուսների ակտիվությունը կարող է նպաստել նաև կենսաբանական պոմպի գործընթացին. վերջինիս ժամանակ խորը օվկիանոսում տեղի է ունենում ածխածնի մեկուսացում և կուտակում[262]։
Միկրօրգանիզմները կազմում են ծովի կենսազանգվածի ավելի քանի 90%-ը։ Ենթադրվում է, որ վիրուսները կարող են ամեն օր ոչնչացնել այս կենսազանգվածի մոտ 20%-ը և որ օվկիանոսում վիրուսները բակտերիաներից և արքեաներից 15 անգամ ավելի շատ են։ Վիրուսները ծաղկող ջրի ջրիմուռները ոչնչացնող հիմնական գործոններն են[270], որոնք հաճախ կարող են ոչնչացնել նաև այլ ջրային օրգանիզմներ[271]։
Վիրուսների քանակը ափից հեռու և օվկիանոսի խորքը շարժվելիս քչանում է, որի պատճառը ավելի քիչ քանակով կենդանի օրգանիզմների գոյությունն է[262]։
Ծովային կաթնասունները նույնպես վարակվում են վիրուսներով։ 1988 և 2002 թվականներին հազարավոր ծովային կատուներ են սպանվել Phocine distemper վիրուսի պատճառով[272]։ Կալցիվիրուսները, հերպեսվիրուսները, ադենովիրուսները և պարվովիրուսները և այլ վիրուսներ, շրջապտույտի են ենթարկվում կաթնասունների պոպուլյացիաներում[262]։
Կիրառություն[խմբագրել | խմբագրել կոդը]
Բնական գիտություններ և բժշկագիտություն[խմբագրել | խմբագրել կոդը]

Վիրուսները որպես պարզագույն համակարգեր մեծ կարևորություն ունեն մոլեկուլային և բջջային կենսաբանության հետազոտությունների համար, դրանք լայնորեն կիրառվում են բջիջների ֆունկցիայի հետազոտման մեջ[273]։ Վիրուսների հետազոտությունն ու կիրառումը թույլ է տվել բացահայտել բջջային կենսաբանության շատ հարցեր[274]։ Օրինակ, վիրուսները հաջողությամբ կիրառվել են գենետիկական հետազոտություններում և օգնել հասկանալ մոլեկուլային գենետիկայի հիմնական մեխանիզմները՝ ԴՆԹ-ի ռեպլիկացիան, փոխադրումը, ՌՆԹ պրոցեսինգը, տրանսլյացիան, սպիտակուցների տեղափոխումը, իմունոլոգիական շատ մեխանիզմներ և այլն։
Գենետիկները հաճախ վիրուսներն օգտագործում են որպես ուսումնասիրվող գեների վեկտորներ։ Այսպես հնարավոր է դառնում բջջին ստիպել սինթեզել օտարածին միացություն, հետազոտել գենոմում տեղագրված նոր գենի ազդեցությունը։ Նույն կերպ, վիրոթերապիայում վիրուսները կիրառվում են տարբեր հիվանդությունների բուժման մեջ, իրենց թիրախ բջջի կամ ԴՆԹ-ի վրա ընտրողաբար ազդելու ընդունակության հաշվին։ Վիրուսների կիրառումը քաղցկեղի բուժման և գենային թերապիայում հեռանկարային է։ Արևելաեվրոպական գիտնականները կիրառել են ֆագ-թերապիան որպես հակաբիոտիկների այլընտրանք։ Այժմ այս մեթոդի հանդեպ հետաքրքրությունը աճում է, քանի որ որոշ ախտածին բակտերիաներ դիմադրողականություն են ձեռք բերում հակաբիոտիկների նկատմամբ[275]։ Վերջերս արտադրության են դրվել որոշ վիրուսային վեկտորներ և դեղագործական սպիտակուցներ, որոնք գտնվում են նախակլինիկական և կլինիկական փորձարկման փուլերում[276]։
Նյութագիտություն և նանոտեխնոլոգիա[խմբագրել | խմբագրել կոդը]
Նանոտեխնոլոգիաների զարգացումը խոստանում է վիրուսների կիրառության ավելի բազմազան ձևեր։ Նյութագետի տեսանկյունից վիրուսները օրգանական նանոմասնիկներ են։
Վիրուսների մակերեսին կան հատուկ մոլեկուլներ, որոնց միջոցով այն թափանցում է տեր բջջի մեջ։ Վիրուսների չափն ու մեծությունը և նրանց մակերեսին առկա ֆունկցիոնալ խմբերի քանակն ու բնույթը ճշտությամբ որոշված է։ Սրա հաշվին, վիրուսները լայնորեն կիրառվում են նյութագիտության մեջ որպես կովալենտ կապերով կապված մակերեսային ձևափոխությունների կաղապարներ։ Որոշ վիրուսներ կարող են ենթարկվել նպատակաուղվված էվոլյուցիայի։ Նանոնյութերի հետ աշխատելու համար մշակված բնագիտական մեթոդները դառնում են նանոինժիներիայի հիմքերից մեկը և օգտագործվում այլ գիտությունների կողմից նույնպես[277]։
Իրենց մեծության, չափերի և լավ բնութագրված քիմիական կառուցվածքի շնորհիվ, վիրուսները օգտագործվել են որպես նանոկաղապարներ։ Վաշինգտոնի Ծովային հետազոտությունների լաբորատորիայում վիրուսները հաջողությամբ կիրառվել են որպես ազդանշանի ուժեղացուցիչներ[278]։ Մեկ այլ հետազոտության մեջ վիրուսներն օգտագործվել են որպես նանոսալիկներ՝ մոլեկուլային էլեկտրոնիկայի համար[279]։
Սինթետիկ վիրուսներ[խմբագրել | խմբագրել կոդը]
Շատ վիրուսներ կարող են սինթեզվել de novo (զրոյից). առաջին սինթետիկ վիրուսը ստեղծվել է 2002 թվականին[280]։ Ի տարբերություն հասարակության մեջ տարածված կարծիքի, սինթեզվում է ոչ թե վիրուսը, այլ ավելի շատ վիրուսային գենոմը՝ ԴՆԹ՝ ԴՆԹ վիրուսների և կոմպլեմենտար ԴՆԹ՝ ՌՆԹ վիրուսների դեպքում։ Վիրուսների շատ ընտանիքիների դեպքում միայն վիրուսային գենոմի տեղագրումը բջջի ներսում արդեն առաջ է բերում վարակում։ Սա նշանակում է, որ այս վիրուսները պարունակում են վիրուսի սինթեզի համար անհրաժեշտ ամբողջ տեղեկատվությունը։ Այս տեխնոլոգիան այժմ կիրառվում է պատվաստանյութերի նոր ռազմավարություններ մշակելու համար[281]։ Այսպիսով վիրուսները չեն համարվում վերացած այնքան ժամանակ, քանի դեռ նրանց գենոմը հայտնի է և կան ընկալունակ բջիջներ։ 2014 թվականի մարտից ծաղիկի գենոմի 3843 հիմքերից բաղկացած հաջորդականությունը ազատ հասանելի է օնլայն Առողջության ազգային ինստիտուտի կայքում[282]։
Կենսաբանական զենք[խմբագրել | խմբագրել կոդը]

Հասարակության մեջ վիրուսների համաճարակ առաջացնելու ընդունակությունը առաջացրել է այն մտահոգությունը, որ նրանք կարող են կիրառվել կենսաբանական զենք ստեղծելու մեջ։ Մտահոգությունն ավելի խորացել է, երբ լաբորատոր պայմաններում արհեստականորեն վերստեղծվել է 1918 թվականի գրիպի վիրուսը[283]։ Ծաղիկի վիրուսը մինչև բուժման հայտնաբերումը պատմության ընթացքում մեծ ազդեցություն է գործել տարբեր հասարակությունների վրա։ Աշխարհում կա ընդամենը երկու կենտրոն, որոնք ԱՀԿ կողմից թույլատրված են պահել ծաղիկի վիրուսը՝ Ռուսաստանի վեկտորի ինստիտուտը և Միացյալ Նահանգների հիվանդությունների կառավարման և կանխարգելման կենտրոնը[284]։ Այն վախը, որ ծաղիկի վիրուսը կարող է օգտագործվել որպես կենսաբանական զենք մասամբ հիմնավորված է, քանի որ ծաղիկի պատվաստը հաճախ ունենում է կողմնակի ազդեցություն և շատ երկրների կողմից պարբերաբար չի օգտագործվում։ Սրա արդյունքում ներկայումս մարդկանց պոպուլյացիան աշխարհում չունի կայուն պատշպանություն ծաղիկի հանդեպ և կարող է խոցելի լինել վիրուսի նկատմամբ[284]։
Զանգվածային մշակույթում[խմբագրել | խմբագրել կոդը]
Ֆիլմերում և այլ ստեղծագործություններում վարակիչ, այդ թվում վիրուսային հիվանդությունների աշխարհը հաճախ ճիշտ ներկայացված չէ։ Ֆիլմերի մեծամասնությունը նոր վարակի բռնկման մասին է, որի հարուցիչը ստեղծվել է կենսաահաբեկչության, լաբորատորիայի պատահարի պատճառով կամ էլ հայտնվել է տիեզերքից[285].
Գրականության մեջ[խմբագրել | խմբագրել կոդը]
Հետևյալ ստեղծագործությունների սյուժեում վիրուսային վարակներն ունեն կարևոր նշանակություն.
- Կոձի Սուձուկի, «Զանգ»
- Կիր Բուլիչյով, «Մանուշակագույն գունդ»
- Սթիվեն Քինգ, «Դիմակայություն»
- Մայքլ Քրայտոն, «Շտամ «Անդրոմեդա»»[285].
- Ռիչարդ Մեթիսոն, «Ես լեգենդ եմ»
- Դեն Բրաուն, «Ինֆեռնո»
Կինոմատոգրաֆիայում[խմբագրել | խմբագրել կոդը]
Հետևյալ ֆիլմերի սյուժեի հիմքում վիրուսային վարակի բռնկումն է[285]՝
- Մահացու սխալ (անգլ.՝ Fatal Error) (1999)
- Պանդորայի ժամացույցը (անգլ.՝ Pandora's Clock) (1996)
- Այրման գոտի (անգլ.՝ Burning Zone) (1996)
- 28 օր անց (լատին․՝ 28 Days Later) (2003)
- 28 շաբաթ անց (անգլ.՝ 28 Weeks Later) (2007)
- Շտամ «Անդրոմետա», այս ֆիլմը նկարահանված է համանուն գրքի սյուժեի հիման վրա[285]։
- 12 կապիկ (1995)
- «Չարիքի կացարանը» (2002) և ֆիլմի հաջորդ մասերը
- «Համաճարակ» (1995)
- «Մանուշակագույն գունդ» (1987)
- «Վարակակիրները» (2009)
- «Ես լեգենդ եմ» (2007)
- «Վարակում» (2011)
- «Կարանտին» (2008)
- «Կարանտին 2։ Տերմինալ» (2011)
- «ՌեԳենեզիս» (հեռուստասերիալ, 2004—2008)
- «Փակ դպրոց» (հեռուստասերիալ, 2011-2013)
- «Արդյունքում կենդանի մնալ» (հեռուստասերիալ, 2013)
Մուլտիպլիկացիայում[խմբագրել | խմբագրել կոդը]
Վերջին շրջանում վիրուսների շատ հաճախ դառնում են մուլտֆիլմերի և մուլտսերիալների «հերոսներ»։ Այդ մուլտֆիլմերից է «Օսմոսիս Ջոնս» (ԱՄՆ, 2001), «Օզին և Դրիքսը» (ԱՄՆ, 2002-2004 թվականներ) և «Վիրուսը հարձակվում է» (Իտալիա, 2011)։
Նշումներ[խմբագրել | խմբագրել կոդը]
- ↑ Անգլերենում այս բառի հոգնակի ձևի օգտագործումը միանշանակ չէ։ Լատիներեն վիրուս բառը (լատին․՝ virus) պատկանում է հազվադեպ հանդիպող -us-ով վերջացող չեզոք սեռի երկրորդ հոլովման գոյականներին և հոլովվում է՝ Nom.Acc.Voc. virus, Gen. viri, Dat.Abl. viro։ Նույն կերպ են հոլովվում նաև լատին․՝ vulgus և pelagus բառերը։ Դասական լատիներենում հոգնակի թիվ ունի միայն վերջին բառը՝ pelage, որն ունի հին հունական ծագում և որում՝ η<εα:
- ↑ Ինչպես նշված է զեկույցում՝ «վիրուսի տեսակը սերունդների ընդհանուր գիծ առաջացնող և որոշակի էկոլոգիական խորշում գոյություն ունեցող վիրուսների պոլիտետիկ դաս է»։ Պոլիտետիկ դասը կարգաբանական խումբ է, որի անդամները ունեն որոշ ընդհանուր հատկանիշներ, սակայն ամբողջությամբ միմյանց նման չեն։ Սրանով վիրուսի տեսակը տարբերվում է ավելի վեր գտնվող կարգաբանական խմբերից, որոնք ունիվերսալ դասեր են՝ բնորոշ հատկանիշները տարածվում են կարգաբանական խմբի բոլոր անդամների վրա
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Վիրուսների կարգաբանությունը Վիրուսների կարագաբանության միջազգային հանձնաժողովի (ICTV) կայքում]]
- ↑ 2,0 2,1 Դիմմոք, Ն.Ջ.; Իստոն, Էնդրու Ջ; Լեփփարդ, Կիթ (2007). Ժամանակակից վիրուսոլոգիայի հիմունքներ(անգլերեն) (6 ed.). Blackwell Publishing. ISBN 1405136456.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Dimmock p. 49
- ↑ 4,0 4,1 Breitbart M, Rohwer F (2005). «Here a virus, there a virus, everywhere the same virus?». Trends Microbiol. 13 (6): 278–84. doi:10.1016/j.tim.2005.04.003. PMID 15936660.
- ↑ Էդվարդս ՌԱ, Ռոհվեր Ֆ. (2005 թ․ հունիս). «Վիրուսական մետագենոմիկա». Nat. Rev. Microbiol. 3 (6): 504–10. doi:10.1038/nrmicro1163. PMID 15886693.
- ↑ Edwards RA, Rohwer F (2005). «Viral metagenomics». Nature Reviews Microbiology. 3 (6): 504–10. doi:10.1038/nrmicro1163. PMID 15886693.
- ↑ Կոլիեր, Լեսլի; Բալոզ, Ալբերտ; Սուսման, Մաքս ((1998)). Մահի, Բրայան և Կոլիեր, Լեսլի։ (ed.). Տոպլի և Վիլսոնի Մանրէաբանություն և Մանրէաբանական Վարակներ (անգլերեն). Vol. 1, Virology (9 ed.). էջ 33–55. ISBN 0340663162.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Կանչայա Ս., Ֆուրնուս Գ., Չիբանի-Չեննուֆի Ս., Դիլման ՄԼ, Բրուսով Հ. (2003 թ․ օգոստոս). «Ֆագերը որպես կողմնային գենի փոխադրումի միջոցներ (անգլերեն)». Curr. Opin. Microbiol. 6 (4): 417–24. PMID 12941415.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors pp. 49–50
- ↑ 10,0 10,1 Harper D (2011). «virus». The Online Etymology Dictionary. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
- ↑ Harper D (2011). «virulent». The Online Etymology Dictionary. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
- ↑ Harper D (2011). «viral». The Online Etymology Dictionary. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
- ↑ Harper D (2011). «virion». The Online Etymology Dictionary. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
- ↑ Casjens S (2010). Mahy BWJ and Van Regenmortel MHV (ed.). Desk Encyclopedia of General Virology. Boston: Academic Press. էջ 167. ISBN 0-12-375146-2.
- ↑ Մեսրոպ Կ. Գույումճեան, Ընդարձակ Բառարան Անգլիերէնէ Հայերէն. Պէյրութ։ Կ. Տօնիկեան և Եղբայրք (1981)։ էջ 1353
- ↑ Օտար բառերի բացատրական բառարան։ (Շուրջ 8000 բառային միավոր). Աշոտ Պուշկինի Հայրապետյան, Երևան 2004
- ↑ Bordenave G. (2003). «Louis Pasteur (1822—1895)». Microbes and Infection / Institut Pasteur. 5 (6): 553–560. doi:10.1016/S1286-4579(03)00075-3. PMID 12758285.
- ↑ Shors, 2008, էջեր 76—77
- ↑ Collier, էջ 3
- ↑ Dimmock, 2007, էջ 4—5
- ↑ 21,0 21,1 Collier, 1998, էջ 3
- ↑ 22,0 22,1 Fenner F. (2009). Mahy B. W. J. and Van Regenmortal M. H. V. (ed.). Desk Encyclopedia of General Virology (1 ed.). Oxford, UK: Academic Press. էջ 15. ISBN 0-12-375146-2.
- ↑ Shors, 2008, էջ 589
- ↑ D'Herelle F. (2007). «On an invisible microbe antagonistic toward dysenteric bacilli: brief note by Mr. F. D'Herelle, presented by Mr. Roux». Research in Microbiology. 158 (7): 553–4. doi:10.1016/j.resmic.2007.07.005. PMID 17855060.
- ↑ Steinhardt E, Israeli C, Lambert R.A. (1913). «Studies on the cultivation of the virus of vaccinia». J. Inf Dis. 13 (2): 294–300. doi:10.1093/infdis/13.2.294.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Collier, 1998, էջ 4
- ↑ Goodpasture EW, Woodruff AM, Buddingh GJ (1931). «The cultivation of vaccine and other viruses in the chorioallantoic membrane of chick embryos». Science. 74 (1919): 371–372. Bibcode:1931Sci....74..371G. doi:10.1126/science.74.1919.371. PMID 17810781.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Stanley WM, Lauffer MA (1939). «Disintegration of tobacco mosaic virus in urea solutions». Science. 89 (2311): 345–347. Bibcode:1939Sci....89..345S. doi:10.1126/science.89.2311.345. PMID 17788438.
- ↑ Rosen, F. S. (2004). «Isolation of poliovirus—John Enders and the Nobel Prize». New England Journal of Medicine. 351 (15): 1481–83. doi:10.1056/NEJMp048202. PMID 15470207.
- ↑ Norrby E (2008). «Nobel Prizes and the emerging virus concept». Arch. Virol. 153 (6): 1109–23. doi:10.1007/s00705-008-0088-8. PMID 18446425.
- ↑ Collier, 1998, էջ 745
- ↑ Temin H. M., Baltimore D. (1972). «RNA-directed DNA synthesis and RNA tumor viruses» (PDF). Adv. Virus Res. 17: 129–86. doi:10.1016/S0065-3527(08)60749-6. PMID 4348509. Վերցված է 2008 թ․ սեպտեմբերի 16-ին.
- ↑ Barré-Sinoussi, F.; և այլք: (1983). «Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS)» (PDF). Science. 220 (4599): 868–871. doi:10.1126/science.6189183. PMID 6189183.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն) - ↑ (Buist J. B. Vaccinia and Variola: a study of their life history Churchill, London)
- ↑ Stanley W. M., Loring H. S. (1936). «The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants». Science. 83 (2143): 85. doi:10.1126/science.83.2143.85. PMID 17756690.
- ↑ Stanley W. M., Lauffer M. A. (1939). «Disintegration of tobacco mosaic virus in urea solutions». Science. 89 (2311): 345–347. doi:10.1126/science.89.2311.345. PMID 17788438.
- ↑ Creager A. N., Morgan G. J. (2008). «After the double helix: Rosalind Franklin's research on Tobacco mosaic virus». Isis. 99 (2): 239–72. doi:10.1086/588626. PMID 18702397.
- ↑ Dimmock, 2007, էջ 12
- ↑ Cello J., Paul A. V., Wimmer E. (2002). «Chemical synthesis of poliovirus cDNA: generation of infectious virus in the absence of natural template». Science. 297 (5583): 1016–8. doi:10.1126/science.1072266. PMID 12114528.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «Ա.Բ.Ալեքսանյանի անվան համաճարակաբանության, վիրուսաբանության և բժշկական մակաբուծաբանության ԳՀԻ պաշտոնական կյանք». Արխիվացված է օրիգինալից 2017 թ․ նոյեմբերի 10-ին. Վերցված է 2015 թ․ հունվարի 19-ին.
- ↑ ՀՀ ԳԱԱ մոլեկուլային կենսաբանության ինստիտուտ ՀՀ ԳԱԱ կայքում
- ↑ Karalyan Z. A., Avagyan H. R. (2006). «Selective cytotoxicity and modification activity of picornaviruses on transformed cell lines». Biopolym. Cell. 27: 377–380. doi:10.7124/bc.000127.
- ↑ Հայաստան հանրագիտարան, Հայկական հանրագիտարան հրատարակչություն, Երևան, 2012 թ, էջ 435-437
- ↑ Iyer LM, Balaji S, Koonin EV, Aravind L (2006). «Evolutionary genomics of nucleo-cytoplasmic large DNA viruses». Virus Res. 117 (1): 156–84. doi:10.1016/j.virusres.2006.01.009. PMID 16494962.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 45,0 45,1 Sanjuán R, Nebot MR, Chirico N, Mansky LM, Belshaw R (2010 թ․ հոկտեմբեր). «Viral mutation rates». Journal of Virology. 84 (19): 9733–48. doi:10.1128/JVI.00694-10. PMC 2937809. PMID 20660197.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors, 2008, էջեր 14—16
- ↑ Collier, 1998, էջեր 11—21
- ↑ Dimmock, 2007, էջ 16
- ↑ Collier, 1998, էջ 11
- ↑ 50,0 50,1 50,2 Mahy W. J. & Van Regenmortel M. H. V. (eds) (2009). Desk Encyclopedia of General Virology. Oxford: Academic Press. էջ 24. ISBN 0-12-375146-2.
{{cite book}}:|author=has generic name (օգնություն) - ↑ Shors, 2008, էջ 574
- ↑ McClintock, B. (1950). «The origin and behavior of mutable loci in maize». Proc Natl Acad Sci U S A. 36 (6): 344–55. doi:10.1073/pnas.36.6.344. PMC 1063197. PMID 15430309.
- ↑ Dimmock, 2007, էջ 4
- ↑ Collier, 1998, էջեր 11—12
- ↑ Dimmock, 2007, էջ 55
- ↑ Shors 551–3
- ↑ Tsagris EM, de Alba AE, Gozmanova M, Kalantidis K (2008). «Viroids». Cell. Microbiol. 10 (11): 2168. doi:10.1111/j.1462-5822.2008.01231.x. PMID 18764915.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors, 2008
- ↑ 59,0 59,1 La Scola B., Desnues C., Pagnier I., Robert C., Barrassi L., Fournous G., Merchat M., Suzan-Monti M., Forterre P., Koonin E., Raoult D. (2008). «The virophage as a unique parasite of the giant mimivirus». Nature. 455 (7209): 100–4. doi:10.1038/nature07218. PMID 18690211.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Collier, 1998, էջ 777
- ↑ Dimmock, 2007, էջեր 55—57
- ↑ Mahy W. J. & Van Regenmortel M. H. V. (eds) (2009). Desk Encyclopedia of General Virology. Oxford: Academic Press. էջ 28. ISBN 0-12-375146-2.
{{cite book}}:|author=has generic name (օգնություն) - ↑ Dimmock pp. 15–16
- ↑ 64,0 64,1 Liberski P. P. (2008). «Prion diseases: a riddle wrapped in a mystery inside an enigma». Folia Neuropathol. 46 (2): 93–116. PMID 18587704.
- ↑ 65,0 65,1 Mahy W. J. & Van Regenmortel M. H. V. (eds) (2009). Desk Encyclopedia of General Virology. Oxford: Academic Press. էջ 26. ISBN 0-12-375146-2.
{{cite book}}:|author=has generic name (օգնություն) - ↑ Dimmock, 2007, էջեր 15—16
- ↑ Инге-Вечтомов С. Г. Генетика с основами селекции. — СПб.: Издательство Н-Л, 2010. — С. 298. — 718 с. — ISBN 978-5-94869-105-3
- ↑ Belay E. D. and Schonberger L. B. (2009). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. էջեր 497–504. ISBN 0-12-375147-0.
- ↑ Lupi O., Dadalti P., Cruz E., Goodheart C. (2007). «Did the first virus self-assemble from self-replicating prion proteins and RNA?». Med. Hypotheses. 69 (4): 724–30. doi:10.1016/j.mehy.2007.03.031. PMID 17512677.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Holmes EC (2007). «Viral evolution in the genomic age». PLoS Biol. 5 (10): e278. doi:10.1371/journal.pbio.0050278. PMC 1994994. PMID 17914905.
{{cite journal}}: CS1 սպաս․ չպիտակված ազատ DOI (link) - ↑ Wimmer E., Mueller S., Tumpey T. M., Taubenberger J. K. (2009). «Synthetic viruses: a new opportunity to understand and prevent viral disease». Nature Biotechnology. 27 (12): 1163–72. doi:10.1038/nbt.1593. PMC 2819212. PMID 20010599.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Horn M. (2008). «Chlamydiae as symbionts in eukaryotes» (PDF). Annual Review of Microbiology. 62: 113–31. doi:10.1146/annurev.micro.62.081307.162818. PMID 18473699.
- ↑ Ammerman N. C., Beier-Sexton M., Azad A. F. (2008). «Laboratory maintenance of Rickettsia rickettsii». Current Protocols in Microbiology. Chapter 3: Unit 3A.5. doi:10.1002/9780471729259.mc03a05s11. PMC 2725428. PMID 19016440.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Koonin E. V., Senkevich T. G., Dolja V. V. (2006). «The ancient Virus World and evolution of cells». Biol. Direct. 1: 29. doi:10.1186/1745-6150-1-29. PMC 1594570. PMID 16984643.
{{cite journal}}: More than one of|pages=and|page=specified (օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ չպիտակված ազատ DOI (link) - ↑ Seed K. D., Lazinski D. W., Calderwood S. B., Camilli A. (2013). «A bacteriophage encodes its own CRISPR/Cas adaptive response to evade host innate immunity». Nature. 494 (7438): 489–91. doi:10.1038/nature11927. PMC 3587790. PMID 23446421. Արխիվացված է օրիգինալից 2016 թ․ մարտի 5-ին. Վերցված է 2015 թ․ հունվարի 19-ին.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 76,0 76,1 Collier, 1998, էջեր 33—55
- ↑ Stefan Sirucek (2014 թ․ մարտի 3). «Ancient "Giant Virus" Revived From Siberian Permafrost». National Geographic. Վերցված է 2014 թ․ մարտի 3-ին.
- ↑ Collier, 1998, էջեր 33—37
- ↑ Kiselev N. A., Sherman M. B., Tsuprun V. L. (1990). «Negative staining of proteins». Electron Microsc. Rev. 3 (1): 43–72. doi:10.1016/0892-0354(90)90013-I. PMID 1715774.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Collier, 1998, էջ 40
- ↑ Caspar D. L., Klug A. (1962). «Physical principles in the construction of regular viruses» (PDF). Cold Spring Harb. Symp. Quant. Biol. 27: 1–24. PMID 14019094.
- ↑ Crick F. H., Watson J. D. (1956). «Structure of small viruses» (PDF). Nature. 177 (4506): 473–5. doi:10.1038/177473a0. PMID 13309339.
- ↑ Falvo, M.R.; S. Washburn, R. Superfine, M. Finch, F. P. Brooks Jr, V. Chi, R. M. Taylor 2nd (1997). «Manipulation of individual viruses: friction and mechanical properties». Biophysical Journal. 72 (3): 1396–1403. doi:10.1016/S0006-3495(97)78786-1. PMC 1184522. PMID 9138585.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ թվային անուններ: authors list (link) - ↑ Kuznetsov, Yu. G.; A. J. Malkin, R. W. Lucas, M. Plomp, A. McPherson (2001). «Imaging of viruses by atomic force microscopy» (PDF). J Gen Virol. 82 (9): 2025–2034. PMID 11514711.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link)(չաշխատող հղում) - ↑ 85,0 85,1 Prangishvili D, Forterre P, Garrett RA (2006). «Viruses of the Archaea: a unifying view». Nature Reviews Microbiology. 4 (11): 837–48. doi:10.1038/nrmicro1527. PMID 17041631.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Collier, 1998, էջ 37
- ↑ Collier, 1998, էջեր 40, 42
- ↑ Casens, S. (2009). Desk Encyclopedia of General Virology. Boston: Academic Press. էջեր 167–174. ISBN 0-12-375146-2.
- ↑ Rossmann MG, Mesyanzhinov VV, Arisaka F, Leiman PG (2004). «The bacteriophage T4 DNA injection machine». Curr. Opin. Struct. Biol. 14 (2): 171–80. doi:10.1016/j.sbi.2004.02.001. PMID 15093831.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Collier, 1998, էջեր 42—43
- ↑ Long G. W., Nobel J., Murphy F. A., Herrmann K. L., Lourie B. (1970). «Experience with electron microscopy in the differential diagnosis of smallpox». Appl Microbiol. 20 (3): 497–504. PMC 376966. PMID 4322005.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Xiao C., Kuznetsov Y. G., Sun S., Hafenstein S. L., Kostyuchenko V. A., Chipman P. R., Suzan-Monti M., Raoult D., McPherson A., Rossmann M. G. Structural studies of the giant mimivirus // PLoS Biol. — 2009. — В. 4. — Т. 7. — С. e92. — — PMID 19402750.
- ↑ Klose T., Kuznetsov Y. G., Xiao C., Sun S., McPherson A., Rossmann M. G. The three-dimensional structure of Mimivirus // Intervirology. — 2010. — В. 5. — Т. 53. — С. 268—273. — — PMID 20551678.
- ↑ «World's biggest virus discovered in ocean depths near Chile». Արխիվացված օրիգինալից 2013 թ․ փետրվարի 1-ին. Վերցված է 2011 թ․ հոկտեմբերի 12-ին.
- ↑ 95,0 95,1 Dimmock, 2007, էջ 49
- ↑ 96,0 96,1 96,2 Collier, 1998, էջեր 96—99
- ↑ Saunders, Venetia A.; Carter, John (2007). Virology: principles and applications. Chichester: John Wiley & Sons. էջեր 72. ISBN 0-470-02387-2.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Van Etten J. L., Lane L. C., Dunigan D. D. (2010). «DNA viruses: the really big ones (giruses)». Annual Review of Microbiology. 64: 83–99. doi:10.1146/annurev.micro.112408.134338. PMC 2936810. PMID 20690825.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Pressing J., Reanney D. C. (1984). «Divided genomes and intrinsic noise». J Mol Evol. 20 (2): 135–46. doi:10.1007/BF02257374. PMID 6433032.
- ↑ Duffy S., Holmes E. C. (2009). «Validation of high rates of nucleotide substitution in geminiviruses: phylogenetic evidence from East African cassava mosaic viruses» (PDF). The Journal of General Virology. 90 (Pt 6): 1539–47. doi:10.1099/vir.0.009266-0. PMID 19264617.(չաշխատող հղում)
- ↑ Pan X. P., Li L. J., Du W. B., Li M. W., Cao H. C., Sheng J. F. (2007). «Differences of YMDD mutational patterns, precore/core promoter mutations, serum HBV DNA levels in lamivudine-resistant hepatitis B genotypes B and C». J. Viral Hepat. 14 (11): 767–74. doi:10.1111/j.1365-2893.2007.00869.x. PMID 17927612. Արխիվացված է օրիգինալից 2021 թ․ մարտի 18-ին. Վերցված է 2015 թ․ հունվարի 18-ին.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Hampson A. W., Mackenzie J. S. (2006). «The influenza viruses». Med. J. Aust. 185 (10 Suppl): S39–43. PMID 17115950.
- ↑ Metzner K. J. (2006). «Detection and significance of minority quasispecies of drug-resistant HIV-1». J HIV Ther. 11 (4): 74–81. PMID 17578210.
- ↑ Goudsmit, Jaap. Viral Sex. Oxford Univ Press, 1998.ISBN 978-0-19-512496-5 ISBN 0-19-512496-0
- ↑ Worobey M., Holmes E. C. (1999). «Evolutionary aspects of recombination in RNA viruses». J. Gen. Virol. 80 (Pt 10): 2535–43. PMID 10573145.(չաշխատող հղում)
- ↑ Lukashev A. N. (2005). «Role of recombination in evolution of enteroviruses». Rev. Med. Virol. 15 (3): 157–67. doi:10.1002/rmv.457. PMID 15578739.
- ↑ Umene K. (1999). «Mechanism and application of genetic recombination in herpesviruses». Rev. Med. Virol. 9 (3): 171–82. doi:10.1002/(SICI)1099-1654(199907/09)9:3<171::AID-RMV243>3.0.CO;2-A. PMID 10479778.
- ↑ Collier, 1998, էջեր 75—91
- ↑ Dimmock, 2007, էջ 70
- ↑ Boevink P, Oparka KJ (2005). «Virus-host interactions during movement processes». Plant Physiol. 138 (4): 1815–21. doi:10.1104/pp.105.066761. PMC 1183373. PMID 16172094.
- ↑ Dimmock, 2007, էջ 71
- ↑ Barman S., Ali A., Hui E. K., Adhikary L., Nayak D. P. (2001). «Transport of viral proteins to the apical membranes and interaction of matrix protein with glycoproteins in the assembly of influenza viruses». Virus Res. 77 (1): 61–9. doi:10.1016/S0168-1702(01)00266-0. PMID 11451488.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors, 2008, էջեր 60, 597
- ↑ Dimmock, 2007, Chapter 15, Mechanisms in virus latentcy, էջեր 243—259
- ↑ Dimmock, 2007, էջեր 185—187
- ↑ Shors p. 54; Collier p. 78
- ↑ Collier, 1998, էջ 79
- ↑ Collier, 1998, էջեր 88—89
- ↑ Staginnus C., Richert-Pöggeler K. R. (2006). «Endogenous pararetroviruses: two-faced travelers in the plant genome». Trends in Plant Science. 11 (10): 485–91. doi:10.1016/j.tplants.2006.08.008. PMID 16949329.
- ↑ Collier, 1998, էջեր 115—146
- ↑ Collier, 1998, էջ 115
- ↑ Roulston A., Marcellus R. C., Branton P. E. (1999). «Viruses and apoptosis». Annu. Rev. Microbiol. 53: 577–628. doi:10.1146/annurev.micro.53.1.577. PMID 10547702.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Alwine J. C. (2008). «Modulation of host cell stress responses by human cytomegalovirus». Curr. Top. Microbiol. Immunol. 325: 263–79. doi:10.1007/978-3-540-77349-8_15. PMID 18637511.
- ↑ Sinclair J. (2008). «Human cytomegalovirus: Latency and reactivation in the myeloid lineage». J. Clin. Virol. 41 (3): 180–5. doi:10.1016/j.jcv.2007.11.014. PMID 18164651.
- ↑ Jordan M. C., Jordan G. W., Stevens J. G., Miller G. (1984). «Latent herpesviruses of humans». Ann. Intern. Med. 100 (6): 866–80. PMID 6326635.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Sissons J. G., Bain M., Wills M. R. (2002). «Latency and reactivation of human cytomegalovirus». J. Infect. 44 (2): 73–7. doi:10.1053/jinf.2001.0948. PMID 12076064.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Barozzi P., Potenza L., Riva G., Vallerini D., Quadrelli C., Bosco R., Forghieri F., Torelli G., Luppi M. (2007). «B cells and herpesviruses: a model of lymphoproliferation». Autoimmun Rev. 7 (2): 132–6. doi:10.1016/j.autrev.2007.02.018. PMID 18035323.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Subramanya D., Grivas P. D. (2008). «HPV and cervical cancer: updates on an established relationship». Postgrad Med. 120 (4): 7–13. doi:10.3810/pgm.2008.11.1928. PMID 19020360.
- ↑ Crawford, Dorothy H. (2011). Viruses: A Very Short Introduction. Oxford University Press, USA. էջ 16. ISBN 0-19-957485-5.
- ↑ Shors, 2008, էջ 388
- ↑ Shors, 2008, էջ 353
- ↑ Dimmock, 2007, էջ 272
- ↑ Baggesen D. L., Sørensen G., Nielsen E. M., Wegener H. C. (2010). «Phage typing of Salmonella Typhimurium – is it still a useful tool for surveillance and outbreak investigation?». Eurosurveillance. 15 (4): 19471. PMID 20122382.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «Systema Naturae 2000: Overview».
- ↑ «Taxonomicon: Aphanobionta».
- ↑ «Taxonomicon: Acytota».
- ↑ «Систематика органического мира: Бесклеточные (Acellularia)». Արխիվացված է օրիգինալից 2012 թ․ փետրվարի 23-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
- ↑ «NCBI taxonomy».
- ↑ Lwoff A, Horne RW, Tournier P (1962). «A virus system». C. R. Hebd. Seances Acad. Sci. (French). 254: 4225–7. PMID 14467544.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ չճանաչված լեզու (link) - ↑ Lwoff A, Horne R, Tournier P (1962). «A system of viruses». Cold Spring Harb. Symp. Quant. Biol. 27: 51–5. PMID 13931895.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Knipe, էջ 27
- ↑ Delwart E. L. (2007). «Viral metagenomics». Rev. Med. Virol. 17 (2): 115–31. doi:10.1002/rmv.532. PMID 17295196.
- ↑ «ICTV: Virus Taxonomy Assignments». Արխիվացված օրիգինալից 2013 թ․ ապրիլի 28-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
- ↑ «Virus Taxonomy: 2012 Release (current) (ICTV)». Արխիվացված է օրիգինալից 2013 թ․ ապրիլի 28-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
- ↑ Colson P., de Lamballerie X., Fournous G., Raoult D. Reclassification of giant viruses composing a fourth domain of life in the new order Megavirales // Intervirology. — 2012. — В. 5. — Т. 55. — С. 321—332. — — PMID 22508375.
- ↑ King A. M. Q., Lefkowitz E., Adams M. J., Carstens E. B. (2011). Virus Taxonomy: Ninth Report of the International Committee on Taxonomy of Viruses. Elsevier. էջ 6. ISBN 0-12-384684-6.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Virus Taxonomy 2009. Արխիվացված 2011-07-23 Wayback Machine International Committee on Taxonomy of Viruses. Retrieved on December 24, 2011.
- ↑ ICTV Master Species List 2009 Արխիվացված 2016-03-05 Wayback Machine
- Այս Excel ֆայլում մինչև 2009 թվականը հայտնի վիրուսներից ցանկն է։
- ↑ Baltimore D (1974). «The strategy of RNA viruses». Harvey Lect. 70 Series: 57–74. PMID 4377923.
- ↑ van Regenmortel MH, Mahy BW (2004). «Emerging issues in virus taxonomy». Emerging Infect. Dis. 10 (1): 8–13. PMID 15078590.
- ↑ Mayo MA (1999). «Developments in plant virus taxonomy since the publication of the 6th ICTV Report. International Committee on Taxonomy of Viruses». Arch. Virol. 144 (8): 1659–66. doi:10.1007/s007050050620. PMID 10486120.
- ↑ de Villiers EM, Fauquet C, Broker TR, Bernard HU, zur Hausen H (2004). «Classification of papillomaviruses». Virology. 324 (1): 17–27. doi:10.1016/j.virol.2004.03.033. PMID 15183049.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Baltimore D. (1974). «The strategy of RNA viruses». Harvey Lect. 70 Series: 57–74. PMID 4377923.
- ↑ Temin H. M., Baltimore D. (1972). «RNA-directed DNA synthesis and RNA tumor viruses». Adv. Virus Res. 17: 129–86. PMID 4348509.
- ↑ «The Big Picture Book of Viruses:Family Groups - The Baltimore Method». Արխիվացված օրիգինալից 2013 թ․ ապրիլի 28-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
- ↑ Komaroff A. L. (2006). «Is human herpesvirus-6 a trigger for chronic fatigue syndrome?». J. Clin. Virol. 37 Suppl 1: S39–46. doi:10.1016/S1386-6532(06)70010-5. PMID 17276367.
- ↑ Chen C., Chiu Y., Wei F., Koong F., Liu H., Shaw C., Hwu H., Hsiao K. (1999). «High seroprevalence of Borna virus infection in schizophrenic patients, family members and mental health workers in Taiwan». Mol Psychiatry. 4 (1): 33–8. doi:10.1038/sj.mp.4000484. PMID 10089006.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Margolis TP, Elfman FL, Leib D; և այլք: (2007). «Spontaneous reactivation of herpes simplex virus type 1 in latently infected murine sensory ganglia». J. Virol. 81 (20): 11069–74. doi:10.1128/JVI.00243-07. PMC 2045564. PMID 17686862.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Whitley R. J., Roizman B. (2001). «Herpes simplex virus infections». Lancet. 357 (9267): 1513–8. doi:10.1016/S0140-6736(00)04638-9. PMID 11377626.
- ↑ Barton E. S., White D. W., Cathelyn J. S.; և այլք: (2007). «Herpesvirus latency confers symbiotic protection from bacterial infection». Nature. 447 (7142): 326–9. doi:10.1038/nature05762. PMID 17507983.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Bertoletti A., Gehring A. (2007). «Immune response and tolerance during chronic hepatitis B virus infection». Hepatol. Res. 37 Suppl 3: S331–8. doi:10.1111/j.1872-034X.2007.00221.x. PMID 17931183.
- ↑ Rodrigues C, Deshmukh M, Jacob T, Nukala R, Menon S, Mehta A (2001). «Significance of HBV DNA by PCR over serological markers of HBV in acute and chronic patients». Indian journal of medical microbiology. 19 (3): 141–4. PMID 17664817.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Nguyen VT, McLaws ML, Dore GJ (2007). «Highly endemic hepatitis B infection in rural Vietnam». Journal of Gastroenterology and Hepatology. 22 (12): 2093. doi:10.1111/j.1440-1746.2007.05010.x. PMID 17645465.
{{cite journal}}: More than one of|pages=and|page=specified (օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Fowler M. G., Lampe M. A., Jamieson D. J., Kourtis A. P., Rogers M. F. (2007). «Reducing the risk of mother-to-child human immunodeficiency virus transmission: past successes, current progress and challenges, and future directions». Am. J. Obstet. Gynecol. 197 (3 Suppl): S3–9. doi:10.1016/j.ajog.2007.06.048. PMID 17825648.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Sauerbrei A., Wutzler P. (2000). «The congenital varicella syndrome». Journal of perinatology: official journal of the California Perinatal Association. 20 (8 Pt 1): 548–54. PMID 11190597.
- ↑ Garnett G. P. (2005). «Role of herd immunity in determining the effect of vaccines against sexually transmitted disease» (PDF). J. Infect. Dis. 191 Suppl 1: S97–106. doi:10.1086/425271. PMID 15627236.(չաշխատող հղում)
- ↑ Platonov A. E. (2006). «(The influence of weather conditions on the epidemiology of vector-borne diseases by the example of West Nile fever in Russia)». Vestn. Akad. Med. Nauk SSSR (Russian) (2): 25–9. PMID 16544901.
{{cite journal}}: CS1 սպաս․ չճանաչված լեզու (link) - ↑ Shors, 2008, էջ 198
- ↑ Shors, 2008, էջեր 199, 209
- ↑ Food and Agriculture Organization. African swine fever—outbreak in the Caucasus and why Australia should be aware. 2008. April [1](չաշխատող հղում)
- ↑ Shors, 2008, էջ 126
- ↑ 172,0 172,1 Shors, 2008, էջեր 193—194
- ↑ Shors, 2008, էջ 194
- ↑ Shors, 2008, էջեր 192—193
- ↑ Ranlet P. (2000). «The British, the Indians, and smallpox: what actually happened at Fort Pitt in 1763?». Pa Hist. 67 (3): 427–41. PMID 17216901. Վերցված է 2008 թ․ սեպտեմբերի 16-ին.(չաշխատող հղում)
- ↑ Van Rijn K. (2006). «"Lo! The poor Indian!" colonial responses to the 1862–63 smallpox epidemic in British Columbia and Vancouver Island». Can Bull Med Hist. 23 (2): 541–60. PMID 17214129.
- ↑ Patterson K. B., Runge T. (2002). «Smallpox and the Native American». Am. J. Med. Sci. 323 (4): 216–22. doi:10.1097/00000441-200204000-00009. PMID 12003378.
- ↑ Sessa R., Palagiano C., Scifoni M. G., di Pietro M., Del Piano M. (1999). «The major epidemic infections: a gift from the Old World to the New?». Panminerva Med. 41 (1): 78–84. PMID 10230264.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Bianchine P. J., Russo T. A. (1992). «The role of epidemic infectious diseases in the discovery of America». Allergy Proc. 13 (5): 225–32. doi:10.2500/108854192778817040. PMID 1483570. Վերցված է 2008 թ․ սեպտեմբերի 16-ին.
- ↑ Hauptman L. M. (1979). «Smallpox and American Indian; Depopulation in Colonial New York». N Y State J Med. 79 (12): 1945–9. PMID 390434.
- ↑ Fortuine R. (1988). «Smallpox decimates the Tlingit (1787)». Alaska Med. 30 (3): 109. PMID 3041871.
{{cite journal}}: More than one of|pages=and|page=specified (օգնություն) - ↑ Collier, 1998, էջեր 409—415
- ↑ Patterson K. D., Pyle G. F. (1991). «The geography and mortality of the 1918 influenza pandemic». Bull Hist Med. 65 (1): 4–21. PMID 2021692.
- ↑ Johnson N. P., Mueller J. (2002). «Updating the accounts: global mortality of the 1918–1920 "Spanish" influenza pandemic». Bull Hist Med. 76 (1): 105–15. doi:10.1353/bhm.2002.0022. PMID 11875246.
- ↑ Gao F., Bailes E., Robertson D. L.; և այլք: (1999). «Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes» (PDF). Nature. 397 (6718): 436–441. doi:10.1038/17130. PMID 9989410. Արխիվացված է օրիգինալից (PDF) 2005 թ․ փետրվարի 23-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors, 2008, էջ 447
- ↑ Mawar N., Saha S., Pandit A., Mahajan U. (2005). «The third phase of HIV pandemic: social consequences of HIV/AIDS stigma & discrimination & future needs» (PDF). Indian J. Med. Res. 122 (6): 471–84. PMID 16517997. Արխիվացված է օրիգինալից (PDF) 2016 թ․ մարտի 4-ին. Վերցված է 2008 թ․ սեպտեմբերի 13-ին.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «Status of the global HIV epidemic» (PDF). UNAIDS. 2008. Արխիվացված (PDF) օրիգինալից 2013 թ․ մարտի 9-ին. Վերցված է 2008 թ․ սեպտեմբերի 15-ին.
- ↑ Towner J. S., Khristova M. L., Sealy T. K.; և այլք: (2006). «Marburgvirus genomics and association with a large hemorrhagic fever outbreak in Angola» (PDF). J. Virol. 80 (13): 6497–516. doi:10.1128/JVI.00069-06. PMC 1488971. PMID 16775337. Արխիվացված է օրիգինալից (PDF) 2018 թ․ հուլիսի 25-ին. Վերցված է 2015 թ․ հունվարի 16-ին.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Einstein M. H., Schiller J. T., Viscidi R. P., Strickler H. D., Coursaget P., Tan T., Halsey N., Jenkins D. (2009). «Clinician's guide to human papillomavirus immunology: knowns and unknowns». The Lancet Infectious Diseases. 9 (6): 347–56. doi:10.1016/S1473-3099(09)70108-2. PMID 19467474.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shuda M., Feng H., Kwun H. J., Rosen S. T., Gjoerup O., Moore P. S., Chang Y. (2008). «T antigen mutations are a human tumor-specific signature for Merkel cell polyomavirus». Proceedings of the National Academy of Sciences of the United States of America. 105 (42): 16272–7. doi:10.1073/pnas.0806526105. PMC 2551627. PMID 18812503.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Pulitzer M. P., Amin B. D., Busam K. J. (2009). «Merkel cell carcinoma: review». Advances in Anatomic Pathology. 16 (3): 135–44. doi:10.1097/PAP.0b013e3181a12f5a. PMID 19395876.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Koike K. (2007). «Hepatitis C virus contributes to hepatocarcinogenesis by modulating metabolic and intracellular signalling pathways». J. Gastroenterol. Hepatol. 22 Suppl 1: S108–11. doi:10.1111/j.1440-1746.2006.04669.x. PMID 17567457.
- ↑ Hu J., Ludgate L. (2007). «HIV-HBV and HIV-HCV coinfection and liver cancer development». Cancer Treat. Res. 133: 241–52. doi:10.1007/978-0-387-46816-7_9. PMID 17672044.
- ↑ Bellon M., Nicot C. (2007). «Telomerase: a crucial player in HTLV-I-induced human T-cell leukemia». Cancer genomics & proteomics. 4 (1): 21–5. PMID 17726237.
- ↑ Schiffman M., Castle P. E., Jeronimo J., Rodriguez A. C., Wacholder S. (2007). «Human papillomavirus and cervical cancer». Lancet. 370 (9590): 890–907. doi:10.1016/S0140-6736(07)61416-0. PMID 17826171.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Klein E., Kis L. L., Klein G. (2007). «Epstein-Barr virus infection in humans: from harmless to life endangering virus-lymphocyte interactions». Oncogene. 26 (9): 1297–305. doi:10.1038/sj.onc.1210240. PMID 17322915.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ zur Hausen H. (2008). «Novel human polyomaviruses—re-emergence of a well known virus family as possible human carcinogens». International Journal of Cancer. Journal International Du Cancer. 123 (2): 247–50. doi:10.1002/ijc.23620. PMID 18449881.
- ↑ Alberts, Bruce; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walters (2002). Molecular Biology of the Cell; Fourth Edition. New York and London: Garland Science. ISBN 0-8153-3218-1. Վերցված է 2008 թ․ սեպտեմբերի 15-ին.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Ding S. W., Voinnet O. (2007). «Antiviral immunity directed by small RNAs». Cell. 130 (3): 413–26. doi:10.1016/j.cell.2007.07.039. PMC 2703654. PMID 17693253.
- ↑ Patton J. T., Vasquez-Del Carpio R., Spencer E. (2004). «Replication and transcription of the rotavirus genome». Curr. Pharm. Des. 10 (30): 3769–77. doi:10.2174/1381612043382620. PMID 15579070.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Jayaram H., Estes M. K., Prasad B. V. (2004). «Emerging themes in rotavirus cell entry, genome organization, transcription and replication». Virus Res. 101 (1): 67–81. doi:10.1016/j.virusres.2003.12.007. PMID 15010218.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Greer S., Alexander G. J. (1995). «Viral serology and detection». Baillieres Clin. Gastroenterol. 9 (4): 689–721. doi:10.1016/0950-3528(95)90057-8. PMID 8903801.
- ↑ Matter L., Kogelschatz K., Germann D. (1997). «Serum levels of rubella virus antibodies indicating immunity: response to vaccination of subjects with low or undetectable antibody concentrations» (PDF). J. Infect. Dis. 175 (4): 749–55. doi:10.1086/513967. PMID 9086126.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Mallery D. L., McEwan W. A., Bidgood S. R., Towers G. J., Johnson C. M., James L. C. (2010 թ․ նոյեմբեր). «Antibodies mediate intracellular immunity through tripartite motif-containing 21 (TRIM21)». Proceedings of the National Academy of Sciences of the United States of America. 107 (46): 19985–90. doi:10.1073/pnas.1014074107. PMC 2993423. PMID 21045130.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Cascalho M., Platt J. L. (2007). «Novel functions of B cells». Crit. Rev. Immunol. 27 (2): 141–51. PMID 17725500.
- ↑ Le Page C., Génin P., Baines M. G., Hiscott J. (2000). «Interferon activation and innate immunity». Rev Immunogenet. 2 (3): 374–86. PMID 11256746.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Hilleman M. R. (2004). «Strategies and mechanisms for host and pathogen survival in acute and persistent viral infections» (PDF). Proc. Natl. Acad. Sci. U.S.A. 101 Suppl 2: 14560–6. doi:10.1073/pnas.0404758101. PMC 521982. PMID 15297608.(չաշխատող հղում)
- ↑ Asaria P, MacMahon E. Measles in the United Kingdom: can we eradicate it by 2010?. BMJ. 2006;333(7574):890–5. doi:10.1136/bmj.38989.445845.7C. PMID 17068034.
- ↑ Lane JM. Mass vaccination and surveillance/containment in the eradication of smallpox. Curr. Top. Microbiol. Immunol.. 2006;304:17–29. doi:10.1007/3-540-36583-4_2. PMID 16989262.
- ↑ Arvin AM, Greenberg HB. New viral vaccines. Virology. 2006;344(1):240–9. doi:10.1016/j.virol.2005.09.057. PMID 16364754.
- ↑ Pastoret PP, Schudel AA, Lombard M. Conclusions—future trends in veterinary vaccinology. Rev. – Off. Int. Epizoot.. 2007;26(2):489–94, 495–501, 503–9. PMID 17892169.
- ↑ Palese P. Making better influenza virus vaccines?. Emerging Infect. Dis.. 2006;12(1):61–5. doi:10.3201/eid1201.051043. PMID 16494719.
- ↑ Thomssen R. Live attenuated versus killed virus vaccines. Monographs in allergy. 1975;9:155–76. PMID 1090805.
- ↑ McLean AA. Development of vaccines against hepatitis A and hepatitis B. Rev. Infect. Dis.. 1986;8(4):591–8. PMID 3018891.
- ↑ Casswall TH, Fischler B. Vaccination of the immunocompromised child. Expert review of vaccines. 2005;4(5):725–38. doi:10.1586/14760584.4.5.725. PMID 16221073.
- ↑ Barnett ED, Wilder-Smith A, Wilson ME. Yellow fever vaccines and international travelers. Expert Rev Vaccines. 2008;7(5):579–87. doi:10.1586/14760584.7.5.579. PMID 18564013.
- ↑ Magden J, Kääriäinen L, Ahola T (2005). «Inhibitors of virus replication: recent developments and prospects». Appl. Microbiol. Biotechnol. 66 (6): 612–21. doi:10.1007/s00253-004-1783-3. PMID 15592828.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Mindel A, Sutherland S (1983). «Genital herpes — the disease and its treatment including intravenous acyclovir». J. Antimicrob. Chemother. 12 Suppl B: 51–9. PMID 6355051.
- ↑ Witthöft T, Möller B, Wiedmann KH; և այլք: (2007). «Safety, tolerability and efficacy of peginterferon alpha-2a and ribavirin in chronic hepatitis C in clinical practice: The German Open Safety Trial». J. Viral Hepat. 14 (11): 788–96. doi:10.1111/j.1365-2893.2007.00871.x. PMC 2156112. PMID 17927615.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Rudin D, Shah SM, Kiss A, Wetz RV, Sottile VM (2007). «Interferon and lamivudine vs. interferon for hepatitis B e antigen-positive hepatitis B treatment: meta-analysis of randomized controlled trials». Liver Int. 27 (9): 1185–93. doi:10.1111/j.1478-3231.2007.01580.x. PMC 2156150. PMID 17919229.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Dimmock p. 3
- ↑ «International Society for Viruses of Microorganisms: Protist Viruses» (անգլերեն). Վերցված է 2013 թ․ փետրվարի 28-ին.(չաշխատող հղում)
- ↑ Philippe Colson, Gregory Gimenez, Mickaël Boyer, Ghislain Fournous, Didier Raoult. The Giant Cafeteria roenbergensis Virus That Infects a Widespread Marine Phagocytic Protist Is a New Member of the Fourth Domain of Life(անգլ.).
- ↑ Goris N, Vandenbussche F, De Clercq K (2008). «Potential of antiviral therapy and prophylaxis for controlling RNA viral infections of livestock». Antiviral Res. 78 (1): 170–8. doi:10.1016/j.antiviral.2007.10.003. PMID 18035428.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Carmichael L (2005). «An annotated historical account of canine parvovirus». J. Vet. Med. B Infect. Dis. Vet. Public Health. 52 (7–8): 303–11. doi:10.1111/j.1439-0450.2005.00868.x. PMID 16316389.
- ↑ Chen YP, Zhao Y, Hammond J, Hsu H, Evans JD, Feldlaufer MF (October–November 2004). «Multiple virus infections in the honey bee and genome divergence of honey bee viruses». Journal of Invertebrate Pathology. 87 (2–3): 84–93. doi:10.1016/j.jip.2004.07.005. PMID 15579317.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Tinsley T. W., Harrap K. A. «Viruses of Invertebrates» (անգլերեն). Վերցված է 2013 թ․ փետրվարի 27-ին.
- ↑ «Invertebrate iridescent viruses (Iridoviridae)» (անգլերեն). Վերցված է 2013 թ․ փետրվարի 27-ին.
- ↑ «Вирусы беспозвоночных» (ռուսերեն). Վերցված է 2013 թ․ փետրվարի 27-ին.
- ↑ 231,0 231,1 231,2 «Вирусы грибов» (ռուսերեն). Վերցված է 2013 թ․ փետրվարի 27-ին.
- ↑ «McGraw-Hill Science & Technology Encyclopedia: Fungal virus» (անգլերեն). Վերցված է 2013 թ․ փետրվարի 27-ին.
- ↑ Дьяков Ю. Т., Шнырева А. В., Сергеев А. Ю. Введение в генетику грибов. — М.: изд. центр «Академия», 2005. — С. 57—58. — 304 с. — ISBN 5-7695-2174-0
- ↑ Белякова Г. А., Дьяков Ю. Т., Тарасов К. Л. Ботаника: в 4 томах. — М.: изд. центр «Академия», 2006. — Т. 1. Водоросли и грибы. — С. 73. — 320 с. — ISBN 5-7695-2731-5
- ↑ Shors p. 584
- ↑ Shors pp. 562–587
- ↑ Dinesh-Kumar SP, Tham Wai-Hong, Baker BJ (2000). «Structure—function analysis of the tobacco mosaic virus resistance gene N». PNAS. 97 (26): 14789–94. Bibcode:2000PNAS...9714789D. doi:10.1073/pnas.97.26.14789. PMC 18997. PMID 11121079.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Shors pp. 573–576
- ↑ Soosaar JL, Burch-Smith TM, Dinesh-Kumar SP (2005). «Mechanisms of plant resistance to viruses». Nature Reviews Microbiology. 3 (10): 789–98. doi:10.1038/nrmicro1239. PMID 16132037.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Lomonossoff, GP (2011). «Virus Particles and the Uses of Such Particles in Bio- and Nanotechnology». Recent Advances in Plant Virology. Caister Academic Press. ISBN 978-1-904455-75-2.
- ↑ Wommack KE, Colwell RR (2000). «Virioplankton: viruses in aquatic ecosystems». Microbiol. Mol. Biol. Rev. 64 (1): 69–114. doi:10.1128/MMBR.64.1.69-114.2000. PMC 98987. PMID 10704475.
- ↑ Bergh O, Børsheim KY, Bratbak G, Heldal M (1989). «High abundance of viruses found in aquatic environments». Nature. 340 (6233): 467–8. Bibcode:1989Natur.340..467B. doi:10.1038/340467a0. PMID 2755508.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «What are Phages? The Microbiome-Friendly Therapeutic Approach to Treating Severe Infections». The Phage - Exploring the virus of microbes (բրիտանական անգլերեն). Վերցված է 2022 թ․ մարտի 9-ին.
- ↑ Shors pp. 595–97
- ↑ Bickle TA, Krüger DH (1993 թ․ հունիսի 1). «Biology of DNA restriction». Microbiol. Rev. 57 (2): 434–50. PMC 372918. PMID 8336674.
- ↑ Barrangou R, Fremaux C, Deveau H; և այլք: (2007). «CRISPR provides acquired resistance against viruses in prokaryotes». Science. 315 (5819): 1709–12. Bibcode:2007Sci...315.1709B. doi:10.1126/science.1138140. PMID 17379808.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Brouns SJ, Jore MM, Lundgren M; և այլք: (2008). «Small CRISPR RNAs guide antiviral defense in prokaryotes». Science. 321 (5891): 960–4. Bibcode:2008Sci...321..960B. doi:10.1126/science.1159689. PMID 18703739.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ В. М. Жданов Человек и вирусы // Наука и человечество, 1984. — М.: Знание. — С. 44-55.
- ↑ Xiang X., Chen L., Huang X., Luo Y., She Q., Huang L. (2005). «Sulfolobus tengchongensis spindle-shaped virus STSV1: virus-host interactions and genomic features». J. Virol. 79 (14): 8677–86. doi:10.1128/JVI.79.14.8677-8686.2005. PMC 1168784. PMID 15994761.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Lawrence CM, Menon S, Eilers BJ; և այլք: (2009). «Structural and functional studies of archaeal viruses». J. Biol. Chem. 284 (19): 12599–603. doi:10.1074/jbc.R800078200. PMC 2675988. PMID 19158076.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Prangishvili D, Garrett RA (2004). «Exceptionally diverse morphotypes and genomes of crenarchaeal hyperthermophilic viruses». Biochem. Soc. Trans. 32 (Pt 2): 204–8. doi:10.1042/BST0320204. PMID 15046572.
- ↑ Mojica FJ, Díez-Villaseñor C, García-Martínez J, Soria E (2005). «Intervening sequences of regularly spaced prokaryotic repeats derive from foreign genetic elements». J. Mol. Evol. 60 (2): 174–82. doi:10.1007/s00239-004-0046-3. PMID 15791728.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Makarova KS, Grishin NV, Shabalina SA, Wolf YI, Koonin EV (2006). «A putative RNA-interference-based immune system in prokaryotes: computational analysis of the predicted enzymatic machinery, functional analogies with eukaryotic RNAi, and hypothetical mechanisms of action». Biol. Direct. 1: 7. doi:10.1186/1745-6150-1-7. PMC 1462988. PMID 16545108. Արխիվացված է օրիգինալից 2013 թ․ մայիսի 10-ին. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
{{cite journal}}: More than one of|pages=and|page=specified (օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ չպիտակված ազատ DOI (link) - ↑ 254,0 254,1 La Scola B., Desnues C., Pagnier I., Robert C., Barrassi L., Fournous G., Merchat M., Suzan-Monti M., Forterre P., Koonin E., Raoult D. The virophage as a unique parasite of the giant mimivirus // Nature. — 2008. — В. 7209. — Т. 455. — С. 100-104. — — PMID 18690211.
- ↑ Helen Pearson (2008). «'Virophage' suggests viruses are alive». Արխիվացված օրիգինալից 2013 թ․ փետրվարի 10-ին. Վերցված է 2013 թ․ փետրվարի 2-ին.
- ↑ Александр Марков (08.09.08). «Вирусы тоже болеют вирусными заболеваниями». Արխիվացված օրիգինալից 2013 թ․ փետրվարի 10-ին. Վերցված է 2013 թ․ փետրվարի 2-ին.
- ↑ Desnues C., Boyer M., Raoult D. Sputnik, a virophage infecting the viral domain of life // Adv Virus Res. — 2012. — Т. 82. — С. 63—89. — — PMID 22420851.
- ↑ Claverie J. M., Abergel C. Mimivirus and its virophage // Annu Rev Genet. — 2009. — Т. 43. — С. 49—66. — — PMID 19653859.
- ↑ La Scola B., Campocasso A., N'Dong R., Fournous G., Barrassi L., Flaudrops C., Raoult D. Tentative characterization of new environmental giant viruses by MALDI-TOF mass spectrometry // Intervirology. — 2010. — В. 5. — Т. 53. — С. 344—353. — — PMID 20551686.
- ↑ Canchaya C, Fournous G, Chibani-Chennoufi S, Dillmann ML, Brüssow H (2003). «Phage as agents of lateral gene transfer». Current Opinion in Microbiology. 6 (4): 417–24. doi:10.1016/S1369-5274(03)00086-9. PMID 12941415.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Forterre P, Philippe H (1999). «The last universal common ancestor (LUCA), simple or complex?». The Biological Bulletin. 196 (3): 373–5, discussion 375–7. doi:10.2307/1542973. PMID 11536914.
- ↑ 262,0 262,1 262,2 262,3 Suttle CA (2007). «Marine viruses—major players in the global ecosystem». Nature Reviews Microbiology. 5 (10): 801–12. doi:10.1038/nrmicro1750. PMID 17853907.
- ↑ International Human Genome Sequencing Consortium (2001). «Initial sequencing and analysis of the human genome». Nature. 409: 860–921. doi:10.1038/35057062.
- ↑ Mi S, Lee X, Li X, Veldman GM, Finnerty H, Racie L, LaVallie E, Tang XY, Edouard P, Howes S, Keith JC Jr, McCoy JM. (2000). «Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis». Nature. 403: 785–789. doi:10.1038/35001608. PMID 10693809.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «ScienceNow — «Ancient Virus Gave Wasps Their Sting»». Արխիվացված է օրիգինալից 2011 թ․ ապրիլի 15-ին. Վերցված է 2015 թ․ հունվարի 15-ին.
- ↑ Элементы — новости науки: Наездники подавляют иммунную защиту своих жертв при помощи прирученных вирусов
- ↑ Shors p. 4
- ↑ Shors p. 5
- ↑ Shors p. 593
- ↑ Suttle CA (2005). «Viruses in the sea». Nature. 437 (7057): 356–61. Bibcode:2005Natur.437..356S. doi:10.1038/nature04160. PMID 16163346.
- ↑ «Harmful Algal Blooms: Red Tide: Home». www.cdc.gov. Վերցված է 2014 թ․ դեկտեմբերի 19–ին-ին.
- ↑ Hall, A. J., Jepson, P. D., Goodman, S. J. & Harkonen, T. "Phocine distemper virus in the North and European Seas — data and models, nature and nurture". Biol. Conserv. 131, 221–229 (2006)
- ↑ Collier p.8
- ↑ Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James.Viruses:Structure, Function, and Uses Retrieved on 16 September 2008
- ↑ Matsuzaki S, Rashel M, Uchiyama J, Sakurai S, Ujihara T, Kuroda M, Ikeuchi M, Tani T, Fujieda M, Wakiguchi H, Imai S (2005 թ․ հոկտեմբեր). «Bacteriophage therapy: a revitalized therapy against bacterial infectious diseases». Journal of Infection and Chemotherapy: Official Journal of the Japan Society of Chemotherapy. 11 (5): 211–9. doi:10.1007/s10156-005-0408-9. PMID 16258815.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Gleba, YY; Giritch, A (2011). «Plant Viral Vectors for Protein Expression». Recent Advances in Plant Virology. Caister Academic Press. ISBN 978-1-904455-75-2.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Fischlechner M, Donath E (2007). «Viruses as Building Blocks for Materials and Devices». Angewandte Chemie International Edition. 46 (18): 3184. doi:10.1002/anie.200603445. PMID 17348058.
{{cite journal}}: More than one of|pages=and|page=specified (օգնություն) - ↑ Soto CM, Blum AS, Vora GJ; և այլք: (2006). «Fluorescent signal amplification of carbocyanine dyes using engineered viral nanoparticles». J. Am. Chem. Soc. 128 (15): 5184–9. doi:10.1021/ja058574x. PMID 16608355.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Blum AS, Soto CM, Wilson CD; և այլք: (2005). «An Engineered Virus as a Scaffold for Three-Dimensional Self-Assembly on the Nanoscale». Small. 7: 702. doi:10.1002/smll.200500021. PMID 17193509.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Cello J, Paul AV, Wimmer E (2002). «Chemical synthesis of poliovirus cDNA: generation of infectious virus in the absence of natural template». Science. 297 (5583): 1016–8. Bibcode:2002Sci...297.1016C. doi:10.1126/science.1072266. PMID 12114528.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Coleman JR, Papamichail D, Skiena S, Futcher B, Wimmer E, Mueller S (2008). «Virus attenuation by genome-scale changes in codon pair bias». Science. 320 (5884): 1784–7. Bibcode:2008Sci...320.1784C. doi:10.1126/science.1155761. PMC 2754401. PMID 18583614.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Genomes. «NIH viral genome database». Ncbi.nlm.nih.gov. Վերցված է 2014 թ․ մարտի 12-ին.
- ↑ Shors p. 331
- ↑ 284,0 284,1 Artenstein A. W., Grabenstein J. D. (2008). «Smallpox vaccines for biodefense: need and feasibility». Expert Review of Vaccines. 7 (8): 1225–37. doi:10.1586/14760584.7.8.1225. PMID 18844596.
- ↑ 285,0 285,1 285,2 285,3 Georgios Pappas, Savvas Seitaridis, Nikolaos Akritidis, Epaminondas Tsianos. Infectious Diseases in Cinema: Virus Hunters and Killer Microbes(անգլ.) // Clinical Infectious Diseases : Oxford Journals. — 2003. — Т. 37. — № 7. — С. 939—942. —
Գրականություն[խմբագրել | խմբագրել կոդը]
- Букринская А. Г. Вирусология. — М.: Медицина, 1986. — 336 с. (ռուս.)
- Mayo M. A., Pringle C. R. Virus taxonomy — 1997 // Journal of General Virology. — 1998. — № 79. — С. 649—657. Архивировано из первоисточника 29 Սեպտեմբերի 2007. (անգլ.)
- Collier, Leslie; Balows, Albert; Sussman, Max. Topley and Wilson’s Microbiology and Microbial Infections / Mahy, Brian and Collier, Leslie. Arnold. — ninth edition. — Virology, 1998. — Т. 1. — ISBN 0-340-66316-2 (անգլ.)
- Dimmock, N.J.; Easton, Andrew J.; Leppard, Keith. Introduction to Modern Virology. — sixth edition. — Blackwell Publishing, 2007. — ISBN 1-4051-3645-6(անգլ.)
- Knipe, David M.; Howley, Peter M.; Griffin, Diane E.; Lamb, Robert A.; Martin, Malcolm A.; Roizman, Bernard; Straus Stephen E. Fields Virology. — Lippincott Williams & Wilkins., 2007. — ISBN 0-7817-6060-7 (անգլ.)
- Shors, Teri. Understanding Viruses. — Jones and Bartlett Publishers, 2008. — ISBN 0-7637-2932-9 (անգլ.)
Արտաքին հղումներ[խմբագրել | խմբագրել կոդը]

- http://phene.cpmc.columbia.edu/index.htm Արխիվացված 2007-12-13 Wayback Machine
- Viruses ՝ բաց հասանելիությամբ ամսագիր։
- ViralZone Շվեյցարիայի կենսաինֆորմատիկայի ինստիտուտի կայքում(անգլ.)
- վիրուսներ 3D կառուցվածքը EM Data Bank (EMDB) կայքում(անգլ.)
| Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի՝ {{{1}}} թվականի {{{2}}} շաբաթվա հոդված։ |
|
|
Այս հոդվածը ներառված է Հայերեն Վիքիպեդիայի ընտրյալ հոդվածների ցանկում |
|
|
Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի՝ 2015 թվականի Տարվա հոդված |




