Ֆտոր
 Անվան այլ կիրառումների համար տե՛ս՝ F (այլ կիրառումներ)
Անվան այլ կիրառումների համար տե՛ս՝ F (այլ կիրառումներ)
| |||||
|---|---|---|---|---|---|
 Դեղին հեղուկ, անգույն գազ[1] Դեղին հեղուկ, անգույն գազ[1] | |||||
| Ատոմի հատկություններ | |||||
| Անվանում, սիմվոլ, կարգաթիվ | Ֆտոր / /Fluorum (F), F, 9 | ||||
| Ատոմային զանգված (մոլային զանգված) | 18,9984032(5)[2] զ. ա. մ. (գ/մոլ) | ||||
| Էլեկտրոնային կոնֆիգուրացիա | [He] 2s2 2p5 | ||||
| Ատոմի շառավիղ | 73 պմ | ||||
| Քիմիական հատկություններ | |||||
| Կովալենտ շառավիղ | 72 պմ | ||||
| Իոնի շառավիղ | (-1e)133 պմ | ||||
| Էլեկտրաբացասականություն | 3,98 (Պոլինգի սանդղակ) | ||||
| Էլեկտրոդային պոտենցիալ | 2,87 В | ||||
| Օքսիդացման աստիճաններ | −1 | ||||
| Իոնացման էներգիա (առաջին էլեկտրոն) | 1680,0 (17,41) կՋ/մոլ (էՎ) | ||||
| Պարզ նյութի թերմոդինամիկական հատկություններ | |||||
| Հալման ջերմաստիճան | 53.48 Կ[4] | ||||
| Եռման ջերմաստիճան | 85,03 Կ[4] | ||||
| Կրիտիկական կետ | 144,4 Կ, 500 ՄՊա | ||||
| Գոլորշիացման տեսակարար ջերմունակություն | 6088 կՋ/կգ ~ 340 կՋ/մոլ | ||||
| Մոլյար ջերմունակություն | 25,14 Ջ/(Կ·մոլ) | ||||
| Մոլային ծավալ | 17,1 սմ³/մոլ | ||||
| Պարզ նյութի բյուրեղային ցանց | |||||
| Բյուրեղացանցի տվյալներ | a=5,50 b=3,28 c=7,28 β=90,0 | ||||
| Դեբայի ջերմաստիճան | 460 Կ | ||||
| Այլ հատկություններ | |||||
| Ջերմահաղորդականություն | (300 Կ) 80.4 Վտ/(մ·Կ) | ||||
| CAS համար | CAS գրանցման համար? | ||||
| 9 | Ֆտոր
|
18,998 | |
| 2s22p5 | |
Ֆտոր (հին հունարեն՝ φθόρος «ոչնչացնել, վնասել, վնասվածք», հետագայում φθείρω «ոչնչացնել, ավերել»), տարրերի պարբերական համակարգի 2-րդ պարբերության 7-րդ խմբի տարր։ Քիմիական նշանը F (լատին․՝ Fluorum)։ Կարգահամարը՝ 9[5], ատոմական զանգվածը՝ 18,9984032(9)։ p-տարր է, պատկանում է հալոգենների շարքին, ատոմի էլեկտրոնային թաղանթների կառուցվածքն է․ 1S22S22P5։
Բնական ֆտորը բաղկացած է միայն 19F կայուն իզոտոպից։ Արհեստականորեն ստացվել են 16F (T½ <1 վրկ), 17F (T½ = 70 վրկ), 18F (111 ր), 20F (11,4 վրկ) և 21F (5 վրկ) ռադիոակտիվ իզոտոպները։
Ֆտորը խիստ թունավոր, սուր հոտով, բաց դեղնավուն գազ է, խտությունը՝ 1,693 կգ/մ³։ Բաղկացած է երկատոմանի մոլեկուլներից՝ F2, որոնց դիսոցման էներգիան 155±4 կջոուլ/մոլ է։
Հայտնագործման պատմություն
[խմբագրել | խմբագրել կոդը]Ֆտորը (F2) հայտնագործել է Կարլ Վիլհելմ Շեելեն 1771 թվականին, իսկ առաջին անգամ մաքուր վիճակում ստացել է Անրի Մուասսանը (1886)։ Իր անունը ստացել է հունարեն ֆտորոս-քայքայում բառից։
Ֆտորիի միացություններից կալցիումի ֆտորիդը՝ CaF2, մարդկությանը հայտնի է վաղուց, այն «ֆլյուոր» անվան տակ նկարագրվել է դեռևս 15-րդ դարի վերջին, որպես մետաղաձուլական մածուցիկ խարամները դյուրահոս դարձնող միջոց (այդտեղից էլ անվանումը՝ լատին․՝ fluo - հոսում եմ)։ 1771 թվականին «ֆլյուորը» ծծմբական թթվի հետ տաքացնելով Կ․ Շեեչեն ստացավ «պլավիկյան թթուն»․ Ա․ Լավուազիեն այն համարում էր անհայտ «ֆլյուորիում» տարրի միասությունը թթվածնի, իսկ ավելի ուշ (1810, Հ․ Դևի)՝ ջրածնի հետ։
Անվան ծագում
[խմբագրել | խմբագրել կոդը]Ֆտորի անվանումն (հունարեն՝ cpdopog - քայքայել) առաջարկել է Ա․ Ամպերը (1810)։ Ազատ ֆտորը առաջինն անջատել է ֆրանսիացի քիմիկոս Ա․ Մուասանը (1886)՝ կալիումի ֆտորիդ պարունակող հեղուկ ֆտորաջրածնի (անջուր) էլեկտրոլիզով։
Ֆտորի քիմիան բուռն զարգացել է 2-րդ՝ համաշխարհային պատերազմի տարիներին, երբ պարզվեց, որ ատոմային զենքի համար անհրաժէշտ 235Ս իզոտոպի անջատումը բնական ուրանից առավել արդյունավետ է իրականացնել UF6-ի օգնությամբ։ Ստացվեցին ֆտորի և նրա միացությունների նկատմամբ կայուն օրգանական միացություններ։
Բնության մեջ
[խմբագրել | խմբագրել կոդը]Ֆտորը երկրակեղևում տարածված տարր է (տարածվածությամբ տասներկուերորդը), կազմում է նրա զանգվածի 6,25-10−2%։ Հայտնի են ֆտորիդային 35 միներալներ, որոնցից ամենատարածվածները ֆլյուորիտը, կրիոլիտը և ֆտորապատիտն են։ Զգալի քանակով ֆտոր են պարունակում ապատիաները՝ և ֆոսֆորիտները։
| Օբյեկտ | Պարունակություն |
|---|---|
| հող | 0,02 |
| Գետի ջուր | 0,00002 |
| Ծովի ջուր | 0,0001 |
| մարդու ատամներում[6] | 0,01 |
Ֆտորը կենսաբանորեն ակտիվ միկրոտարր է, պարունակվում է բուսակա և կենդանական օրգանիզմներում։ Նրա կենսաբանական դերը վատ է ուսումնասիրված, պարզված է նրա նշանակությունը միայն ոսկրային հյուսվածքների համար։ Կենդանի օրգանիզմներում գտնվում է անօրգանական միացությունների ձևով, հատկապես ոսկրերում (100-300 մգ/կգ) և ատամներում։
| Ֆտորի ամենատարածված միացություններ | ||

|

|

|
| Ֆլյուորիտ | Ֆտորապատիտ | Կրիոլիտ |
Իզոտոպներ
[խմբագրել | խմբագրել կոդը]Բնական ֆտորը բաղկացած է միայն 19F կայուն իզոտոպից։ Արհեստականորեն ստացվել են 16F (T½ <1 վրկ), 17F (T½ = 70 վրկ), 18F (111 ր), 20F (11,4 վրկ) և 21F (5 վրկ) ռադիոակտիվ իզոտոպները։
Ֆտորի միջուկային իզոտոպների հատկությունները
[խմբագրել | խմբագրել կոդը]| Իզոտոպներ | Հարաբերական զանգված, զ. ա. մ. | Կյանիք տևողությունը | Տրոհման տեսակը | Միջուկային սպին | Միջուկային մագնիսական պահ |
|---|---|---|---|---|---|
| 17F | 17,0020952 | 64,5 c | β+-տրոհում 17O-ում | 5/2 | 4.722 |
| 18F | 18,000938 | 1,83 ժամ | β+-տրոհում в 18O | 1 | |
| 19F | 18,99840322 | կայուն | — | 1/2 | 2.629 |
| 20F | 19,9999813 | 11 c | β−-տրոհում 20Ne-ում | 2 | 2.094 |
| 21F | 20,999949 | 4,2 c | β−-տրոհում 21Ne-ում | 5/2 | |
| 22F | 22,00300 | 4,23 c | β−-տրոհում 22Ne-ում | 4 | |
| 23F | 23,00357 | 2,2 c | β−-տրոհում 23Ne-ում | 5/2 |
Էլեկտրոնային կառուցվածք
[խմբագրել | խմբագրել կոդը]
Ատոմի էլեկտրոնային թաղանթների կառուցվածքն է․ 1S22S22P5։
Ֆտորի ատոմում՝ 2-րդ էներգիական մակարդակում, չկա d օրբիտալ, շնորհիվ իր մեկ չզույգված էլեկտրոնի, բնորոշ է -1 օքսիդացման աստիճան և 1 վալենտականություն։ Ֆտորն ամենաէլեկտրաբացասական տարրն է (ԷԲ = 3,98) և օժտված է ուժեղագույն օքսիդիչ հատկությամբ։
Բյուրեղցանցի կառուցվածք
[խմբագրել | խմբագրել կոդը]
Ֆտորն առաջացնում է 2 բյուրեղային վերափոխակներ, որոնք մթնոլորտային ճնշման պայմաններում կայուն են։
- α-ֆտոր -գոյություն ունի 45,6 K ջերմաստիճանից բարձր պայմաններում, բյուրեղցանցի կառուցվածքը՝ ութանկյուն, տարածությունը C 2/c, տվյալները a = 0,550 նմ, b = 0,328 նմ, c = 0,728 նմ, β = 102,17°, Z = 4[7][8]։
- β-ֆտոր - գոյություն ունի 45,6 ÷ 53,53 K ջերմաստիճանային միջակայքում, բյուրեղցանցի կառուցվածք խորանարդ, տվյալները a = 0,667 նմ, Z = 8:
Ստացում
[խմբագրել | խմբագրել կոդը]Ֆտորիի ստացման հիմնական հումքը ֆլյուորիտն է (մասամբ նաև՝ ապատիտները և ֆոսֆորիտները)։ Նախ ստանում են HF, ապա՝ KF-HF որի հալույթը HF-ով հարստացնելուց հետո (մինչև 40-41 % HF) ենթարկում են էլեկտրոլիզի (95-100 °C, 9ժ11 վ)։ Գրաֆիտե անոդի վրա ստացված ֆտորը անջատում են սառեցնելով և նատրիումի ֆտորիդով կլանելով։

- Ֆտորը ստանում են հիմնականում կալիումի ֆտորիդի հալույթի էլեկտրոլիզով.
- 1986 թվականին ֆտորի 100-ամյակի միջոցառման կոնֆերանսին պատրաստվելու ժամանակ, Կառլ Կրիստը բացհայտեց մաքուր ֆտորի ստացման քիմիական եղանակը, օգտագործելով ֆտորաջրածինը K2MnF6 և SbF5 150 °C-ում լուծելիս[9].
- ։
Ֆտորի ուժեղ օքսիդացնող հատկությամբ պայմանավորված՝ գրեթեբոլոր մետաղները ենթարկվում են կոռոզիայի, այդ պատճառով ինչպես էլեկտրոլիզարարը, այնպես էլ տեղափոխման և պահպանման տարաները ստիպված պատրաստում են նիկելից, որը կայունություն է ձեռքբերում՝ շնորհիվ մետաղի մակերևույթին գոյացող աղի՝ NiF2, պաշտպանիչ շերտի։
Ֆիզիկական հատկություններ
[խմբագրել | խմբագրել կոդը]Բնականոն պայմաններում (0 °C, 0,1 ՄՆ/մ2) ֆտորը սուր հոտով, բաց դեղնավուն խիստ թունավոր գազ է, tեռ=-183C, tհալ =-219 C, խտությունը՝ 1,693 կգ/մ3։ Բաղկացած է երկատոմանի մոլեկուլներից՝ F2, որոնց դիսոցման էներգիան 155±4 կջոուլ/մոլ է։
Քիմիապես չափազանց ակտիվ և ռեակցիոնունակ տարր է, բնորոշ ոչ մետաղ։ Միացություններում ցուցաբերում է —1 օքսիդացման աստիճան։ Ամենաէլեկտրաբացասական տարրն է, ունի էլեկտրոնային մեծ խնամակցություն՝ 3,62 ԷՎ և իոնացման էներգիա՝ 17,418 ԷՎ։ Միանում է քիմիական բոլոր տարրերի հետ (բացառությամբ He, Ne և Ar)՝ առաջացնելով կայուն քիմիական կապեր։
Քիմիական հատկություններ
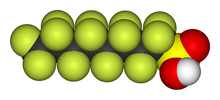
[խմբագրել | խմբագրել կոդը]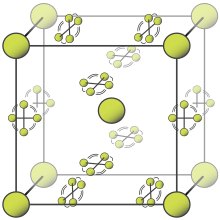
- Ֆտորի մթնոլորտում այրվում են այնպիսի կայուն նյութեր, ինչպիսիք ջուրը և ապակին են (բամբակի տեսքով).
Այրման արգասիքներից մեկը թթվածինն է, ինչը նշանակում է, որ ֆտորն ավելի ուժեղ օքսիդիչ է, քան թթվածինը։
- Ֆտորացման ռեակցիաները էքսոթերմիկ են և հաճախ ընթանում են բոցավառմամբ կամ պայթյունով։ Ջրածինը ֆտորում ինքնաբոցավառվում է, խառնուրդը պայթում է մթության մեջ անգամ առանց տաքացնլուց, ստացվում է ֆտորաջրածին, որի ջրային լուծույթը կոչվում է ֆտորաջրածնական թթու.
- Թթվածնի և ազոտի հետ ֆտորը միանում է էլեկտրական պարպումների ազդեցությամբ՝ առաջացնելով ֆտորիդներ։ Թթվածնի ֆտորիդները՝ OF2, Օ2F2, Օ3F3 և այլն, թունավոր են, ուժեղ օքսիդիչներ՝ օքսիդացնում են անգամ ջուրը և հալոգենները։ Նրանցից համեմատաբար կայուն է երկֆտորիդը՝ OF2, որը բնորոշ հոտով, անգույն գազ է։
- Ազոտի ֆտորիդները՝ NF3, N2F4 (անգույն գազեր), ավելի կայուն են, քայքայվում են տաքացնելիս, օքսիդիչներ են։ Մյուս հալոգենների հետ ֆտորը միանում է ջերմություն անջատելով՝ ստացվում են միջհալոգենային միացություններ (ֆտորիդներ), որոնք ուժեղ օքսիդներ են։ Քլորի հետ ֆտորը առաջացնում է ClF և C1F3 (200-250 °C-ում)։
- Յոդը և բրոմը բոցավառվում են ֆտորի մթնոլորտում, ստացվում են BrF, BrF3, BrF5, IF, IF5 և IF7։

- Ֆտորը անմիջականորեն միանում է կրիպտոնի, քսենոնի և ոադոնի հետ, առաջացնելով ֆտորիդներ՝ XeF4, XeFe, K2F2, RnF2 և այլն։
- Հալկոգենների ֆտորիդներից գործնական նշանակություն ունի միայն ծծմբի վեցֆտորիդը՝ SF6, որն օգտագործվում է որպես գազային դիէլեկտրիկ և աշխատանքային մարմին քիմիական գազային լազերներում։
- Մետաղների ֆտորիդները իոնական կառուցվածքով բյուրեղական նյութեր են, ֆտորաջրածնական թթվի աղերը։
- Ֆտորը շատ եռանդուն փոխազդում է ջրի, հիդրօքսիդների աղերի, ածխաջրածինների և բազմաթիվ այլ նյութերի հետ։
- Միակ թթուն է, որը լուծում է ապակին, շնորհիվ հետևյալ ռեակցիայի.
կամ
Այդ պատճառով պլավիկյան թթուն պահում են պլաստմասսայե կամ մոմապատ ամաններում։
Օքսիդը (F2O) անգույն, բնորոշ հոտով գազ է, tհալ=-224 °C, tեռ=19,5 °C։ Ստանում են ֆտորի և ալկալիների փոխազդեցությունից.
Պահպանում
[խմբագրել | խմբագրել կոդը]Ֆտորը պահում են և գազային վիճակում (ճնշման տակ), և հեղուկ վիճակում, ուժեղ օքսիդացնող հատկությամբ պայմանավորված՝ գրեթե բոլոր մետաղները ենթարկվում են կոռոզիայի, այդ պատճառով ինչպես էլեկտրոլիզարարը, այնպես էլ տեղափոխման և պահպանման տարաները ստիպված պատրաստում են նիկելից, որը կայունություն է ձեռքբերում՝ շնորհիվ մետաղի մակերևույթին գոյացող աղի՝ NiF2, պաշտպանիչ շերտի։
Կիրառություն
[խմբագրել | խմբագրել կոդը]
Ֆտորն օգտագործում են հատուկ պլաստմասսաների (տեֆլոն), ֆրեոնների և հեղուկ հրթիռային վառելիքի օքսիդիչի ստացման համար։ Ֆտորը լայնորեն օգտագործվում է որոշ օրգանական նյութերի՝ սառնագենտների և ֆտորապլաստների արտադրության համար։
Ֆտորը օգտագործվում է UF6, C1F2, SF6 և այլն ստանալով, UF6-ը՝ ուրանի իզոտոպներն իրարից բաժանելու համար, C1F3, WF6, SF6, BrF5-ը՝ և այլն որպես ֆտորացնող միջոցներ, իսկ SF6-ը՝ նաև էլեկտրատեխնիկայի արդյունաբերության մեջ։ Սառնարաններում գործածվող ֆրեոն՝ CCl2F2, դյուրաեռ հեղուկը, որը գոլորշիացման ենթարկվելիս (ճնշումը կտրուկ փոքրացնելու միջոցով) շրջապատից խլում է մեծ քանակով ջերմություն։ Նշված նյութը, որի քիմիական անունն է երկքլորերկֆտորմեթան, օգտագործվում է նաև որպես պրոպելենտ (ցնդելիություն ապահովող նյութ) զանազան աերոզոլերում և կենցաղային օդափոխիչներում։
Ֆտորից ստանում են քառաֆտոր էթիլեն՝ C2F4, որից էլ պոլիմերացման ռեակցիայով արտադրում են թանկարժեք պլաստմասսա՝ պոլիտետրաֆտորէթիլեն՝ տեֆլոն։
Հեղուկ ֆտորը հրթիռային վառելանյութի օքսիդիչ է։ Լայն կիրառում ունեն ֆտորաջրածինը, ալյումինի ֆտորիդը, սիլիցիումի ֆտորիդը և այլն։ Ֆտորի թույլատրելի առավելագույն քանակությունն օդում 0,15 մգ/մ3 է։
Կենսաբանական և ֆիզիոլագիական դեր
[խմբագրել | խմբագրել կոդը]Ֆտորի կենսաբանորեն ակտիվ միկրոտարր է, պարունակվում է բուսական և կենդանդանական օրգանիզմներում։ Նրա կենսաբանական դերը վատ է ուսումնասիրված, պարզված է նրա նշանակությունը միայն ոսկրային հյուսվածքների համար։ Կենդանի օրգանիզմներում գտնվում է անօրգ․ միացությունների ձևով, հատկապես ոսկրերում (100-300 մգ/կգ) և ատամներում։
Ֆտորը մարդու և կենդանիների օրգանիզմ է ներմուծվում հիմնականում խմելու ջրի հետ (այն պետք է պարունակի 1-1,5 մգ/լ ֆտոր )։ Ֆտորի անբավարարության դեպքում առաջանում է ատամների փտում, ավելցուկի դեպքում՝ ֆլյուորոզ։ Ֆտորը խիստ թունավոր է։ Ֆտոր պարունակող պատրաստուկներն ՛օգտագործվում են որպես հակաուռուցքային նեյրոլեպտիկ, հակաընկճումային և նարկոտիկ միջոցներ։
Տես նաև
[խմբագրել | խմբագրել կոդը]Ծանոթագրություններ
[խմբագրել | խմբագրել կոդը]- ↑ «Фтор». Արխիվացված օրիգինալից 2013 թ․ մարտի 15-ին. Վերցված է 2013 թ․ մարտի 14-ին.
- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report)(անգլ.) // Pure and Applied Chemistry. — 2013. — Т. 85. — № 5. — С. 1047-1078. — ISSN 0033-4545. —
- ↑ Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9
- ↑ 4,0 4,1 Haynes, 2011, էջ 4.121
- ↑ Таблица Менделеева на сайте ИЮПАК
- ↑ Главным образом в эмали зубов
- ↑ Journal of Solid State Chemistry, Vol. 2, Issue 2, 1970, P. 225—227.
- ↑ J. Chem. Phys. 49, 1902 (1968)
- ↑ Гринвуд Н., Эрншо А. «Химия элементов» т. 2, М.: БИНОМ. Лаборатория знаний, 2008 стр. 147—148, 169 — химический синтез фтора
Գրականություն
[խմբագրել | խմբագրել կոդը]- Рысс И. Г. Химия фтора и его неорганических соединений. М. Госхимиздат, 1966 г. — 718 с.
- Некрасов Б. В. Основы общей химии. (издание третье, том 1) М. Химия, 1973 г. — 656 с.
- L. Pauling, I. Keaveny, and A.B. Robinson, J. Solid State Chem., 1970, 2, p. 225. անգլ.՝ {{{1}}} — Մարամասն ֆտորի բյուրեղային կառուցվածքի մասին
- Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente. Weinheim 1988, ISBN 3-527-26169-9, S. 1018–1022.
- Michael Binnewies, Menfred Jäckel, Helge Willner, Geoff Rayner-Canham: Allgemeine und Anorganische Chemie. Spektrum Akademischer Verlag, Heidelberg 2004, ISBN 3-8274-0208-5, S. 552, 556–557 575.
- Ralf Steudel: Chemie der Nichtmetalle. de Gruyter, Berlin 1998, ISBN 3-11-012322-3.
- Haynes, William M., ed. (2011). Handbook of Chemistry and Physics (92nd ed.). Boca Raton: CRC Press. ISBN 1-4398-5511-0.
{{cite book}}: CS1 սպաս․ ref duplicates default (link)
Արտաքին հղումներ
[խմբագրել | խմբագրել կոդը]- Информация о Перфторане
- Кровезаменитель Перфторан // Вестник РАН, 1997, том 67, N 11, с. 998—1013.
- chemie-master.de – Foto von flüssigem Fluor
- It's Elemental – Fluorine
- EnvironmentalChemistry.com – Fluorine
| Պարբերական աղյուսակ | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |













