Էլեկտրոլիզ

Էլեկտրոլիզ, ֆիզիկաքիմիական գործընթաց և էլեկտրական հոսանքով նյութի քայքայում։ Իոնները ստանում են ուղղորդված շարժում, երբ էլեկտրոլիտի լուծույթը կամ հալույթը տեղավորում են էլեկտրական դաշտում։ Դրական լիցքավորված իոնները՝ կատիոնները, շարժվում են դեպի բացասական[1] էլեկտրոդը՝ կաթոդը, իսկ անիոնները՝ դեպի դրական լիցք կրող էլեկտրոդը՝ անոդը։
Որպես իներտ էլեկտրոդներ, սովորաբար օգտագործվում են գրաֆիտից, պլատինից և չժանգոտվող պողպատից պատրաստված թիթեղներ։ Կաթոդն ունի ավելցուկային էլեկտրոդներ, որոնք շարունակ մատակարարվում են հաստատուն հոսանքի աղբյուրից, իսկ անոդը, ընդհակառակը, ունի էլեկտրոնային մեծ պակասորդ (դեֆիցիտ)։
Էլեկտրոլիզն իրականացնում են էլեկտրոլիզարար կոչվող տաշտակում, որը պարունակում է էլեկտրոլիտի լուծույթ կամ հալույթ, և որի մեջ տեղադրվում են հաստատուն հոսանքի աղբյուրին միացված էլեկտրոդներ։
Էլեկտրոլիզի համար չի պահանջվում հոսանքի մեծ լարում, բավարար է միայն մի քանի վոլտը, սակայն անհրաժեշտ է հոսանքի մեծ ուժ (ամպեր), քանի որ էլեկտրոլիզին մասնակցում են վիթխարի թվով էլեկտրոններ։ Էլեկտրոլիզն ունի մեծ կիրառություն մետաղարտադրությունում և քիմիական արդյունաբերության զանազան ճյուղերում։
Ֆարադեյի առաջին օրենք[խմբագրել | խմբագրել կոդը]
Ֆարադեյի I օրենքը հետևյալն է, անջատված նյութերի m զանգվածները համեմատական են էլեկտրոլիտով անցած q էլեկտրականության քանակին,
որտեղ k-ն տվյալ նյութի էլեկտրաքիմիական համարժեքն է։
Հետևություն Ֆարադեյի օրենքներից[խմբագրել | խմբագրել կոդը]
- (1)
- (2)
- (3)
- (4)
- , որտեղ z - նյութերի ատոմի (իոնի) վալենտականությունն է, e - լիցքավորված էլեկտրոնն է (5)
(2)-(5) բանաձևերը տեղադրելով (1) բանաձևի մեջ, կստացվի
որտեղ - Ֆարադեյի հաստատուն է։
Օրինակներ[խմբագրել | խմբագրել կոդը]
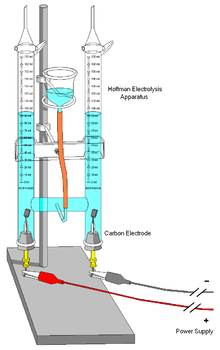
NaCl-ի հալույթի էլեկտրոլիզ[խմբագրել | խմբագրել կոդը]
Հալույթում աղը լրիվ տրոհվում, դիսոցվում է իոնների, այս անգամ՝ արդեն առանց ջրի մոլեկուլների մասնակցության։
Կերակրի աղը իոնական միացություն է, հալույթում ևս դիսոցված է իոնների։ Էլեկտրոլիզի ջերմաստիճանը մոտ 800 °C է.
Նատրիումի կատիոնը, որ զրկված է էլեկտրոնից, մոտենալով կաթոդին, վերցնում է այնտեղից էլեկտրոն և վերածվում ատոմային նատրիումի։ Նատրիումի կատիոնը վերականգնվում է՝ օքսիդացման աստիճանն փոքրանում է, և կաթոդի մոտ կուտակվում է մետաղական նատրիում
- K"Կաթոդ"(-) :
Կաթոդի վրա միշտ կատարվում է վերականգնման գործընթաց։ Քլորիդ իոնը, ընդհակառակը, ունի էլեկտրոնի ավելցուկ, և անոդին մոտենալիս վերջինս խլում է այդ էլեկտրոնն, ու տեղի է ունենում քլորիդ իոնի օքսիդացում։ Երկու ատոմ, միանալով իրար, առաջացնում են քլորի մոլեկուլ։ Անոդի մոտ անջատվում է քլոր գազը։
- A"Անոդ"(+) :,
Անոդի վրա միշտ կատարվում է օքսիդացման գործընթաց։
Կերակրի աղի հալույթի էլեկտրոլիզի ընդհանուր հավասարումն ունի այսպիսի տեսք.
Էլեկտրոլիտների, մասնավորապես աղերի ջրային լուծույթների էլեկտրոլիզը մի փոքր ավելի բարդ է, քանի որ էլեկտրոդային գործընթացներին կարող են մասնակից դառնալ ջրից գոյացած H+ և OH– իոնները կամ հենց ջրի մոլեկուլները։ Այս դեպքերում անհրաժեշտ է հաշվի առնել կաթոդային և անոդային գործընթացների օրինաչափությունները, որոնք կախված են լուծույթում առկա կատիոնների և անիոնների բնույթից։
Կաթոդային օրինաչափություններ[խմբագրել | խմբագրել կոդը]
- Եթե աղի մետաղի տեղը էլեկտրաքիմիական շարքում գտնվում է լիթիումից մինչև ալյումինը (ներառյալ), օրինակ՝ K, Na, Ca, ապա կաթոդի մոտ վերականգնվում է ոչ թե մետաղի կատիոնը, այլ ջուրը։
- Եթե աղի մետաղը ալյումինից հետո է՝ մինչև ջրածինը, օրինակ՝ Zn, Ni, Fe, ապա կաթոդի մոտ վերականգնվում է և՛ ջուրը, և՛ մետաղի կատիոնը։
- Եթե աղի մետաղը ջրածնից հետո է, օրինակ՝ Cu, Ag, ապա վերականգնվում է միայն մետաղը, իսկ ջրի հետ փոփոխություն տեղի չի ունենում։
Անոդային գործընթացներ[խմբագրել | խմբագրել կոդը]
- Եթե աղի անիոնը անթթվածին թթվից է, օրինակ՝ Cl–, Br–, Ι–, S2–, ապա անոդի մոտ օքսիդանում է անիոնը, իսկ ջուրը մնում է անփոփոխ։
- Եթե անիոնը թթվածնավոր թթվից է, օրինակ՝ SO2−4, NO−3, CO2−3, PO3−4,
ապա օքսիդանում է միայն ջուրը, իսկ անիոնը մնում է անփոփոխ։
NaCl–ի ջրային լուծույթի էլեկտրոլիզ[խմբագրել | խմբագրել կոդը]
Ջրային լուծույթում, նատրիումի և քլորի իոններից բացի, կան նաև ջրի մոլեկուլներ.
Չնայած նատրիումի իոնները ձգվում և հավաքվում են կաթոդի մոտ, սակայն կաթոդից էլեկտրոն վերցնում են միայն ջրի մոլեկուլները։ Այսինքն՝ վերականգնվում է ջուրը՝ H2O։ Նկատի ունենալով ջրի մեջ ջրածնի (+1) և թթվածնի (–2) օքսիդացման աստիճանները՝ կարելի է եզրակացնել, որ վերականգնվելու հնարավորություն ունի միայն ջրածինը։ Օքսիդացման աստիճանը կարող է նվազել մինչև զրո (0)։ Ընդ որում՝ փոփոխությունը կատարվում է ջրածնի միայն մեկ ատոմի հետ (HOH), իսկ լուծույթում աստիճանաբար ավելանում են հիդրօքսիդ՝ OH–, իոնները.
- K"Կաթոդ"(-) :
Այս գործընթացը անվանում են «ջրի կաթոդային վերականգնում».
Անոդի վրա օքսիդանում են քլորիդ իոնները, իսկ ջրի մոլեկուլների հետ փոփոխություն տեղի չի ունենում։
- A"Անոդ"(+) ::
Կերակրի աղի ջրային լուծույթի էլեկտրոլիզի դեպքում ծախսվում է և՛ աղը, և՛ ջուրը։ Անջատվում են ջրածին և քլոր գազերը, իսկ լուծույթը հարստանում է Na+ և OH– իոններով, այսինքն՝ նատրիումի հիդրօքսիդով։ Գումարային հավասարումն ունի հետևյալ տեսքը.
Այս ճանապարհով արդյունաբերության մեջ ստանում են ալկալիներ՝ NaOH, KOH, քլոր։
Նշանակություն[խմբագրել | խմբագրել կոդը]
Հայաստանում գոյություն ունի պղնձի արտադրություն, որում օգտագործվում են հրամետալուրգիան և էլեկտրոլիզը։
Աղերի հալույթների և ջրային լուծույթների էլեկտրոլիզը լայնորեն օգտագործվում է ամենատարբեր նյութեր՝ մետաղներ, ալկալիներ, թթուներ, ջրածին, թթվածին, քլոր ստանալու, ինչպես նաև զանազան իրեր և առարկաներ պղնձապատելու, արծաթապատելու, ոսկեզօծելու համար։
Օրինակ՝ թեյնիկները, մարդատար ավտոմեքենաների որոշ մետաղյա մասերը նիկելապատելու համար դրանք մտցնում են նիկելի աղի լուծույթ պարունակող էլեկտրոլիզային տաշտակի մեջ, միացնում են կաթոդին և կատարում էլեկտրոլիզ։ Վերականգնվող մետաղական նիկելը բարակ շերտով նստում է որպես կաթոդ ծառայող այդ իրերի վրա։ Նիկելապատված մետաղյա իրերը ոչ միայն գեղեցիկ տեսք ունեն, այլև ավելի կայուն են զանազան ֆիզիկական և քիմիական ազդակների նկատմամբ։
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Обратное обозначение знака катода и анода встречается в литературе при описании гальванических элементов
Գրականություն[խմբագրել | խմբագրել կոդը]
- Handbuch der experimentellen Chemie Sekundarbereich II, Band 6։ Elektrochemie, Aulis Verlag Deubner GmbH & Co. KG
- Ullmann Encyklopädie der technischen Chemie 3. Auflage, Band 6, S. 253–304; 4. Auflage, Band 3, S. 262–298, 5. Auflage, Band A9, S. 220 ff..
- Gerd Wedler, Lehrbuch der Physikalischen Chemie, Verlag Chemie 1982, ISBN 3-527-25880-9, S. 172–212, S. 405–445, S. 821–836
- Udo R. Kunze, Grundlagen der quantitativen Analyse, Georg Thieme Verlag, Oktober 1980, S. 169–171.
- Carl H. Hamann, Wolf Vielstich։ Elektrochemie, 4. Auflage, WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim 2005, ISBN 3-527-31068-1 .
- B. Speiser։ Elektroanalytische Methoden I: Elektrodenreaktionen und Chronoamperometrie, in։ Chemie in unserer Zeit 1981, 15, 21–26; .
- W.-D. Luz, E. Zirngiebel։ Die Zukunft der Elektrochemie, Einige Betrachtungen aus der Sicht der Chemie, in։ Chemie in unserer Zeit, 1989, 23, 151–160; .
Արտաքին հղումներ[խմբագրել | խմբագրել կոդը]
- Էլեկտրոլիզի ժամանակ առաջացող գործընթացներ
- «Էլեկտրոլիզ» Հոդված (Քիմիական հանրագիտարան)
- Էլեկտրոդիալիզ
- Էլեկտրոֆլոտացիա Արխիվացված 2015-02-15 Wayback Machine
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 4, էջ 29)։ |




















