Ջերմաստիճան
Ջերմաստիճանը տաքի և սառի կամ ջերմության[1] չափողական մեծություն է։ Սառը մարմինները ունեն ցածր ջերմաստիճան, տաք մարմինները ունեն ավելի բարձր ջերմաստիճան։ Ջերմությունը բարձր ջերմաստիճան ունեցող մարմնից ինքնաբերաբար անցնում է ցածր ջերմաստիճան ունեցող մարմնին, ինչի հետևանքով ջերմաստիճանների տարբերությունը փոքրանում է, և վերջիվերջո, վերանում։ Այս դեպքում ասում են, որ մարմինները գտնվում են ջերմային հավասարակշռության վիճակում։
Որևէ մարմնի ջերմաստիճանը քառակուսային օրենքով կախված է այդ մարմինը կազմող մասնիկների միջին արագությունից, այսինքն՝ համեմատական է մասնիկների միջին կինետիկ էներգիային։ Ձևականորեն ջերմաստիճանը որոշվում է որպես ներքին էներգիայի ածանցյալ ըստ էնտրոպիայի։
Ջերմաստիճանը չափվում է ջերմաչափերով, որոնք կարող են սանդղավորված լինել տարբեր ջերմաստիճանային սանդղակներով։
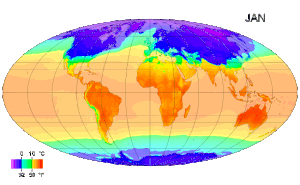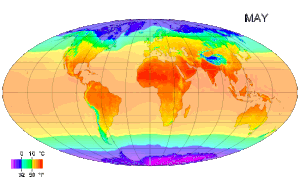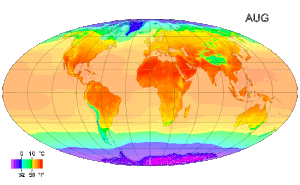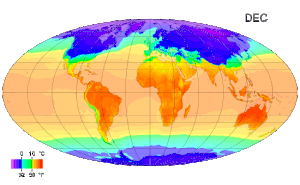
Ջերմաստիճանը կարևոր դեր է խաղում բնական գիտությունների մի շարք բնագավառներում, որոնցից են ֆիզիկան, աշխարհագրությունը, քիմիան, կենսաբանությունը և մթնոլորտային գիտությունները։ )
Կիրառությունը գիտության մեջ[խմբագրել | խմբագրել կոդը]
Նյութի բազմաթիվ ֆիզիկական հատկություններ, ներառյալ հեղուկ, պինդ, գազային կամ պլազմային փուլերը, խտությունը, լուծելիությունը, հագեցած գոլորշին, էլեկտրահաղորդականությունը և այլն կախված են ջերմաստիճանից։ Ջերմաստիճանը կարևոր դեր է խաղում նաև քիմիական ռեակցիաների մեջ։ Դա է պատճառը, որ մարդու մարմնի մեխանիզմները բնականոն գործում են 310 Կ ջերմաստիճանում, մինչդեռ ընդամենը մի քանի աստիճանով բարձր ջերմաստիճանները կարող են առաջ բերել ծանր հետևանքների հանգեցնող վտանգավոր ռեակցիաներ։ Ջերմաստիճանով է որոշվում նաև մարմինների մակերևույթից առաքվող ջերմային ճառագայթումը։ Այս երևույթի քաջ հայտնի կիրառություններից է շիկացման լամպը, որում վոլֆրամի թելիկը էլեկտրականության օգնությամբ տաքացվում է մինչև որոշակի ջերմաստիճան, որի դեպքում սկսում է ճառագայթել տեսանելի լույս։
Աստղաֆիզիկա[խմբագրել | խմբագրել կոդը]
Ջերմաստիճան աստղաֆիզիկայում, երկնային մարմինների և, ընդհանրապես, միջավայրի ջերմային վիճակը և ճառագայթումը բնորոշող մեծություն։ Երկնային մարմինների ջերմաստիճանը որոշվում է դրանց ճառագայթումն ուսումնասիրելու միջոցով։
Ենթադրվում է, որ միջավայրը գտնվում է թերմոդինամիկական հավասարակշռության մեջ, որի համար կիրառելի են բացարձակ սև մարմնի ճառագայթման օրենքները։ Քանի որ երկնային օբյեկտներում (աստղեր, միգամածություններ և այլն) գոյություն ունեցող պայմանները խիստ տարբեր են թերմոդինամիկական հավասարակշռությունից, ապա տարբեր մեթոդներով ջերմաստիճանի որոշման արդյունքները կարող են զգալի չափով տարբերվել։ Աստղաֆիզիկայում օգտագործվում են ջերմաստիճանների հետևյալ տեսակները։ Էֆեկտիվ ջերմաստիճան, այնպիսի բացարձակ սև մարմնի ջերմաստիճան, որի յուրաքանչյուր 1 ԱէԲ ամբողջ սպեկտրում ճառագայթում է տվյալ մարմնի 1 սմ քառակուսիից ճառագայթած էներգիայի հոսքին հավասար էներգիա։
Պայծառային ջերմաստիճանը բնորոշվում է նույն ձևով, երբ հոսքը վերաբերում է սպեկտրում տվյալ ալիքի երկարությանը։ Այս ջերմաստիճան հաճախ օգտագործվում է ռադիոաստղագիտությունում։ Գոլնային ջերմաստիճան վերաբերում է այն դեպքին, երբ բացարձակ սև մարմնի և տվյալ մարմնի սպեկտրների միևնույն հատվածներում էներգիաների հարաբերական բաշխումներն համընկնում են։
Կինետիկ ջերմաստիճանը համեմատական է մեկ մասնիկի միջին կինետիկ էներգիային, մասնավոր դեպքում, երբ մասնիկներն էլեկտրոններ կամ իոններ են, ջերմաստիճան կոչվում է էլեկտրոնային կամ իոնային։ Գրգռման ջերմաստիճանը պարամետր է, որը բնութագրում է ատոմների բաշխումն ըստ գրգռման վիճակների (էլեկտրոնային էներգետիկական մակարդակների «բնակվածություն»)։ Իոնացման ջերմաստիճանը՝ նյութի իոնացման աստիճանը բնութագրող պարամետր է, որը որոշվում է ըստ սպեկտրային գծերի հարաբերական ինտենսիվության։
Երկնային մարմինների ջերմաստիճանների որոշման եղանակները կիրառվում են ըստ տվյալ միջավայրի ֆիզիկական հատկությունների։ Այդ պատճառով աստղերի և, օրինակ, նոսր գազային միգամածությունների ջերմաստիճանների որոշման եղանակները տարբեր են[2]։
Թերմոդինամիկական մոտեցում[խմբագրել | խմբագրել կոդը]

Ջերմաստիճանը թերմոդինամիկայում ուսումնասիրվող հիմնական մեծություններից է։ Թերմոդինամիկան հետազոտում է ջերմության և աշխատանքի կապը՝ օգտագործելով հատուկ սանդղակ, որը կոչվում է բացարձակ ջերմաստիճան։ Թերմոդինամիկական տերմիններով ջերմաստիճանը մակրոսկոպիկ, ինտենսիվ փոփոխական է, քանի որ կախված է մարմինը կազմող մասնիկներից՝ լինեն դրանք ատոմներ, մոլեկուլներ թե էլեկտրոններ։ Այլ կերպ ասած՝թերմոդինամիկական հավասարակշռության մեջ գտնվող մարմնի ջերմաստիճանը նույնն է մարմինը կազմող բոլոր մասնիկների կամ մասերի համար և հավասար չէ դրանց առանձին ջերմաստիճանների գումարին։
Վիճակագրական մեխանիկայի մոտեցում[խմբագրել | խմբագրել կոդը]
Վիճակագրական մեխանիկան տալիս է ջերմաստիճանի միկրոսկոպիկ մեկնաբանությունը՝ ընդունելով, որ մակրոսկոպիկ համակարգը կազմված է տարբեր տիպի մասնիկներից (օրինակ՝ ատոմներից և իոններից) և որ նույն տեսակի մասնիկները նման են միմյանց։ Այն բացատրում է մակրոսկոպիկ երևույթը մոլեկուլների և իոնների մեխանիկայի հասկացություններով և կինետիկ տեսությամբ։ Վիճակագրական մեխանիկայում մասնիկների փոխարեն օգտագործվում են նրանց ազատության աստիճանները։
Մոլեկուլային մակարդակով ջերմաստիճանը նյութը կազմող մասնիկների շարժման հետևանքն է։ Շարժվող մասնիկներն օժտված են կինետիկ էներգիայով։ Շարժման և կինետիկ էներգիայի աճի հետ բարձրանում է ջերմաստիճանը։ Շարժում կարող է լինել մասնիկների համընթաց շարժումը, մոլեկուլային տատանումներով պայմանավորված մասնիկի էներգիան կամ էլեկտրոնի գրգռումը էներգիական մակարդակում։ Չնայած համընթաց ջերմային շարժումները ուղղակիորեն չափելու համար անհրաժեշտ են հատուկ լաբորատորային սարքավորումներ, հեղուկում գտնվող փոքր մասնիկների հետ ատոմների կամ մոլեկուլների ջերմային բախումների հետևանքով առաջացած Բրոունյան շարժումը հնարավոր է տեսնել սովորական միկրոսկոպով։ Ատոմների ջերմային շարժումները շատ արագ են, և դրանք նկատելու համար անհրաժեշտ են բացարձակ զրոյին մոտ ջերմաստիճաններ։
Մոլեկուլը (օրինակ, թթվածինը՝ O2) ավելի շատ ազատության աստիճաններ ունի քան ատոմը և մասնակցում է ինչպես համընթաց, այնպես էլ պտտական և տատանողական շարժումների։ Տաքանալու արդյունքում ջերմաստիճանը աճում է, քանի որ աճում է մոլեկուլների համընթաց շարժման միջին էներգիան։ Աճում է նաև տատանողական և պտտական մոդերի էներգիան։ Ուստի երկատոմ գազի ջերմաստիճանը բարձրացնելու համար կպահանջվի ավելի շատ էներգիա, այսինքն՝ երկատոմ գազն ավելի մեծ ջերմունակություն ունի, քան միատոմ գազը։
Սառեցման պրոցեսը համարժեք է համակարգից ջերմային էներգիան վերցնելուն։ Եթե այլևս հնարավոր չէ էներգիա վերցնել, ուրեմն համակարգը գտնվում է բացարձակ զրոյում, որին հնարավոր չէ հասնել փորձնականորեն։ Բացարձակ զրոն թերմոդինամիկական ջերմաստիճանային սանդղակի (բացարձակ ջերմաստիճան) զրոն է։ Եթե հնարավոր լինել համակարգը սառեցնել մինչև բացարձակ զրո, համակարգը կազմող բոլոր մասնիկների շարժումը կդադարեր և համակարգը կգտնվեր դասական իմաստով կատարյալ դադարի վիճակում։ Սակայն քվանտամեխանիկական նկարագրությամբ նյութը նույնիսկ բացարձակ զրոյում օժտված է զրոյական տատանումների էներգիայով` անորոշությունների սկզբունքի համաձայն։
Ջերմաստիճանի չափում[խմբագրել | խմբագրել կոդը]

Թերմոդինամիկական ջերմաստիճանի չափման համար ընտրվում է ջերմաչափային նյութի որևէ պարամետր, որի չափումը միարժեքորեն կապվում է ջերմաստիճանի չափման հետ։ Թերմոդինամիկական ջերմաչափի դասական օրինակ է գազային ջերմաչափը, որում ջերմաստիճանը որոշվում է հաստատուն ծավալում գտնվող գազի ճնշումը չափելու միջոցով։ Կիրառվում են նաև ճառագայթային, աղմուկային, ակուստիկական ջերմաչափեր։ Թերմոդինամիկական ջերմաչափը շատ բարդ սարք է, որը հնարավոր չէ օգտագործել գործնական նպատակների համար։ Այդ պատճառով չափումների մեծ մասն իրականացվում է գործնական ջերմաչափերի միջոցով, որոնք երկրորդական են, քանի որ չեն կարող նյութի որևէ հատկություն անմիջականորեն կապել ջերմաստիճանի հետ։
Որևէ մարմնի ջերմաստիճանը չափելու համար այն պետք է կոնտակտի մեջ դնել «փորձող» մարմնի՝ ջերմաչափի հետ։ Ջերմաչափի զանգվածը չպետք է մեծ լինի, հակառակ դեպքում զանգվածեղ ջերմաչափը կփոխի այն մարմնի ջերմաստիճանը, որի հետ գտնվում է ջերմային կոնտակտի մեջ։ Ջերմաչափը ֆիքսում է իր սեփական ջերմաստիճանը, որը իր հետ թերմոդինամիկական հավասարակշռության վիճակի մեջ գտնվող մարմնի ջերմաստիճանն է։
Ջերմաստիճանի չափման միջոցները հաճախ սանդղավորվում են ըստ Ցելսիուսի կամ Ֆարենհայտի սանդղակների։
Ամենաճշգրիտ գործնականում կիրառվող ջերմաչափը պլատինային դիմադրության ջերմաչափն է[3]։
Ջերմաստիճանի չափման նորագույն եղանակները հիմնված են լազերային ճառագայթման պարամետրերի չափումների վրա[4]։
Ջերմաստիճանի չափման միավորներ և սանդղակներ[խմբագրել | խմբագրել կոդը]
Աշխարհում ամենալայն կիրառությունն ունի Ցելսիուսի սանդղակը (°C)։ Այն ունի նույն աստիճանային բաժանումները, ինչ և գիտնականների կողմից օգտագործվող Կելվինի սանդղակը։ Վերջինիս զրոն համապատասխանում է Ցելսիուսի սանդղակով ջրի սառչելու ջերմաստիճանին (մեկ մթնոլորտ ճնշման տակ)` 0 ° C = 273,15 Կ[5]։ Միացյալ Նահանգներում օգտագործվում է Ֆարենհայտի սանդղակը, ըստ որի ջրի սառչելու ջերմաստիճանը 32 °F է, եռմանը` 212 °F (մեկ մթնոլորտ ճնշման տակ)։ Գիտական ջերմաստիճանային չափումների համար Միավորների միջազգային համակարգը (ՄՀ) թերմոդինամիկական ջերմաստիճանի սանդղակի միավորը որոշելու համար որպես կողմնորոշիչ կետ ընդունում է ջրի եռակի կետը։ Այս ընտրությունը հիմնավորված է նրանով, որ ի տարբերություն սառչելու և եռման ջերմաստիճանների, եռակի կետում ջերմաստիճանը անկախ է ճնշումից։ Պատմական պատճառներով ջրի եռակի կետը համարվում է 273,16 միավոր։ Այդ միավորը կոչվում է կելվին (Կ)` սանդղակը հորինող շոտլանդացի ֆիզիկոս Կելվինի պատվին։
Բացարձակ զրոն սահմանվում է ճշգրիտ 0 Կելվին, որը հավասար է −273,15 °C կամ −459,68 °F:
Քանի որ ջերմաստիճանը մոլեկուլների կինետիկ էներգիան է, ավելի բնական կլիներ այն չափել էներգիական միավորներով (ՄՀ միավորներով` Ջոուլներով)։ Սակայն ջերմաստիճանը սկսել են չափել մոլեկուլային-կինետիկական տեսության ստեղծումից շատ առաջ, այդ պատճառով գործնական սանդղակները ջերմաստիճանը չափում են պայմանական միավորով՝ աստիճանով։
Կելվինի սանդղակ[խմբագրել | խմբագրել կոդը]
Բացարձակ ջերմաստիճանի գաղափարը առաջ է քաշել Վ. Կելվինը, ուստի բացարձակ ջերմաստիճանի սանդղակը կոչվում է Կելվինի սանդղակ կամ թերմոդինամիկական ջերմաստիճանային սանդղակ։ Այդ սանդղակի միավորը Կելվինն է (Կ)։
Բացարձակ ջերմաստիճանային սանդղակի ստորին սահմանը բացարձակ զրոն է՝ ամենացածր հնարավոր ջերմաստիճանը, որի դեպքում հնարավոր չէ նյութից ջերմային էներգիա վերցնել։
Ըստ սահմանման բացարձակ զրոն 0 Կ է, որը ճշգրիտ հավասար է −273,15 °C:
Կելվինի սանդղակի հաշվարկման սկիզբ ընդունված է բացարձակ զրոն։
Կենցաղում օգտագործվող Ցելսիուսի և Ֆարենհայտի սանդղակները բացարձակ չեն, այդ պատճառով հարմար չեն որոշակի պայմաններում ընթացող փորձերում օգտագործելու համար, երբ ջերմաստիճանը իջնում է ջրի սառման կետից ներքև և հարկ է լինում այն արտահայտել բացասական թվով։ Այդ պատճառով կիրառվում են ջերմաստիճանի բացարձակ սանդղակները։
Դրանցից մեկը Ռենկինի սանդղակն է (չափման միավորը՝ °Ռ, ), մյուսը՝ բացարձակ ջերմաստիճանային (Կելվինի) սանդղակը։ Երկուսի համար էլ հաշվարկի սկիզբը զրոն է, միայն թե Կելվինի սանդղակի մեկ բաժանումը հավասար է Ցելսիուսի սանդղակի մեկ բաժանմանը, իսկ Ռենկինի սանդղակինը՝ համապատասխանաբար Ֆարենհայտի սանդղակի մեկ բաժանմանը։ Ջրի սառչելու ջերմաստիճանը ստանդարտ մթնոլորտային ճնշման դեպքում համապատասխանում է 273,15 Կ, 0 °C, 32 °F:
Կելվինի սանդղակի մասշտաբը կապված է ջրի եռակի կետին (273,16 Կ), ընդ որում Բոլցմանի հաստատունը կախված է նրանից։ Դա խնդիրներ է ստեղծում բորձոր ջերմաստիճանների չափման ճշտության մեջ։ Ներկայումս քննարկվում է կելվինի՝ եռակի կետին կապելու փոխարեն նոր սահմանում տալու և Բոլցմանի հաստատունը ֆիքսելու հնարավորությունը[6]։
Ցելսիուսի սանդղակ[խմբագրել | խմբագրել կոդը]
Ցելսիուսի սանդղակն օգտագործվում է տեխնիկայում, կենցաղում, բժշկության և եղանակի տեսության մեջ։ Այս սանդղակով ջերի եռակի կետի ջերմաստիճանը հավասար է 0,008 °C, և հետևաբար, ջրի սառչելու կետը 1 մթն ճնշման դեպքում 0 °C է։ Ներկայումս Ցելսիուսի սանդղակը սահմանում են Կելվինի սանդղակի միջոցով. Ցելսիուսի սանդղակի մեկ բաժանումը հավասար է Կելվինի սանդղակի մեկ բաժանմանը՝ t(°С) = Т(Կ) - 273,15։ Ուստի ջրի եռման կետը, որը սկզբում Ցելսիուսն ընտրել էր որպես հաշվարկի հիմք՝ համարելով 100 °C, այժմ կորցրել է իր արժեքը և ըստ ժամանակակից հաշվարկների, ջրի եռման ջերմաստիճանը նորմալ մթնոլորտային ճնշման դեպքում 99,975 °C է։ Ցելսիուսի սանդղակը գործնականում շատ հարմար է, քանի որ ջուրը մեր մոլորակի վրա շատ տարածված է և կյանքը նրանով է պայմանավորված։ Ցելսիուսի զրոն հատուկ կետ է օդերևութաբանության մեջ, քանի որ կապված է մթնոլորտային ջրի սառչելու հետ։ Այս սանդղակն առաջարկել է Անդերս Ցելսիուսը 1742 թ.:
Ֆարենհայտի սանդղակ[խմբագրել | խմբագրել կոդը]
Անգլիայիում և ԱՄՆ-ում կիրառվում է Ֆարենհայտի սանդղակը։ Ցելսիուսի սանդղակի զրոն համապատասխանում է Ֆարենհայտի սանդղակի 32 աստիճանին, իսկ 100 աստիճանը՝ 212 աստիճանին։ Կապը Ֆարենհայտի և Ցելսիուսի սանդղակների ջերմաստիճանների միջև տրվում է հետևյալ առնչությամբ՝ t °С = 5/9 (t °F - 32), t °F = 9/5 t °С + 32: Առաջարկել է Գ. Ֆարենհայտը 1724 թ.:
Ռեոմյուրի սանդղակ[խմբագրել | խմբագրել կոդը]
Առաջարկել է 1730 թ. Ռենե Անտուան Ռեոմյուրը՝ նկարագրելով իր հայտնագործած սպիրտային ջերմաչափը։
Միավորը աստիճան Ռեոմյուրն է (°R), 1 °R համապատասխանում է որպես հիմնական կետեր ընտրված սառույցի հալման (0 °R) և ջրի եռման (80 °R) միջև ընկած ջերմաստիճանային միջակայքի 1/80 մասին՝ 1 °R = 1,25 °C:
Ներկայումս այս սանդղակը չի օգտագործվում։
Կապը տարբեր սանդղակների միջև[խմբագրել | խմբագրել կոդը]
Աղյուսակում պատկերված են Ցելսիուսի և այլ սանդղակների ջերմաստիճանների միջև կապ հաստատող առնչությունները.
| Ցելսիուսով | Ցելսիուս | |
|---|---|---|
| Ֆարենհայտ (°F) | [°F] = [°C] × 9⁄5 + 32 | [°C] = ([°F] − 32) × 5⁄9 |
| Կելվին (K) | [K] = [°C] + 273,15 | [°C] = [K] − 273,15 |
| Ռենկին | [°R] = ([°C] + 273,15) × 9⁄5 | [°C] = ([°R] − 491,67) × 5⁄9 |
| Դելիլ | [°De] = (100 − [°C]) × 3⁄2 | [°C] = 100 − [°De] × 2⁄3 |
| Նյուտոն | [°N] = [°C] × 33⁄100 | [°C] = [°N] × 100⁄33 |
| Ռեոմյուր | [°Ré] = [°C] × 4⁄5 | [°C] = [°Ré] × 5⁄4 |
| Ռոմեր | [°Rø] = [°C] × 21⁄40 + 7,5 | [°C] = ([°Rø] − 7,5) × 40⁄21 |
Ջերմային շարժման էներգիան բացարձակ զրոյում[խմբագրել | խմբագրել կոդը]
Երբ նյութը սառչում է, ջերմային էներգիայի շատ ձևեր և դրանց հետ կապված էֆեկտներ մեծությամբ փոխվում են։ Նյութը պակաս կարգավորված վիճակից անցում է կատարում ավելի կարգավորված վիճակի։
Բացարձակ զրոյի ժամանակակից հասկացությունը բացարձակ հանգստի հասկացությունը չէ, ընդհակառակը, բացարձակ զրոյում կարող է լինել շարժում և կա, սակայն դա կատարյալ կարգի վիճակն է։
Պ. Լ. Կապիցա (Հեղուկ հելիումի հատկությունները)
Գազը վերածվում է հեղուկի, ապա՝ բյուրեղանում՝ դառնալով պինդ մարմին (հելիումը նույնիսկ բացարձակ զրոյում մնում է հեղուկ վիճակում՝ մթնորորտային ճնշման պայմաններում)։ Ատոմների և մոլեկուլների շարժումը դանդաղում է, կինետիկ էներգիան նվազում է։ Մետաղների մեծ մասի դիմադրությունը ընկնում է։ Նույնիսկ բացարձակ զրոյում հաղորդականության էլեկտրոնը ատոմների միջև շարժվում է ֆերմիի կարգի արագությամբ (1×106 մ/վ)։
Ջերմաստիճանը, որի դեպքում նյութի մասնիկները միայն քվանտամեխանիկական շարժման շնորհիվ դեռևս գտնվում են շարժման մեջ, բացարձակ զրո ջերմաստիճանն է (Т=0 Կ)։
Բացարձակ զրո ջերմաստիճանին հնարավոր չէ հասել։ Ամենացածր ջերմաստիճանը, որ ստացվել է 2003 թ. նատրիումի ատոմների Բոզե-Այնշտայնի կոնդենսացիայի միջոցով, 450±80×10−12 Կ է։ Ընդ որում ջերմային ճառագայթման բարձրակետը համապատասխանում է մոտ 6400 կմ ալիքի երկարությանը, ինչը մոտավորապես հավասար է Երկրի շառավղին։
Ջերմաստիճան և ճառագայթում[խմբագրել | խմբագրել կոդը]
Մարմնի ճառագայթման էներգիան համեմատական է ջերմաստիճանի չորս աստիճանին։ Օրինակ, 300Կ ջերմաստիճանի դեպքում մեկ քառակուսի մակերեսից ճառագայթվում է մինչև 450 վատտ էներգիա։ Դրանով է բացատրվում գիշերվա ընթացքում Երկրի մակերևույթի սառչելը շրջակա օդից ավելի ցածր ջերմաստիճաններ։ Բացարձակ սև մարմնի ճառագայթման էներգիան նկարագրվում է Ստեֆան-Բոլցմանի օրենքով։
Ուշագրավ ջերմաստիճաններ[խմբագրել | խմբագրել կոդը]
| Ջերմաստիճան | Սև մարմնի ճառագայթման ալիքի երկարության[7] պիկը | ||
|---|---|---|---|
| Կելվին | Ցելսիուս | ||
| Բացարձակ զրո (ըստ ճշգրիտ սահմանման) |
0 K | −273,15 °C | որոշված չէ |
| Ամենասառը ջերմաստիճանը[8] | 100 պԿ | −273,149 999 999 900 °C | 29 000 կմ |
| Բոզե-Այնշտայնի կոնդենսատ[9] |
450 պԿ | −273,149 999 999 55 °C | 6 400 կմ |
| Մեկ միլիկելվին (ըստ ճշգրիտ սահմանման) |
0,001 Կ | −273,149 °C | 2,897 77 մ ( FM տիրույթ)[10] |
| Ջրի եռակի կետ (ըստ ճշգրիտ սահմանման) |
273,16 Կ | 0,01 °C | 10 608,3 նմ ( երկար ինֆրակարմիր ալիքներ) |
| Ջրի եռման կետ | 373,1339 Կ | 99,9839 °C | 7 766,03 նմ (միջին ինֆրակարմիր տիրույթ) |
| Շիկացման լամպ | 2500 Կ | ≈2 200 °C | 1 160 նմ (մոտիկ ինֆրակարմիր) |
| Արեգակի մակերևույթ[11] | 5,778 Կ | 5 505 °C | 501,5 նմ (կանաչ և կապույտ լույս) |
| Կայծակ | 28 կԿ | 28 000 °C | 100 նմ (հեռու ուլտրակարմիր լույս) |
| Արեգակի միջուկ | 16 ՄԿ | 16 միլիոն °C | 0,18 նմ (ռենտգենյան ճառագայթներ) |
| Միջուկային զենք (պիկի ջերմաստիճանը)[12] |
350 ՄԿ | 350 միլիոն °C | 8,3×10−3 նմ (գամմա-ճառագայթներ) |
| Սանդիայի ազգային լաբորատորիա Z մեքենա[13] |
2 ԳԿ | 2 միլիոն °C | 1,4×10−3 նմ (գամմա ճառագայթներ) |
| Մեծ զանգվածով աստղի միջուկը վերջին օրերին[14] |
3 ԳԿ | 3 միլիոն °C | 1×10−3 նմ (գամմա-ճառագայթներ) |
| Կրկնակի նեյտրոնային աստղերով համակարգեր[15] |
350 ԳԿ | 350 միլիոն °C | 8×10−6 նմ (գամմա-ճառագայթներ) |
| Ռելյատիվիստական ծանր իոնային կոլայդեր[16] |
1 ՏԿ | 1 տրիլիոն °C | 3×10−6 նմ (գամմա-ճառագայթներ) |
| Տիեզերքը Մեծ պայթյունից 5,391×10−44 վ հետո |
1,417×1032 Կ | 1,417×1032 °C | 1,616×10−26 նմ (Պլանկի երկարություն)[17] |
Տես նաև[խմբագրել | խմբագրել կոդը]
- Ջերմաչափ
- Բացասական ջերմաստիճան
- Պլանկի ջերմաստիճան
- Ֆարենհայտի սանդղակ
- Ջերմային ճառագայթում
- Ցելսիուսի աստիճան (չափման միավոր)
- Բացարձակ զրո
- Զրոյական տատանումների էներգիա
- Ջերմաստիճան (աստղաֆիզիկա)
- Էֆեկտիվ ջերմաստիճան
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Temperature measure & Sensor Technology (2019).
- ↑ Համբարձումյան, Վիկտոր, ed. (1983). «ՋԵՐՄԱՍՏԻՃԱՆ աստղաֆիզիկայում». Հայկական սովետական հանրագիտարան. Vol. 9. Երևան: Հայ սովետական հանրագիտարան հրատարակչություն. Վերցված է 2016 թ․ հունիսի 2-ին.
- ↑ Պլատինային դիմադրության ջերմաչափ
- ↑ Լազերային ջերմաստիճանային չափումներ
- ↑ Պատմականորեն Ցելսիուսի սանդղակը մաքուր փորձնական ջերմաստիճանային սանդղակ է, որը սահմանվել է միայն ըստ ջրի սառչելու և եռման կետերի։ Միավորների միջազգային համակարգում կելվինի ընդգրկվելուց հետո դրա սահմանումը սկսեցին տալ ըստ Կելվինի սանդղակի համապատասխան կետերի
- ↑ Կելվինի նոր սահմանման մշակումը
- ↑ Բերված արժեքները հավասարակշռության մեջ գտնվող սև մարմնի համար են։ CODATA 2006-ը բաշխման օրենքի b հաստատունի համար առաջարկում է 2,8977685(51)×10-3մԿ։
- ↑ «Ցածր ջերմաստիճանների համաշխարհային ռեկորդը». Վերցված է 2009 թ․ մայիսի 5-ին.
- ↑ Բոզե-Այնշտայնի կոնդենսատի ջերմաստիճանի 450 ±80 պԿ արժեքը գրանցվել է 2003 թ. Մասաչուսետսի տեխնոլոգիական համալսարանում, նատրիումի ատոմների համար։
- ↑ 2,897 77 ալիքի երկարությամբ ճառագայթման պիկի հաճախությունը 103,456 ՄՀց է։
- ↑ Չափումներն իրականացվել են 2002 թ. ±3 կելվին ճշտությամբ։ 1989 measurement տալիս է 5 777,0±2,5 Կ արժեքը։ Հղում. Արևի նկարագրությունը Արխիվացված 2008-03-07 Wayback Machine :
- ↑ The 350 ՄԿ ջրածնային ռումբի ջերմամիջուկային վառելիքի այրման առավելագույն ջերմաստիճանն է։ Ատոմային ռումբին համապատասխանում է 50-ից 100 ՄԿ տիրույթը։ Հղում. Միջուկային զենքի ՀՏՀ, 3.2.5 Նյութը բարձր ջերմաստիճաններում Համապատասխան էջի հղումը ։ Տվյալները բերված են հանրության համար բաց աղբյուրներից։
- ↑ «Տես». Արխիվացված է օրիգինալից 2010 թ․ մայիսի 30-ին. Վերցված է 2012 թ․ հունիսի 1-ին.
- ↑ Տես Աստղի էվոլյուցիան Հավելյալ հղումներ` [1] Արխիվացված 2013-04-11 Wayback Machine,[2] Արխիվացված 2011-08-14 Wayback Machine
- ↑ Տես Ներյտրոնային աստղերի տորոիդային ձևավորումների և կարճ գամմա-ճառագայթների շուրջ, Ամփոփ տեքստ.
- ↑ Տես Փյունիկ Relativistic Heavy Ion Collider Brookhaven National Laboratory
- ↑ Պլանկի հաճախությունը 1,85487(14) ×1043Հց է (փոխկապակցված է Պլանկի ժամանակի հետ)։ Պլանկի հաճախությամբ ֆոտոնները ունեն Պլանկի ալիքի երկարություն։ 1,41679 (11) ×1032 Կ Պլանկի ջերմաստիճանը համապատասխանության մեջ է b /T = λmax հաշված 2,04531(16) ×10-26 նմ ալիքի երկարությանը։
| Այս հոդվածն ընտրվել է Հայերեն Վիքիպեդիայի օրվա հոդված: |

