Տրանսպլանտատի մերժում
| Տրանսպլանտատի մերժում | |
|---|---|
 | |
| Բժշկական մասնագիտություն | Տրանսպլանտոլոգիա |
| ՀՄԴ-10 | T86 |
| Կանխարգելում | Դոնորների ընտրություն, Իմունոսուպրեսիա |
Տրանսպլանտատի մերժումը տեղի է ունենում, երբ փոխպատվաստված հյուսվածքը կամ օրգանը մերժվում է ռեցիպիենտի իմուն համակարգի կողմից, և վերջինս սկսում է ոչնչացնել փոխպատվաստված հյուսվածքները։ Տրանսպլանտատի (այլ կերպ անվանվում է նաև տրանսպլանտ կամ փոխպատվաստուկ) մերժման պատասխանի ծանրությունը հնարավոր է նվազեցնել, եթե ընտրված դոնորի և ռեցիպիենտի մոլեկուլային համատեղելիության գործոնները միանման լինեն, ինչպես նաև եթե ռեցիպիենտը փոխպատվաստումից հետո ստանա իմունոդեպրեսանտ դեղորայք (որպես օրենք՝ մինչև կյանքի վերջ)[1]։
Մերժման կանխարգելումը մինչև փոխպատվաստումը[խմբագրել | խմբագրել կոդը]
Օրգանի փոխպատվաստման առաջին հաջողված փորձն իրականացվել է 1954թ., Ջոզեֆ Մյուրրեյի կողմից։ Քանի որ փոխպատվաստումն իրականացվել էր միաձվանի երկվորյակների միջև (այսպես կոչված՝ իզոտրանսպլանտացիա), ռեցիպիենտի մոտ տրանսպլանտատի մերժում տեղի չէր ունեցել։ Հակառակ դեպքում՝ MHC (I և II դասի) մակերեսային մոլեկուլները կոդավորող գեների տարբերակների (ալելների) անհամապատասխանությունների քանակն ուղիղ համեմատական է տրանսպլանտատի մերժման առաջացման արագության և ծանրության հետ։ Մարդու դեպքում MHC-ն հայտնի է որպես մարդու լեյկոցիտար հակածին (HLA)։
Չնայած, որ ցիտոտոքսիկ-համատեղելիության թեստերը կարող են կանխարգելել բջջային իմունիտետով պայմանավորված մերժումը, սակայն գենային էքսպրեսիայի թեստերը, որոնք որ սպեցիֆիկ են փոխպատվաստվող այս կամ այն օրգանի համար (Օրինակ՝ AlloMap մոլեկուլյար էքսպրեսիայի թեստը), ունեն բարձր բացասական կանխատեսման արժեք։ Հումորալ իմունիտետով պայմանավորված մերժումից խուսափելու համար նաև հարկավոր է, որ տրանսպլանտատները համատեղելի լինեն նաև ըստ ABO համակարգի։
ABO-անհամատեղելի տրանսպլանտատներ[խմբագրել | խմբագրել կոդը]
Քանի որ շատ փոքր տարիքի երեխաների մոտ (որպես օրենք՝ 12 ամսականից ցածր, սակայն հաճախ՝ 24 ամսականից ցածր[2]) իմուն համակարգը բավարար զարգացած չէ[3], նրանց հնարավոր է փոխպատվաստել օրգաններ այլապես անհամատեղելի դոնորներից։ Այս երևույթը հայտնի է որպես ABO-անհամատեղելի (ABOi) փոխպատվաստում։ Տրանսպլանտատի կենսունակությունը և պացիենտների մահացությունը մոտավորապես նույնն է լինում ABOi և ABO-համատեղելի (ABOc) ռեցիպիենտների համար[4]։ Թեպետ այս ասպարեզում ուսումնասիրություններն առավելապես կենտրոնացված են եղել մանկական սրտային փոխպատվաստման վրա, սակայն այս սկզբունքները մեծապես տարածվում են նաև այլ օրգանների փոխպատվաստման դեպքում[2]։
Այս հարցում ամենակարևոր գործոններն են՝ նախ՝ որ ռեցիպիենտի օրգանիմզը դեռևս արտադրած չի լինում իզոհեմագլյուտինիններ, և հետո՝ որ նրանց օրգանիզմում T բջիջ-անկախ հակածինների մակարդակը ցածր է լինում[3][5]։ Օրգանների փոխանակման միասնական ցանցի (UNOS) կանոնակարգերը թույլ են տալիս իրականացնել ABOi փոխպատվաստում 2 տարեկանից ցածր տարիքի երեխաների մոտ, եթե իզոհեմագլյուտինինների տիտրերը 1։4 են կամ դրանից ցածր[6][7], և եթե չկա հասանելի ABOc տարբերակ[6][7][8]։ Ուսումնասիրությունները ցույց են տվել, որ ABOi փոխպատվաստում ստանալու թույլատրելի ժամկետները հնարավոր է երկարաձգել՝ պացիենտին ոչ սեփական A և B հակածինների ազդեցությանը ենթարկելու դեպքում[9]։ Ավելին՝ եթե ռեցիպիենտը (ով, օրինակ, արյան B-դրական խմբի է պատկանում, և ստացել է AB-դրական տրանսպլանտատ) հետագայում կրկնակի փոխպատվաստման (ռետրանսպլանտացիա) կարիք զգա, ապա նա կարող է ստանալ թե՛ մեկ, թե՛ մյուս խմբի արյան խմբի տրանսպլանտատ[2][7]։
Մեծահասակներին ABOi սրտային փոխպատվաստման մոտեցումներում ավելի քիչ հաջողություններ են գրանցվել[10], այս դեպքում պահանջվում է, որ ռեցիպիենտի օրգանիզմում անտի-A կամ անտի-B հակամարմինների մակարդակները ցածր լինեն[10]։ Երիկամի տրանսպլանտացիայի դեպքում հաջողված ելքեր ավելի հաճախ են գրանցվում, այս դեպքում ABOi և ABOc տրանսպլանտատների երկարաժամկետ պահպանման հավանականությունները համեմատելի են[7]։
Տրանսպլանտատի մերժման իմունաբանական մեխանիզմներ[խմբագրել | խմբագրել կոդը]
Մերժումը ադապտիվ իմուն պատասխան է, որը պայմանավորված է առավելապես բջջային իմունիտետով (T-քիլլեր լիմֆոցիտների կողմից միջնորդված, որոնք առաջացնում են թիրախ բջիջների ապոպտոզ), ինչպես նաև հումորալ իմունիտետով (ակտիվացված B լիմֆոցիտներով միջնորդված, որոնք արտադրում են հակամարմիններ), չնայած, որ դեր է խաղում նաև բնածին իմունիտետի բաղադրիչների (ֆագոցիտներ և լուծելի իմուն սպիտակուցներ) մասնակցությունը։ Փոխպատվաստվող հյուսվածքների տարբեր տեսակների դեպքում մերժման գործընթացների աստիճանները տարբեր են։
Իմունիզացիա[խմբագրել | խմբագրել կոդը]
Կենդանուն նույն կամ մոտ գտնվող տեսակի պատկանող այլ առանձնյակի հակածինների ազդեցության երթարկելը կոչվում է ալոստիմուլյացիա, և հյուսվածքը կոչվում է ալոգեն։ Փոխպատվասման համար հաճախ օգտագործվում են դիակներից վերցված օրգաններ, որոնցում արդեն առկա է որոշ աստիճանի իշեմիա կամ բորբոքում։
Դոնորական հյուսվածքի դենդրիտային բջիջները, որոնք հիմնական հակածին-ներկայացնող բջիջներից են, տեղափոխվում են ռեցիպիենտի պերիֆերիկ լիմֆոիդ հյուսվածք (ավշային ֆոլիկուլներ և ավշահանգույցներ) և ներկայացնում են դոնորի սեփական պեպտիդները ռեցիպիենտի լիմֆոցիտներին (իմուն համակարգի բջիջներ, որոնք բնակվում են լիմֆոիդ հյուսվածքներում)։ Կա լիմֆոցիտների երկու հիմնական դաս, որոնք գործարկում են ադապտիվ իմունիտետը, որն այլ կերպ անվանվում է նաև ձեռքբերովի կամ սպեցիֆիկ իմունիտետ։ Սպեցիֆիկ իմունիտետի լիմֆոցիտներն են՝ T բջիջները (որոնք ներառում են T-հելփեր և T-քիլլեր ենթադասերը) և B բջիջները։
Ռեցիպիենտի T-հելփեր լիֆոցիտները համակարգում են սպեցիֆիկ իմուն պատասխան, որն ուղղված է դոնորական սեփական պեպտիդներին, դոնորական հյուսվածահամատեղելիության գլխավոր համալիրին (MHC), կամ նշված երկուսին միաժամանակ։
Իմունաբանական հիշողություն[խմբագրել | խմբագրել կոդը]
Երբ հիշողության T-հելփեր բջիջների CD4 ընկալիչները կապվում են տրանսպլանտատի թիրախ-բջիջների մակերեսին էքսպրեսվող MHC դաս II մոլեկուլներին, հիշողության T-հելփեր բջիջների T-բջջային ընկալիչները (TCR-ներ) կարող են ճանաչել թիրախային հակածինը, որը ներկայացված է լինում MHC դաս II մոլեկուլների վրա։ Այնուհետև հիշողության T-հելփեր բջիջն առաջացնում է կլոններ, որոնք, որպես էֆեկտոր բջիջներ, սկսում են արտազատել իմունային ազդանաշանային մոլեկուլներ (ցիտոկիններ)՝ հանգեցնելով ցիտոկինների հավասարակշռության մոտավորապես նույն մակարդակներին, որոնք եղել են այն պահին, երբ հիշողության T բջիջը պահպանում էր տվյալ հակածինն իր հիշողության մեջ։ Քանի որ այս երևույթն (այսպես կոչված՝ պրայմինգ) այս դեպքում տեղի է ունենում բորբոքման պայմաններում, իմուն պատասխանը լինում է պրոբորբոքային։
Բջջային իմունիտետ[խմբագրել | խմբագրել կոդը]
Ինչպես երևում է cyto- նախածանցից (որը նշանակում է «բջիջ»), ցիտոտոքսիկ ազդեցությունն ուղղված է բջջի ոչնչացմանը։ Ալոռեակտիվ T-քիլլեր բջիջները, որոնք նաև հայտնի են որպես ցիտոտոքսիկ T Լիմֆոցիտներ (CTL), ունեն CD8 ընկալիչներ, որոնք կապվում են տրանսպլանտատի MHC դաս I մոլեկուլներին, որոնց վրա ներկայացնում են դոնորի սեփական պեպտիդները (դոնորի կյանքի ընթացքում, սեփական հակածինների այսպիսի ներկայացումն օգնում էր պահպանել իմուն տոլերատնությունը սեփական հակածինների հանդեպ)։ Այնուհետև T-քիլլեր բջիջների T-բջջային ընկալիչները (TCR) ճանաչում են իրենց համապատասխանող էպիտոպը և առաջացնում են թիրախ-բջիջների ծրագրավորված մահ՝ ապոպտոզի միջոցով։
Հումորալ իմունիտետ[խմբագրել | խմբագրել կոդը]
Նախապես ոչ սեփական հակածնի հանդեպ առաջացած ձեռքբերովի (սպեցիֆիկ) իմունիզացիայի հետևանքով, ռեցիպիենտի օրգանիզմում կարող է առաջացած լինել սպեցիֆիկ հակամարմին, որը խաչաձև ազդեցություն կունենա նաև դոնորական հյուսվածքի հանդեպ. այս դեպքում սա դիտվում է որպես հակածնի երկրորդային ազդեցություն։ Սա հատկապես բնորոշ է այն դեպքերին, երբ, նախապես օրգանիզմ է ներթափանցում հակածնային կազմով (օրինակ՝ ըստ Kell հակածնային համակարգի) տարբերվող արյուն՝ ալոգեն արյան փոխներարկման կամ հղիության ընթացքում տրավմայի հետևանքով։ Այնուհետև՝ երկրորդային ազդեցության դեպքում, խաչաձև ռեակտիվ այս հակամարմինները փոխազդում են բնածին իմունիտետի բաղադրիչների հետ՝ կոմպլեմենտ կոչվող լուծելի իմուն սպիտակուցների հետ, ինչպես նաև բնածին իմունիտետի մաս կազմող բջիջների հետ, որոնք կոչվում են ֆագոցիտներ։ Սա հանգեցնում է փոխպատվաստված հյուսվածքում բորբոքման առաջացման, ինչն ի վերջո հանգեցնում է փոխպատվաստված հյուսվածքի ոչնչացմանը։
Հակամարմին[խմբագրել | խմբագրել կոդը]
Հակամարմինն իրենից ներկայացնում է լուծելի իմունոգլոբուլինի մոլեկուլ, որն արտադրվում է ակտիվացված B բջջի կողմից (որը կոչվում է պլազմատիկ բջիջ)։ Հակամարմնի մոլեկուլի հիմնական կառուցվածքային բաղադրիչն ունի Y տառի ձև։ Հակամարմինը կազմված է երկու Fab ռեգիոններից և մեկ Fc ռեգիոնից։ Fab ռեգիոններից յուրաքանչյուրի ծայրային հատվածը կոչվում է պարատոպ, որը կապվում է թիրախ-հակածնի մաս կազմող համապատասխան մոլեկուլային խմբի (այդ «թիրախ» խումբը՝ իր սպեցիֆիկ հաջորդականությամբ և կոնֆորմացիայով հանդերձ, կոչվում է էպիտոպ)։
Օպսոնիզացիա[խմբագրել | խմբագրել կոդը]
Գամմա իմունոգլոբուլինի (IgG) Fc ռեգիոնը նաև հնարավորություն է տալիս օպսոնիզացիայի. սա մի գործընթաց է, որի ժամանակ ֆագոցիտի (արյան մեջ՝ նեյտրոֆիլներ, հյուսվածքներում՝ մակրոֆագեր) վրա գտնվող Fc-ընկալիչը կապվում է հակամարմնի մոլեկուլի Fc հատվածին, և սա նպաստում է ֆագոցիտի կողմից հակամարմնի Fab ռեգիոնին միացված հակածնի յուրացման գործընթացի ավելի ակտիվացմանը։
Կոմպլեմենտային կասկադ[խմբագրել | խմբագրել կոդը]
Երբ գամմա դասի իմունոգլոբուլինի (IgG) պարատոպը կապվում է համապատասխան էպիտոպի հետ, IgG-ի Fc ռեգիոնը ենթարկվում է կոնֆորմացիոն փոփոխության, և ունակ է լինում իր վրա ընդունել կոմպլեմենտի համակարգի սպիտակուց՝ թողարկելով կոմպլեմենտի կասկադը, որն ավարտվում է բջջի թաղանթին անցքեր առաջացնելով։ Երբ առաջանում են մեծ քանակությամբ այդպիսի անցքեր, հեղուկը սկսում է մեծ քանակով ներթափանցել բջիջ, ինչը հանգեցնում է բջջաթաղանթի պատռման։
Ֆագոցիտների թաղանթին գտնվող պատտերն-ճանաչող ընկալիչները (PRR), որպիսիք են, օրինակ, Toll-անման ընկալիչները, կարող են բջիջների մնացորդները ճանաչել որպես վնասման հետ ասոցացված մոլեկուլային ֆրագմենտներ (DAMP-ներ), ինչից հետո ֆագոցիտները սկսում են արտազատել պրոբորբոքային ցիտոկիններ՝ նպաստելով դեպի տվյալ տեղամաս այլ ֆագոցիտների տեղափոխմանը և ներգրավմանը, քանի որ վերջիններս ունակ են զգալ արտազատված ցիտոկինների (քեմոտաքսիններ) կոնցենտրացիոն գրադիենտը։
| Հյուսվածք | Մեխանիզմ |
|---|---|
| Արյուն | Հակամարմիններ (իզոհեմագյլուտինիններ) |
| Երիկամ | Հակամարմիններ; Բջջային իմունիտետ |
| Սիրտ | Հակամարմիններ; Բջջային իմունիտետ |
| Մաշկ | Բջջային իմունիտետ |
| Ոսկրածուծ | Բջջային իմունիտետ |
| Եղջերաթաղանթ | Եթե չկա անոթավորում, սովորաբար ընդունվում է ռեցիպիենտի
օրգանիզմի կողմից; բջջային իմունիտետ |
Բժշկական կատեգորիաներ[խմբագրել | խմբագրել կոդը]
Խթանվելով նախապես առկա հումորալ իմունիտետիտետի կողմից՝ գերսուր մերժումն արտահայտվում է փոխպատվաստումից հետո րոպեներ անց, և, եթե փոխպատվաստված հյուսվածքն անհապաղ չի հեռացվում, առաջանում է համակարգային բորբոքային պատասխանի համախտանիշ։ Երիկամային տրանսպլանտատների դեպքում կա էրիթրոցիտների ագլյուտինացիայի (այսպես կոչված՝ «սոսնձման») արագ առաջացման ռիսկ, քանի որ հակամարմնի մոլեկուլը միանգամից կապվում է մի քանի թիրախ-էրիթրոցիտների։
Թեպետ մարդկային դոնորական երիկամներ հնարավոր է ստանալ քիչ թե շատ ռուտին կերպով, սակայն մյուս օրգանների մեծ մասի դեպքում առկա է մարդկային դոնորական օրգանների խիստ պակասություն, այդ իսկ պատճառով գիտնականները որպես այլընտրանքային տարբերակ սկսել են դիտարկել քսենոտրանսպլանտացիան՝ այլ տեսակի կենդանի օրգանիզմներից վերցված օրգանների փոխպատվաստումը։ Քսենոտրանսպլանտացիայի համար որպես ամենից հավանական դոնոր դիտարկվող կենդանիները խոզերն են, քանի որ այս կենդանիների օրգանիզմը մարդու օրգանիզմի հետ ունի անատոմիական և ֆիզիոլոգիական շատ նմանություններ[11]։ Սակայն, քսենոտրանսպլանտացիայի դեպքում գերսուր մերժում առաջացնող գլխավոր գործոններից մեկն է համարվում գալակտոզ-ալֆա-1,3-գալակտոզ (αGal) կոչվող ածխաջուրը։ Ի տարբերություն գրեթե բոլոր մյուս կաթնասունների՝ մարդու և այլ պրիմատների օրգանիզմում չի արտադրվում αGal-ը, և, փաստորեն, նրանց օրգանիզմը ճանաչում է այն որպես հակածին[12]։ Փոխպատվաստման դեպքում, այսպես կոչված, քսենոռեակտիվ բնական հակամարմինները ճանաչում են տրանսպլանտատում առկա αGal-ը որպես հակածին, որից հետո կոմպլեմենտի համակարգով միջնորդված իմուն պատասխանը հանգեցնում է տրանսպլանտատի մերժման[13]։
Տրանսպլանտատի սուր մերժում[խմբագրել | խմբագրել կոդը]
Առաջանալով բջջային իմունիտետի ձևավորմանը զուգընթաց՝ սուր մերժումը որոշ չափով տեղի է ունենում բոլոր տրանսպլանտատների դեպքում (բացառությամբ՝ միաձվանի երկվորյակների միջև տրանսպլանտացիայի դեպքերի), քանի դեռ տեղի չի ունենում ռեցիպիենտի օրգանիզմում իմուն համակարգի ճնշում (սովորաբար՝ իմունոդեպրեսանտ դեղորայքի միջոցով)։ Սուր մերժումը սկսվում է տրանսպլանտացիայից հետո մոտավորապես մեկ շաբաթ անց, և դրա ռիսկն ամենաբարձր մակարդակին է մնում փոխպատվաստումից հետո առաջին երեք ամսվա ընթացքում. սակայն այն կարող է առաջանալ նաև ավելի ուշ՝ ամիսներ և նույնիսկ տարիներ անց։ Իրենց մեջ շատ արյունատար անոթներ պարունակող հյուսվածքների և օրգանների, օրինակ՝ երիկամի կամ լյարդի դեպքում, սովորաբար դիտվում են ամենավաղ նշանները, մասնավորապես՝ արյունատար անոթները ներսից պատող էնդոթելային բջիջների մոտ, սակայն երևույթը տեղի է ունենում լյարդի տրանսպլանտատների մոտավորապես 10-30%-ի և երիկամային տրանսպլանտատների մոտավորապես 10-20%-ի դեպքում։
Սուր մերժման առանձին էպիզոդը հնարավոր է ժամանակին ախտորոշել և անհապաղ բուժել, ինչի միջոցով սովորաբար հնարավոր է լինում կանխարգելել օրգանի անբավարարության առաջացումը։ Սակայն, սուր մերժման կրկնվող էպիզոդները, որպես օրենք, հանգեցնում են քրոնիկական մերժման։ Համարվում է, որ սուր մերժման գործընթացը տեղի է ունենում բջիջներով միջնորդված ուղիով, մասնավորապես՝ դեր են խաղում մոնոնուկլեար մակրոֆագերը և T լիմֆոցիտները։ Սուր մերժման դեպքում հյուսվածաբանական պատկերը բնորոշվում է խիտ լիմֆոցիտար բջջային ինֆիլտրատով, ինչպես նաև դոնորական օրգանի անոթներում վասկուլիտի նշաններով։
Տրանսպլանտատի քրոնիկական մերժում[խմբագրել | խմբագրել կոդը]
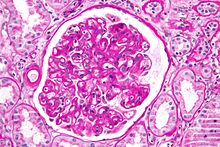
Ի սկզբանե «քրոնիկական մերժում» տերմինով բնութագրվել է փոխպատվաստված օրգանների ֆունկցիայի երկարաժամկետ խանգարումը՝ տրանսպլանտատի արյունատար անոթների ֆիբրոզի հետևանքով։ Սակայն այժմ նշված երևույթը կոչվում է «ալոտրանսպլանտատի քրոնիկ վասկուլոպաթիա», իսկ «քրոնիկական մերժում» տերմինով առավելապես բնութագրում են իմուն համակարգի առավել ազդեցիկ մեխանիզմների ներգործությամբ մերժումը։
Քրոնիկական մերժման երևույթով է հնարավոր բացատրել թոքային տրանսպլանտատներ ստացող ռեցիպիենտների մեծ մասի մոտ դիտվող քրոնիկական հիվանդացությունը[14][15], մոտավորապես 4.7 տարվա վերապրելիության միջին ցուցանիշը, որը այլ կենսական օրգանների փոխպատվաստման դեպքում դիտվող վերապրելիության ցուցանիշներից մոտ 2 անգամ ցածր է[16]։ Ախտաբանական հյուսվածաբանության մեջ այս վիճակը կոչվում է bronchiolitis obliterans, որը կլինիկորեն արտահայտվում է որպես շնչուղիների պրոգրեսիվող օբստրուկցիա, որի դեպքում հաճախ դիտվում է դիսպնեա և հազ, և ի վերջո հիվանդի մոտ զարգանում է թոքային անբավարարություն կամ երկրորդային սուր ինֆեկցիա։
Երբ առկա է լինում շնչուղիների օբստրուկցիա, որը հնարավոր չի լինում վերագրել այլ պատճառի, ապա դրվում է bronchiolitis obliterans համախտանիշ (BOS) ախտորոշումը։ Այն հաստատվում է, երբ դիտվում է FEV1-ի (առաջին վայրկյանում ուժեղացված արտաշնչման ծավալ) կայուն իջեցում առնվազն 20%-ով՝ երեք կամ ավել շաբաթվա ընթացքում[17]։ Այս համախտանիշը դիտվում է թոքային տրանսպլանտատներ ստացած ռեցիպիենտների ավելի քան 50%-ի մոտ՝ փոխպատվաստումից 5 տարի անց, իսկ 10 տարի անց՝ ավելի քան 80%-ի մոտ։ Առաջինը դիտվում է լիմֆոցիտներով ինֆիլտրացիա, որին հաջորդում է էպիթելային բջիջների վնասումը, այնուհետև՝ բորբոքումը և ֆիբրոբլաստների ու միոֆիբրոբլաստների ներգրավումը պրոցեսի մեջ, որոնք սկսում են արտադրել սպիտակուցներ՝ առաջացնելով սպիական հյուսվածք[18]։ BOS-ի պրոգրեսիվման աստիճանը լինում է տարբեր, և այն համարվում է մեծապես անկանխատեսելի. օրինակ, կարող է դիտվել թոքերի ֆունկցիայի կտրուկ անկում, սակայն տարիների ընթացքում այն կարող է վերականգնվել, կամ էլ հակառակը՝ արագորեն պրոգրեսիվել և ամիսների ընթացքում հանգեցնել մահվան։ Ռիսկի գործոններից են՝ նախկինում տարած սուր մերժման էպիզոդները, գաստրոէզոֆագեալ ռեֆլյուքս հիվանդությունը, սուր ինֆեկցիաները, պատկանելիությունը որոշակի տարիքային խմբերի, HLA անհամապատասխանությունը, լիմֆոցիտային բրոնխիոլիտը և փոխպատվաստված օրգանի (կամ հյուսվածքի) ֆունկցիայի խանգարումները (օրինակ՝ օդուղիների իշեմիան)[19]։
Տրանսպլանտատի մերժում՝ հիվանդի անհետևողականության պատճառով[խմբագրել | խմբագրել կոդը]
Տրանսպլանտատի մերժման կարևորագույն պատճառներից մեկն է հանդիսանում նշանակված իմունոդեպրեսանտ դեղորայքի ընդունման ռեժիմի խախտումը հիվանդի կողմից։ Մասնավորապես՝ այս խնդիրը տարածված է դեռահաս ռեցիպիենտների մոտ[20]՝ երբեմն դեղերի ընդունման ճիշտ ռեժիմը չպահպանելու դեպքերը նրանց մոտ հասնում են 50%-ի[20]։
Տրանսպլանտատի մերժման ախտորոշումը[խմբագրել | խմբագրել կոդը]
Սուր մերժման ախտորոշումը հիմնվում է կլինիկական տվյալների վրա, սակայն ախտորոշումը հաստատելու համար նաև պահանջվում են լաբորատոր տվյալներ՝ արյան անալիզներ և անգամ հյուսվածքային բիոպսիա։ Հյուսվածաբանական անալիզի ընթացքում երեք հիմնական հյուսվածաբանական նշան կա, որոնք կարող են վկայել մերժման մասին։ Դրանք են՝ (1) T բջիջներով ինֆիլտրացիա, որը կարող է ուղեկցվել նաև էոզինոֆիլներով, պլազմատիկ բջիջներով և նեյտրոֆիլներով ինֆիլտրացիայով, (2) հյուսվածքի կառուցվածքային վնասումներ, որոնք տարբեր հյուսվածքների դեպքում տարբեր են, և (3) արյունատար անոթների վնասում[21][22][23]։ Ոչ ինվազիվ հետազոտություններից կարող է լինել նաև in vivo ռադիոնշակրված իմունային բջիջների հայտնաբերումը բջջային ՄՌՇ-ի միջոցով, ինչպես նաև գենային էքսպրեսիայի քանակական անալիզը (GEP)[24][25]։
Տրանսպլանտատի մերժման բուժումը[խմբագրել | խմբագրել կոդը]
Գերսուր մերժումը տեղի է ունենում շատ արագ և շատ ծանր կերպով՝ րոպեների ընթացքում, հետևաբար՝ այս դեպքում անհրաժեշտ են անհապաղ միջոցառումներ, մասնավորապես՝ փոխպատվաստված հյուսվածքի անհապաղ հեռացում։ Քրոնիկական մերժումը, որպես օրենք, համարվում է անդարձելի և բուժման դժվար ենթարկվող գործընթաց. այս ժամանակ սովորաբար հնարավորության դեպքում ցուցված է լինում ռետրանսպլանտացիա՝ կրկնակի փոխպատվաստում։ Չնայած, ներկայումս ուսումնասիրվում է մասնավորապես ցիկլոսպորինի ինհալյացիայի կիրառումը, որը պոտենցիալ կարող է թոքերի փոխպատվաստման դեպքում հետաձգել կամ կանխարգելել քրոնիկական մերժումը։ Բժշկության մեջ կա Սուր մերժման բուժման մի քանի մարտավարություն։ Սակայն, չնայած բուժման մեթոդների զարգացմանը՝ տրանսպլանտատի մերժումը համարվում է փոխպատվաստված օրգանների անբավարարության գլխավոր պատճառներից մեկը[26]։
Իմունոդեպրեսիվ թերապիա (իմունաճնշում, իմունոսուպրեսիա)[խմբագրել | խմբագրել կոդը]
Կարող է կիրառվել կորտիկոստերոիդների բարձր դոզաներով կարճատև բուժման կուրս, և այդ կուրսը հետագայում կրկնվում է։ Եռակի բուժման մեթոդի դեպքում ավելացվում է նաև կալցինևրինի ինհիբիտոր և հակապրոլիֆերատիվ դեղամիջոց։ Եթե կալցինևրինի ինհիբիտորները կամ ստերոիդները հակացուցված են, կիրառվում են mTOR-ի ինհիբիտորներ։
Իմունոդեպրեսանտ դեղամիջոցներ.
- Կորտիկոստերոիդներ
- Կալցինևրինի ինհիբիտորներ
- Հակապրոլիֆերատիվ դեղորայք
- mTOR-ի ինհիբիտորներ
Հակամարմինների կիրառմամբ բուժման մեթոդներ[խմբագրել | խմբագրել կոդը]
Իմունոդեպրեսանտներով բուժումը կարող է համակցվել իմուն համակարգի որոշ կոնկրետ բաղադրիչների հանդեպ սպեցիֆիկ հակամարմինների կիրառմամբ։ Մոնոկլոնալ հակա-T-բջջային հակամարմին OKT3-ը, որը ժամանակին օգտագործվել է տրանսպլանտատի մերժման կանխարգելման նպատակով, մինչ այժմ երբեմն օգտագործվում է սուր մերժման ծանր դեպքերի բուժման նպատակով, սակայն ներկայումս դրա կիրառությունը խիստ սահմանափակվել է, քանի որ հայտնաբերվել է, որ հաճախ այն առաջացնում է ծանր ցիտոկինային արտազատման համախտանիշ և ուշ հետ-փոխպատվաստումային լիմֆոպրոլիֆերատիվ խանգարում։
Հակամարմինային պրեպարատներ.
- Մոնոկլոնալ հակա-IL-2Rα ընկալիչային հակամարմիններ
- Պոլիկլոնալ հակա-T-բջջային հակամարմիններ
- Մոնոկլոնալ հակա-CD20 հակամարմիններ
Արյան փոխանցում[խմբագրել | խմբագրել կոդը]
Իմունոսուպրեսիայի կամ հակամարմինային պրեպարատներով բուժման անարդյունավետության դեպքում երբեմն կիրառվում է ֆոտոֆորեզ, կամ արտամարմնային ֆոտոիմուն թերապիա (ECP)՝ փոխպատվաստված հյուսվածքին սպեցիֆիկ հակամարմինների հեռացման նպատակով։
Ոսկրածուծի փոխպատվաստում[խմբագրել | խմբագրել կոդը]
Ոսկրածուծային տրանսպլանտատը կարող է փոխարինել ռեցիպիենտի իմուն համակարգի մի մասը դոնորական իմունիտետի բաղադրիչներով, ինչի հետևանքով ռեցիպիենտի օրգանիզմը սկսում է ընդունել նոր օրգանը, և չի առաջանում մերժում։ Ոսկրածուծի հեմատոպոետիկ ցողունային բջիջները (մահացած արյան բջիջների (այդ թվում՝ իմունիտետի մաս կազմող լեյկոցիտների) փոխարինումն իրականացնող արյունաստեղծ ցողունային բջիջների խումբ) պետք է վերցված լինեն այն նույն դոնոր օրգանիզմից, որից որ վերցված է տվյալ օրգանը, կամ նրա միաձվանի երկվորյակից, կամ (տեսականորեն) նրա կլոնից։ Կա ռիսկ «տրանսպլանտատն ընդդեմ տիրոջ» հիվանդության (ՏԸՏՀ, GVHD) առաջացման, որի դեպքում ոսկրածուծի հետ ներթափանցող հասուն լիմֆոցիտները որպես օտար են սկսում ճանաչել ռեցիպիենտի հյուսվածքները և պայքարում են դրանց դեմ։
Գենային թերապիա[խմբագրել | խմբագրել կոդը]
Գենային թերապիան մեկ այլ մեթոդ է, որը կարող է օգտագործվել որպես բուժման մոտեցում։ Այս մեթոդի դեպքում պետք է ապաակտիվացվեն այն գեները, որոնք օրգանիզմում պայմանավորում են տրանսպլանտատի մերժումը։ Այս ոլորտը դեռևս ուսումնասիրությունների փուլում է, և գենային թերապիան դեռևս չի օգտագործվել հիվանդների բուժման նպատակով[27][28][29][30]։ Ներկայիս ուսումնասիրությունները հակված են կենտրոնանալ Th1-ի և Th17-ի վրա, որոնք միջնորդում են ալոտրանսպլանտատների մերժումը CD4 և CD8 T լիմֆոցիտների միջոցով[31]։
Տես նաև[խմբագրել | խմբագրել կոդը]
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Frohn, C; Fricke, L; Puchta, JC; Kirchner, H (Feb 2001). «The effect of HLA-C matching on acute renal transplant rejection». Nephrology, Dialysis, Transplantation. 16 (2): 355–60. doi:10.1093/ndt/16.2.355. PMID 11158412.
- ↑ 2,0 2,1 2,2 ABO Incompatible Heart Transplantation in Young Infants. (2009, July 30). ABO Incompatible Heart Transplantation in Young Infants. American Society of Transplantation. Retrieved from «Archived copy». Արխիվացված է օրիգինալից 2013 թ․ դեկտեմբերի 20-ին. Վերցված է 2013 թ․ դեկտեմբերի 25-ին.
{{cite web}}: CS1 սպաս․ արխիվը պատճենվել է որպես վերնագիր (link) - ↑ 3,0 3,1 West, L. J. (2011). «ABO-incompatible hearts for infant transplantation». Current Opinion in Organ Transplantation. 16 (5): 548–54. doi:10.1097/MOT.0b013e32834a97a5. PMID 21836514.
- ↑ Saczkowski, R; Dacey, C; Bernier, PL (Jun 2010). «Does ABO-incompatible and ABO-compatible neonatal heart transplant have equivalent survival?». Interactive Cardiovascular and Thoracic Surgery. 10 (6): 1026–33. doi:10.1510/icvts.2009.229757. PMID 20308266.
- ↑ Burch, M; Aurora, P (Apr 2004). «Current status of paediatric heart, lung, and heart-lung transplantation». Archives of Disease in Childhood. 89 (4): 386–389. doi:10.1136/adc.2002.017186. PMC 1719883. PMID 15033856.
- ↑ 6,0 6,1 United Network for Organ Sharing. (2013, January 31). OPTN Policy 3.7 - Allocation of Thoracic Organs. Retrieved from «Archived copy». Արխիվացված է օրիգինալից 2013 թ․ դեկտեմբերի 7-ին. Վերցված է 2013 թ․ դեկտեմբերի 25-ին.
{{cite web}}: CS1 սպաս․ արխիվը պատճենվել է որպես վերնագիր (link) - ↑ 7,0 7,1 7,2 7,3 Urschel, S; Larsen, IM; Kirk, R; Flett, J; Burch, M; Shaw, N; Birnbaum, J; Netz, H; Pahl, E; Matthews, KL; Chinnock, R; Johnston, JK; Derkatz, K; West, LJ (Mar 2013). «ABO-incompatible heart transplantation in early childhood: an international multicenter study of clinical experiences and limits». The Journal of Heart and Lung Transplantation. 32 (3): 285–92. doi:10.1016/j.healun.2012.11.022. PMID 23305695.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Almond, CS; Gauvreau, K; Thiagarajan, RR; Piercey, GE; Blume, ED; Smoot, LB; Fynn-Thompson, F; Singh, TP (2010 թ․ մայիսի 4). «Impact of ABO-incompatible listing on wait-list outcomes among infants listed for heart transplantation in the United States: a propensity analysis». Circulation. 121 (17): 1926–33. doi:10.1161/CIRCULATIONAHA.109.885756. PMC 4273502. PMID 20404257.
- ↑ Fan, X; Ang, A; Pollock-Barziv, SM; Dipchand, AI; Ruiz, P; Wilson, G; Platt, JL; West, LJ (Nov 2004). «Donor-specific B-cell tolerance after ABO-incompatible infant heart transplantation». Nature Medicine. 10 (11): 1227–33. doi:10.1038/nm1126. PMID 15502841.
- ↑ 10,0 10,1 Tydén, G; Hagerman, I; Grinnemo, KH; Svenarud, P; van der Linden, J; Kumlien, G; Wernerson, A (Dec 2012). «Intentional ABO-incompatible heart transplantation: a case report of 2 adult patients». The Journal of Heart and Lung Transplantation. 31 (12): 1307–10. doi:10.1016/j.healun.2012.09.011. PMID 23107062.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Klymiuk, N; Aigner, B; Brem, G; Wolf, E (Mar 2010). «Genetic modification of pigs as organ donors for xenotransplantation». Molecular Reproduction and Development. 77 (3): 209–21. doi:10.1002/mrd.21127. PMID 19998476.
- ↑ Galili, U (Dec 2005). «The alpha-gal epitope and the anti-Gal antibody in xenotransplantation and in cancer immunotherapy». Immunology and Cell Biology. 83 (6): 674–86. doi:10.1111/j.1440-1711.2005.01366.x. PMID 16266320.
- ↑ Candinas, D; Adams, DH (Feb 2000). «Xenotransplantation: postponed by a millennium?». QJM : Monthly Journal of the Association of Physicians. 93 (2): 63–6. doi:10.1093/qjmed/93.2.63. PMID 10700475.
- ↑ Jaramillo, A; Fernández, FG; Kuo, EY; Trulock, EP; Patterson, GA; Mohanakumar, T (Feb 2005). «Immune mechanisms in the pathogenesis of bronchiolitis obliterans syndrome after lung transplantation». Pediatric Transplantation. 9 (1): 84–93. doi:10.1111/j.1399-3046.2004.00270.x. PMID 15667618.
- ↑ Lau, CL; Patterson, GA (Nov 2003). «Current status of lung transplantation». The European Respiratory Journal. Supplement. 47: 57s–64s. doi:10.1183/09031936.03.00022103. PMID 14621118.
- ↑ http://www.OPTN.org Արխիվացված 2011-11-11 Wayback Machine
- ↑ Lama, VN; Murray, S; Lonigro, RJ; Toews, GB; Chang, A; Lau, C; Flint, A; Chan, KM; Martinez, FJ (2007 թ․ հունիսի 1). «Course of FEV(1) after onset of bronchiolitis obliterans syndrome in lung transplant recipients». American Journal of Respiratory and Critical Care Medicine. 175 (11): 1192–8. doi:10.1164/rccm.200609-1344OC. PMC 1899272. PMID 17347496.
- ↑ Nicod, LP (Jul 2006). «Mechanisms of airway obliteration after lung transplantation». Proceedings of the American Thoracic Society. 3 (5): 444–9. doi:10.1513/pats.200601-007AW. PMID 16799090.
- ↑ Belperio, JA; Weigt, SS; Fishbein, MC; Lynch JP, 3rd (2009 թ․ հունվարի 15). «Chronic lung allograft rejection: mechanisms and therapy». Proceedings of the American Thoracic Society. 6 (1): 108–21. doi:10.1513/pats.200807-073GO. PMID 19131536.
{{cite journal}}: CS1 սպաս․ թվային անուններ: authors list (link) - ↑ 20,0 20,1 Dobbels, F; Hames, A; Aujoulat, I; Heaton, N; Samyn, M (Feb 2012). «Should we retransplant a patient who is non-adherent? A literature review and critical reflection». Pediatric Transplantation. 16 (1): 4–11. doi:10.1111/j.1399-3046.2011.01633.x. PMID 22248250.
- ↑ Kidney biopsy:risks
- ↑ Heart biopsy:risks
- ↑ Lung biopsy:risks
- ↑ Hitchens, TK; Ye, Q; Eytan, DF; Janjic, JM; Ahrens, ET; Ho, C (Apr 2011). «19F MRI detection of acute allograft rejection with in vivo perfluorocarbon labeling of immune cells». Magnetic Resonance in Medicine. 65 (4): 1144–53. doi:10.1002/mrm.22702. PMC 3135171. PMID 21305593.
- ↑ Gheith OA (2011). «Gene expression profiling in organ transplantation». Int J Nephrol. 2011: 180201. doi:10.4061/2011/180201. PMC 3154482. PMID 21845224.
{{cite journal}}: CS1 սպաս․ չպիտակված ազատ DOI (link) - ↑ Naesens, M (2014). «The Histology of Kidney Transplant Failure: A Long-Term Follow-Up Study». Transplantation. 98 (4): 427–435. doi:10.1097/TP.0000000000000183. PMID 25243513.
- ↑ Gene group responsible for transplant rejection: the Major_histocompatibility_complex
- ↑ Transplant rejection and genomics
- ↑ Gene Therapy Progress and Prospects: Gene therapy in organ transplantation
- ↑ Gene therapy in transplantation
- ↑ The John Iacomini Lab
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Տրանսպլանտատի մերժում» հոդվածին։ |
| ||||||||||
