Կոնֆորմացիա (քիմիա)
Կոնֆորմացիա (լատին․՝ conformatio, ձև, կառուցվածք, դասավորություն) մոլեկուլի, երկրաչափական ձև, որը կարող է ընդունել օրգանական միացության մոլեկուլը պարզ կապի շուրջն ատոմների կամ ատոմական խմբերի պտտման ժամանակ։ Միայն կոնֆորմացիայով տարբերվող մոլեկուլները կոչվում են կոնֆորմերներ կամ պտտական իզոմերներ։ Կոնֆորմացիայի գոյությունը պայմանավորված է իրար հետ անմիջապես չկապված տեղակալիչների, այդ թվում նաև ջրածնի ատոմների տարածական փոխազդեցությամբ (օրինակ, վանմամբ, ձգմամբ, ջրածնական կապերի առաջացմամբ)։ Օրինակ, պենտանի մոլեկուլի մի քանի հարթ կոնֆորմացիաները։ Ի տարբերություն երկրաչափական և օպտիկական իզոմերների կոնֆորմերները սովորական պայմաններում հեշտությամբ են անցնում մեկը մյուսին (առանց կապերի խզման), այդ պատճառով դրանք չեն անջատվում ազատ վիճակում։ Օրգանական միացությունների մոլեկուլները, սովորաբար, գոյություն ունեն կոնֆորմերների հավասարակշռված խառնուրդի ձևով, որոնց մեջ գերակշռում է էներգետիկորեն ամենաձեռնտու իզոմերը։ Մոլեկուլի կոնֆորմացիոն վիճակներն ազդում են նյութերի ֆիզիկական հատկությունների, դրանց փոխազդեցությունների ուղղության և արագության վրա։
Կոնֆորմացիոն իզոմերներ։ Բաց շղթայով միացությունների կոնֆորմացիաները[խմբագրել | խմբագրել կոդը]
Ինչպես վերը նշեցինք, ատոմների տարբեր տարածական դասավորվածության հետևանքով, որը առաջանում է պարզ կապերի շուրջ կատարվող պտույտի ժամանակ, առաջանում են կոնֆորմացիոն իզոմերներ (կոնֆորմերներ)։ Կոնֆորմացիոն իզոմերները ընդունված է պատկերել Նյումենի բանաձևերով, որոնց վրա նշվում են տեղակալիչների դիրքերը կապերի շուրջ պտույտ կատարելու դեպքում։ Էթանի օրինակի վրա քննարկենք հնարավոր կոնֆորմերների թիվը, ընդունելով մինիմալ պտույտը հավասար 60°։ Կոնֆորմացիաները, որոնցում տեղակալիչները գտնվում են միմյանց դիմաց (պտտման աստիճանը 0°,կամ 360°), առավել մոտ դիրքում, օժտված են բարձր էներգիայով և կոչվում են «ծածկված»։ Կոնֆորմացիաները, որոնցում տեղակալիչները գտնվում են առավել մեծ հեռավորության վրա (պտտման անկյունը 180°), գտնվում են ցածր էներգետիկ մակարդակի վրա և կոչվում են «արգելակված»[1]։.

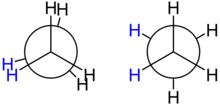
Էթանի ծածկված կոնֆոմացիայի պոտենցիալ էներգիան 12կՋ/մոլ-ով բարձր է, քան արգելակվածինը։ Դա պայմանավորված է հարևան դիրքերում գտնվող կապերի էլեկտրոնների միջև առաջացող վանող ուժերով, որի հետևանքով զարգանում է այսպես կոչված տորսիոն լարվածություն։ Էթանի տարբեր կոնֆորմերների էներգետիկ մակարդակների տարբերությունը մեծ չէ և սովորական պայմաններում մեկ կոնֆերմերը հեշտությամբ անցնում է մյուսի։ Բութանի մոտ տորսիոն լարվածությանը գումարվում է ևս մեկը, որը առաջանում է մեթիլ խմբերի փոխադարձ վանման հետևանքով և կոչվում է Վան-դեր-Վալսի լարվածություն։ Այս դեպքում համակարգի լարվածությունը ավելի մեծ է։ Հետևաբար մոլեկուլները ձգտում են ընդունել այնպիսի կոնֆորմացիա, որի դեպքում առավել կայուն են[2]։.

Էներգետիկ առումով միջին դիրք գրավող կոնֆորմացիաները կոչվում են շեղված, կամ գոշ-կոնֆորմացիաներ։
Ցիկլիկ միացությունների կոնֆորմացիաներ[խմբագրել | խմբագրել կոդը]
Ցիկլոալկաններում, տորսիոն և Վան-դեր-Վալսի լարվածությանը գումարվում է Բայերի անկյունային լարվածությունը։ Վերջինս պայմանավորված է ցիկլում վալենտային անկյունների շեղումով՝ նորմալ տետրաէդրի անկյունից։ Օրինակ, առավել պարզ ներկայացուցչի, ցիկլոպրոպանի վալենտային անկյունները կազմում են 60°,որի հետևանքով առաջանում է մեծ լարվածություն։


Ցիկլոպրոպանում պտույտ կապերի շուրջ չի կատարվում, և ջրածնի բոլոր ատոմները գտնվում են ծածկված դիրքում։ Հետևաբար, ցիկլոպրոպանը չունի կոնֆորմերներ։ Ելնելով վերը նշվածից, հասկանալի է, որ եռանդամ ցիկլը անկայուն է։ Հաջորդ ներկայացուցիչը ցիկլոբութանն է, որի վալենտային անկյունները հավասար են 90°։ Ջրածնի ատոմները գտնվում են ծածկված դիրքում։ Բարձր տորսիոն և անկյունային լարվածության հետևանքով քառանդամ ցիկլը նույնպես անկայուն է։
Ցիկլոպենտանի համար հայտնի է երկու կոնֆորմեր, հարթ ձևի մոտ բացակայում է անկյունային լարվածությունը, քանի որ վալենտային անկյունները հավասար են 108°, որը մոտ է նորմալ արժեքին։ Սակայն հարթ ձևի մոտ ուժեղ է դրսևորվում տորսին լարվածությունը (ծածկման լարվածությունը), որը ծրարի կոնֆորմացիայի դեպքում ավելի ցածր է։


-
Ցիկլոհեքսանի նավակը
-
Ցիկլոհեքսանի բազկաթոռ
Ցիկլոհեքսանում անկյունները հավասար են 120°։ Սրա համար հայտնի են մի շարք կոնֆորմերներ, որոնցից ավելի ցածր լարվածություն ունեն մի քանի որ հարթ, այսպես կոչված, նավակ, բազկաթոռ և զեթաձև կոնֆորմերները։


Նյումենի պրոյեկցիոն բանաձևերը հնարավորություն են տալիս հստակ պատկերացնել ատոմների փոխադարձ դիրքը։ Առանցքին զուգահեռ կապերը կոչվում են աքսիալ, իսկ 109,28° անկյան տակ գտնվողներինը՝ էկվատորիալ։


Ցիկլոհեքսանի բազկաթոռի կոնֆորմացիայում ջրածնի ատոմների դիրքը նույնն է, ինչ էթանի արգելակված կոնֆորմացիայում, իսկ ածխածինները՝ բութանի շեղված կոնֆորմացիայում։ Նավակ կոնֆորմացիայի դեպքում ածխածինների մոտ գտնվող ջրածինների ծածկված դիրքի շնորհիվ, ցիկլի լարվածությունը մեծ է։ Հետևաբար, բազկաթոռ կոնֆորմերը էներգետիկ տեսակետից ավելի շահավետ է։
Տես նաև[խմբագրել | խմբագրել կոդը]
Գրականություն[խմբագրել | խմբագրել կոդը]
- Физер Л., Физер М., Органическая химия. Углубленный курс. т. 1. пер с англ., Под ред. д.х.н. Н. С. Вульфсона. Изд. «Химия». М., 1969.
- Пальм В. А., Введение в теоретическую органическую химию, М., 1974;
- Соколов В И., Введение в теоретическую стереохимию, М., 1979;
- Сланина 3., Теоретические аспекты явления изомерии в химии, пер. с чеш., М., 1984;
- Потапов В М., Стереохимия М., 1988.
- Большой энциклопедический словарь. Химия. Изд.։ Большая Российская энциклопедия, 2003, ISBN 5-85270-253-6
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 5, էջ 587)։ |





