Իզոմերիա
Նարեկ Հայրապետյաների գոյության հնարավորությունը։ Այդպիսի միացությունները կոչվեցին իզոմերներ։ Համաձայն IUPAC-ի կանոնների, տարբերում են երկու տեսակի իզոմերներ՝
- 1. կառուցվածքային և
- 2.տարածական (ստերեոիզոմերներ)[1]։
Կառուցվածքային իզոմերիա[խմբագրել | խմբագրել կոդը]
Մոլեկուլի կառուցվածքը որոշվում է ատոմների միջև եղած կապերի բնույթով և հաջորդականությամբ։ Մոլեկուլները, որոնք ունեն նույն մոլեկուլային բանաձևը, բայց տարբեր կառուցվածքային բանաձևեր, կոչվում են կառուցվածքային իզոմերներ[2]։
Կառուցվածքային իզոմերիայի տեսակներից են.
- պայմանավորված ածխածնային շղթայի կառուցվածքով։
Օրինակ՝ բութան և մեթիլպրոպան,C4H10
- CH3CH2CH2CH3-բութան
- CH3CH(CH3)2-2-մեթիլպրոպան
- 2.Տեղակալիչի դիրքի իզոմերիա։ Օրինակ՝ C4H9J
- CH3CJHCH2CH3-2-յոդբութան
- JCH2CH2CH2CH3-1-յոդբութան
- 3.Ֆունկցիոնալ իզոմերիա, որը պայմանավորված է տարբեր ֆունկցիոնալ խմբերի առկայությամբ՝ օրինակ, դիմեթիլեթեր և էթանոլ,C2H6O
- CH3OCH3-դիմեթիլեթեր
- C2H5OH-էթանոլ
- 4.Մետամերիա։ Իզոմերիայի այս տեսակը պայմանավորված է ֆունկցիոնալ խմբի պոլիվալենտ ատոմի հետ կապված նույն հոմոլոգիական շարքին պատկանող տարբեր ալիլ ռադիկալներով։
Օրինակ՝ C2H5OC2H5 CH3OCH(CH3)2
- Տաուտոմերիա։ Իզոմերիայի այս ձևը իրականանում է շնորհիվ շարժուն ջրածնի և կոչվում է դինամիկ իզոմերիա։ Տաուտոմերները անընդհատ կարող են անցնել մեկը մյուսի։ Օրինակ ացետոքացախաթթվային էսթերը փոխազդում է և որպես կետո միացություն և որպես չհագեցած հիդրօքսիմիացություն։ Դա պայմանավորված է նրանով, որ տվյալ միացությունը հանդես է գալիս երկու իզոմեր ձևերով՝ ացետոքացախաթթվային եթերի կետո- և ենոլային ձևերով՝
CH3-CO-CH2-CO-O-C2H5-կետո ձև
CH3-C(OH)=CH-CO-O-C2H5-ենոլ ձև

Ստերեոիզոմերիա, կոնֆիգուրացիա, կոնֆորմացիա[խմբագրել | խմբագրել կոդը]
Ստերեիզոմերներ են կոչվում այն միացությունները, որոնք ունեն նույն մոլեկուլային կառուցվածքը (կապերի և ատոմների հաջորդականությունը) և տարբերվում են միայն միմյանց հետ կապ չունեցող ատոմների տարածական դասավորվածությամբ[3]։
Ստերեոիզոմերները իրենց հերթին կարող են լինել կոնֆիգուրացիոն և կոնֆորմացիոն տիպի։ «Կոնֆիգուրացիա» տերմինը նշանակում է, որ հայտնի կառուցվածք ունեցող մոլեկուլում գոյություն ունի ատոմների և կապերի որոշակի հաջորդականություն, որը պայմանավորված չէ մոլեկուլի հատվածների պտույտով պարզ C-C կապերի շուրջը։ Կոնֆիգուրացիան տվյալ մոլեկուլում ատոմների որոշակի տարածական դասավորությունն է, օրինակ՝ sp3-քառանիստ կոնֆիգուրացիա,sp 2-հարթ կոնֆիգուրացիա։
Տարբեր կոնֆիգուրացիա ունեցող իզոմերները կոչվում են կոնֆիգուրացիոն իզոմերներ, օրինակ՝ D- և L- գլիցերինային ալդեհիդները, ցիս- և տրանս-բութենները։



«Կոնֆորմացիա» տերմինը նշանակում է հայտնի կոնֆիգուրացիա ունեցող մոլեկուլի կազմի մեջ մտնող ատոմների կամ ատոմների խմբերի տարածական զանազան դիրքորոշում, որը պայմանավորված է պտույտով մեկ կամ մի քանի պարզ կապերի շուրջը, օրինակ, բութանի շեղված (գոշ) և արգելակված (անտի) կոնֆորմացիաները։

Խիրալություն[խմբագրել | խմբագրել կոդը]
Հայտնի են բազմազան օրինակներ, երբ երկու առարկա միմյանց համար հանդիսանում են հայելապատկեր, օրինակ, աջ և ձախ ձեռքը, աջ և ձախ բյուրեղը և այլն։ «Խիրալություն» տերմինը օգտագործում են այն դեպքում, երբ երկու առարկա գտնվում են նման հարաբերության մեջ։ Մոլեկուլների այդպիսի զույգերը կոչվում են էնանթիոմերներ։ Մոլեկուլները երկրաչափական մարմիններ են, որոնց համար կարելի է կիրառել սիմետրիայի հատկությունները։ Սիմետրիայի հիմնական տարրերն են սիմետրիայի առանցքը, սիմետրիայի հարթությունը և սիմետրիայի կենտրոնը։
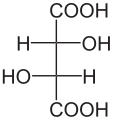
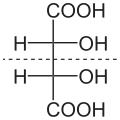
Մոլեկուլները, որոնք ունեն սիմետրիայի տարրեր (առանցք, հարթություն կամ կենտրոն) օժտված են արտացոլման սիմետրիայով և կոչվում են ախիրալ։ Այդպիսի մոլեկուլները չեն կարող կազմել էնանթիոմեր զույգեր և օպտիկական ակտիվություն չեն ցուցաբերում։ Օրինակ, մեզոգինեթթուն։ Սիմետրիայի տարրեր չունեցող մոլեկուլները կոչվում են խիրալ։ Այս միացությունները չեն համընկնում իրենց հայելապատկերի հետ և կարող են գոյություն ունենալ էնանթիոմեր զույգերի ձևով.
-
L(−)-Գինեթթու
-
D(+)-Գինեթթու
-
Մեզոգինեթթու
Սիմետրիայի բացակայությունը պայմանավորված է տվյալ միացություններում ասիմետրիկ ածխածինների, կամ խիրալ կենտրոնների, առկայությամբ։ Այդպես են անվանում ածխածնի այն ատոմները, որոնց չորս կապերը առաջացած են տարբեր ռադիկալների հետ։ Ասիմետրիկ ածխածին պարունակող միացությունները հարթության վրա պատկերելու համար օգտագործում են Ֆիշերի պրոյեկցիոն բանաձևերը։ Այս բանաձևերում ածխածնային շղթան հարթության վրա տեղադրվում է ուղղահայած դիրքով այնպես, որ ավագ խումբը գտնվի վերևում։ Ուղղահայած և հորիզոնական գծերի հատման կետերը համապատասխանում են ասիմետրիկ ածխածիններին, այդ ածխածինները չեն գրվում։ Օրինակ.
Ասիմետրիկ ածխածին պարունակող միացությունները հիմնականում օպտիկապես ակտիվ են։ Օպտիկապես ակտիվ են կոչվում այն միացությունները, որոնք պտտում են բևեռացված լույսի հարթությանը։ Անհրաժեշտ է նշել, որ ոչ բոլոր ասիմետրիկ կենտրոն ունեցող միացություններն են խիրալ և օժտված օպտիկական ակտիվությամբ։ Այն դեպքում, երբ ասիմետրիկ ածխածին պարունակող միացություններում գոյություն ունի սիմետրիայի հարթություն, մոլեկուլը ախիրալ է (մեզոգինեթթու, ցիստին և այլն)։
Բացարձակ և հարաբերական կոնֆիգուրացիա[խմբագրել | խմբագրել կոդը]
Բոլոր խիրալ կենտրոն ունեցող միացությունները ընդունված է բաժանել երկու ստերեոքիմիական շարքերի՝ D և L։ Օրգանական միացությունների բացարձակ կոնֆիգուրացիան դա տեղակալիչների իրական տարածական դասավորվածությունն է խիրալ կենտրոնի շուրջը, որը որոշվում է ճշգրիտ, մասնավորապես ռենտգենոկառուցվածքային անալիզի եղանակով։ Սակայն, որոշելով մի շարք հանգուցային միացությունների, որոնք հայտնի են այժմ որպես էտանոլային միացությունների, բացարձակ կոնֆիգուրացիաները, ապա համեմատելով անհայտ կոնֆիգուրացիա ունեցող միացության հետ, կարելի է որոշել վերջինիս հարաբերական կոնֆիգուրացիան։ Մինչ ճշգրիտ եղանակների ի հայտ գալը, որպես կոնֆիգուրացիոն էտալոն էին ընդունվել D(+) և L(-)-գլիցերինային ալդեհիդները։D-ստերեոքիմիական շարքին են պատկանում խիրալ կենտրոնի այնպիսի կոնֆիգուրացիա ունեցող միացությունները, որոնցում ֆունկցիոնալ խմբերը (OH,NH2,հալոգենները) Ֆիշերի պրոյեկցիաներում գտնվում են ուղղահայաց գծից աջ, իսկ L-շարքին-ձախ։
Օրինակ՝

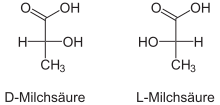
Այժմ բավականին հաճախ D,L համակարգի փոխարեն կիրառվում է R,S-նոր ստերեոքիմիական անվանակարգը, որը հիմնված է խիրալ կենտրոնի մոտ գտնվող տեղակալիչների ավագության նվազման ուղղության վրա (տեղակալիչների ավագությունը որոշվում է խիրալ կենտրոնի հետ կապված տարրի ատոմական համարով)։
Մեկ ասիմետրիկ ածխածին պարունակող միացությունը կարող է հանդես գալ երկու ստերեոիզոմերների ձևով։ Ստերեոիզոմերների թիվը որոշվում է 2n բանաձևով, որտեղ n-ը ասիմետրիկ ածխածինների թիվն է։
Կոնֆիգուրացիոն ստերեոիզոմերները բաժանվում են էնանթիոմերների և դիաստերեոմերների։
Մոլեկուլները, որոնք ունեն նույն կառուցվածքային բանաձևերը, իսկ բոլոր խիրալ կենտրոնների կոնֆիգուրացիաները հակառակն են (միմյանց հայելապատկերն են),կոչվում են էնանթիոմերներ։
Էնանթիոմերներ են D(+) և L(-) գլիցերինային ալդեհիդները,D և L կաթնաթթուները,D և L գլյուկոզները և այլն։ Էնանթիոմերները ունեն նույն քիմիական և ֆիզիկական հատկությունները, բացառությամբ բևեռացված լույսի հարթության պտտման ուղղությունից (պտտման անկյունը նույնն է)։ Աջ պտտող էնանթիոմերները ստանում են (+),իսկ ձախ պտտողները՝ (-) նշանը։ Էնանթիոմերների էկվիմոլային խառնուրդը կոչվում է ռացեմատ։ Ռացեմատները օպտիկապես ակտիվ չեն, քանի որ երկու էնանթիոմերների էֆեկտները կոմպեսում (մարում) են միմյանց։ Պտտման ուղղությունը (նշանը) և աստիճանը (մեծությունը) որոշվում է փորձնական ճանապարհով։
Դիաստերեոմերներ։ Բոլոր ստերեոիզոմերները, որոնք էնանթիոմեր չեն, կոչվում են դիաստերեոմերներ, որոնք նույն կառուցվածքային բանաձևը, բայց տարբերվում են միմյանցից խիրալ կենտրոնների կոնֆիգուրացիայով։ Դիաստերեոմերիայի մասնավոր դեպք է էպիմերիան, երբ իզոմերները տարբերվում են միայն մեկ խիրալ կենտրոնի կոնֆիգուրացիայով։ Դիաստերեոմերները տարբերվում են իրենց ֆիզիկաքիմիական հատկություններով։
Կոնֆորմացիոն իզոմերներ։ Բաց շղթայով միացությունների կոնֆորմացիաները[խմբագրել | խմբագրել կոդը]
Ինչպես վերը նշեցինք, ատոմների տարբեր տարածական դասավորվածության հետևանքով, որը առաջանում է պարզ կապերի շուրջ կատարվող պտույտի ժամանակ, առաջանում են կոնֆորմացիոն իզոմերներ (կոնֆորմերներ)։ Կոնֆորմացիոն իզոմերները ընդունված է պատկերել Նյումենի բանաձևերով, որոնց վրա նշվում են տեղակալիչների դիրքերը C-C կապերի շուրջ պտույտ կատարելու դեպքում։ Էթանի օրինակի վրա քննարկենք հնարավոր կոնֆորմերների թիվը, ընդունելով մինիմալ պտույտը հավասար 60°։ Կոնֆորմացիաները, որոնցում տեղակալիչները գտնվում են միմյանց դիմաց (պտտման աստիճանը 0°, կամ 360°), առավել մոտ դիրքում, օժտված են բարձր էներգիայով և կոչվում են «ծածկված»։ Կոնֆորմացիաները, որոնցում տեղակալիչները գտնվում են առավել մեծ հեռավորության վրա (պտտման անկյունը 180°), գտնվում են ցածր էներգետիկ մակարդակի վրա և կոչվում են «արգելակված»։

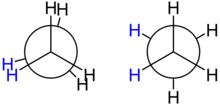
Էթանի ծածկված կոնֆոմացիայի պոտենցիալ էներգիան 12կՋ/մոլ-ով բարձր է, քան արգելակվածինը։ Դա պայմանավորված է հարևան դիրքերում գտնվող կապերի էլեկտրոնների միջև առաջացող վանող ուժերով, որի հետևանքով զարգանում է այսպես կոչված տորսիոն լարվածություն։ Էթանի տարբեր կոնֆորմերների էներգետիկ մակարդակների տարբերությունը մեծ չէ և սովորական պայմաններում մեկ կոնֆերմերը հեշտությամբ անցնում է մյուսի։ Բութանի մոտ տորսիոն լարվածությանը գումարվում է ևս մեկը, որը առաջանում է մեթիլ խմբերի փոխադարձ վանման հետևանքով և կոչվում է Վան-դեր-Վալսի լարվածություն։ Այս դեպքում համակարգի լարվածությունը ավելի մեծ է։ Հետևաբար մոլեկուլները ձգտում են ընդունել այնպիսի կոնֆորմացիա, որի դեպքում առավել կայուն են։

Էներգետիկ առումով միջին դիրք գրավող կոնֆորմացիաները կոչվում են շեղված, կամ գոշ-կոնֆորմացիաներ։
Ցիկլիկ միացությունների կոնֆորմացիաներ[խմբագրել | խմբագրել կոդը]
Ցիկլոալկաններում, տորսիոն և Վան-դեր-Վալսի լարվածությանը գումարվում է Բայերի անկյունային լարվածությունը։ Վերջինս պայմանավորված է ցիկլում վալենտային անկյունների շեղումով՝ նորմալ տետրաէդրի անկյունից։ Օրինակ, առավել պարզ ներկայացուցչի, ցիկլոպրոպանի վալենտային անկյունները կազմում են 60°, որի հետևանքով առաջանում է մեծ լարվածություն։


Ցիկլոպրոպանում պտույտ C-C կապերի շուրջ չի կատարվում, և ջրածնի բոլոր ատոմները գտնվում են ծածկված դիրքում։ Հետևաբար, ցիկլոպրոպանը չունի կոնֆորմերներ։ Ելնելով վերը նշվածից, հասկանալի է, որ եռանդամ ցիկլը անկայուն է։ Հաջորդ ներկայացուցիչը ցիկլոբութանն է, որի վալենտային անկյունները հավասար են 90°։ Ջրածնի ատոմները գտնվում են ծածկված դիրքում։ Բարձր տորսիոն և անկյունային լարվածության հետևանքով քառանդամ ցիկլը նույնպես անկայուն է։
Ցիկլոպենտանի համար հայտնի է երկու կոնֆորմեր, հարթ ձևի մոտ բացակայում է անկյունային լարվածությունը, քանի որ վալենտային անկյունները հավասար են 108°, որը մոտ է նորմալ արժեքին։ Սակայն հարթ ձևի մոտ ուժեղ է դրսևորվում տորսին լարվածությունը (ծածկման լարվածությունը),որը ծրարի կոնֆորմացիայի դեպքում ավելի ցածր է։


-
Ցիկլոհեքսանի նավակը
-
Ցիկլոհեքսանի բազկաթոռ
Ցիկլոհեքսանում անկյունները հավասար են 120°։ Սրա համար հայտնի են մի շարք կոնֆորմերներ, որոնցից ավելի ցածր լարվածություն ունեն մի քանի որ հարթ, այսպես կոչված, նավակ, բազկաթոռ և զեթաձև կոնֆորմերները։


Նյումենի պրոյեկցիոն բանաձևերը հնարավորություն են տալիս հստակ պատկերացնել ատոմների փոխադարձ դիրքը։ Առանցքին զուգահեռ կապերը կոչվում են աքսիալ, իսկ 109,28° անկյան տակ գտնվողներինը՝ էկվատորիալ։


Ցիկլոհեքսանի բազկաթոռի կոնֆորմացիայում ջրածնի ատոմների դիրքը նույնն է, ինչ էթանի արգելակված կոնֆորմացիայում, իսկ ածխածինները՝ բութանի շեղված կոնֆորմացիայում։ Նավակ կոնֆորմացիայի դեպքում C-2,C-3,C-5,C-6 ածխածինների մոտ գտնվող ջրածինների ծածկված դիրքի շնորհիվ, ցիկլի լարվածությունը մեծ է։ Հետևաբար, բազկաթոռ կոնֆորմերը էներգետիկ տեսակետից ավելի շահավետ է։
Տես նաև[խմբագրել | խմբագրել կոդը]
Գրականություն[խմբագրել | խմբագրել կոդը]
- Физер Л., Физер М., Органическая химия. Углубленный курс. т. 1. пер с англ., Под ред. д.х.н. Н. С. Вульфсона. Изд. «Химия». М., 1969.
- Пальм В. А., Введение в теоретическую органическую химию, М., 1974;
- Соколов В И., Введение в теоретическую стереохимию, М., 1979;
- Сланина 3., Теоретические аспекты явления изомерии в химии, пер. с чеш., М., 1984;
- Потапов В М., Стереохимия М., 1988.
- Большой энциклопедический словарь. Химия. Изд.։ Большая Российская энциклопедия, 2003, ISBN 5-85270-253-6
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Petrucci R.H., Harwood R.S. and Herring F.G. "General Chemistry" (8th ed., Prentice-Hall 2002), p.91
- ↑ Smith, Janice Gorzynski. General, Organic and Biological Chemistry. The McGraw-Hill Companies. 1st ed 2010. pg. 450
- ↑ IUPAC definition of cis and trans
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 4, էջ 314)։ |