Կոնֆիգուրացիա (քիմիա)
Ստերեոիզոմերիա,կոնֆիգուրացիա[խմբագրել | խմբագրել կոդը]
Ստերեոիզոմերները իրենց հերթին կարող են լինել կոնֆիգուրացիոն և կոնֆորմացիոն տիպի։ «Կոնֆիգուրացիա» տերմինը նշանակում է, որ հայտնի կառուցվածք ունեցող մոլեկուլում գոյություն ունի ատոմների և կապերի որոշակի հաջորդականություն, որը պայմանավորված չէ մոլեկուլի հատվածների պտույտով պարզ C-C կապերի շուրջը։ Կոնֆիգուրացիան տվյալ մոլեկուլում ատոմների որոշակի տարածական դասավորությունն է, օրինակ՝ sp3-քառանիստ կոնֆիգուրացիա,sp 2-հարթ կոնֆիգուրացիա[1]։.
Տարբեր կոնֆիգուրացիա ունեցող իզոմերները կոչվում են կոնֆիգուրացիոն իզոմերներ, օրինակ՝ D- և L- գլիցերինային ալդեհիդները, ցիս- և տրանս-բութենները։



Բացարձակ և հարաբերական կոնֆիգուրացիա[խմբագրել | խմբագրել կոդը]
Բոլոր խիրալ կենտրոն ունեցող միացությունները ընդունված է բաժանել երկու ստերեոքիմիական շարքերի՝ D և L։ Օրգանական միացությունների բացարձակ կոնֆիգուրացիան դա տեղակալիչների իրական տարածական դասավորվածությունն է խիրալ կենտրոնի շուրջը, որը որոշվում է ճշգրիտ, մասնավորապես ռենտգենոկառուցվածքային անալիզի եղանակով։ Սակայն, որոշելով մի շարք հանգուցային միացությունների, որոնք հայտնի են այժմ որպես էտանոլային միացությունների, բացարձակ կոնֆիգուրացիաները, ապա համեմատելով անհայտ կոնֆիգուրացիա ունեցող միացության հետ, կարելի է որոշել վերջինիս հարաբերական կոնֆիգուրացիան։ Մինչ ճշգրիտ եղանակների ի հայտ գալը, որպես կոնֆիգուրացիոն էտալոն էին ընդունվել D(+) և L(-)-գլիցերինային ալդեհիդները։D-ստերեոքիմիական շարքին են պատկանում խիրալ կենտրոնի այնպիսի կոնֆիգուրացիա ունեցող միացությունները, որոնցում ֆունկցիոնալ խմբերը (OH,NH2,հալոգենները) Ֆիշերի պրոյեկցիաներում գտնվում են ուղղահայաց գծից աջ, իսկ L-շարքին-ձախ։
Օրինակ՝

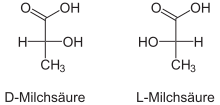
Այժմ բավականին հաճախ D,L համակարգի փոխարեն կիրառվում է R,S-նոր ստերեոքիմիական անվանակարգը, որը հիմնված է խիրալ կենտրոնի մոտ գտնվող տեղակալիչների ավագության նվազման ուղղության վրա (տեղակալիչների ավագությունը որոշվում է խիրալ կենտրոնի հետ կապված տարրի ատոմական համարով)։
Մեկ ասիմետրիկ ածխածին պարունակող միացությունը կարող է հանդես գալ երկու ստերեոիզոմերների ձևով։ Ստերեոիզոմերների թիվը որոշվում է 2n բանաձևով, որտեղ n-ը ասիմետրիկ ածխածինների թիվն է։
Կոնֆիգուրացիոն ստերեոիզոմերները բաժանվում են էնանթիոմերների և դիաստերեոմերների։
Մոլեկուլները, որոնք ունեն նույն կառուցվածքային բանաձևերը, իսկ բոլոր խիրալ կենտրոնների կոնֆիգուրացիաները հակառակն են (միմյանց հայելապատկերն են),կոչվում են էնանթիոմերներ։
Էնանթիոմերներ են D(+) և L(-) գլիցերինային ալդեհիդները,D և L կաթնաթթուները,D և L գլյուկոզները և այլն։ Էնանթիոմերները ունեն նույն քիմիական և ֆիզիկական հատկությունները, բացառությամբ բևեռացված լույսի հարթության պտտման ուղղությունից (պտտման անկյունը նույնն է)։ Աջ պտտող էնանթիոմերները ստանում են (+),իսկ ձախ պտտողները՝ (-) նշանը։ Էնանթիոմերների էկվիմոլային խառնուրդը կոչվում է ռացեմատ։ Ռացեմատները օպտիկապես ակտիվ չեն, քանի որ երկու էնանթիոմերների էֆեկտները կոմպեսում (մարում) են միմյանց։ Պտտման ուղղությունը (նշանը) և աստիճանը (մեծությունը) որոշվում է փորձնական ճանապարհով։
Դիաստերեոմերներ։ Բոլոր ստերեոիզոմերները, որոնք էնանթիոմեր չեն, կոչվում են դիաստերեոմերներ, որոնք նույն կառուցվածքային բանաձևը, բայց տարբերվում են միմյանցից խիրալ կենտրոնների կոնֆիգուրացիայով։ Դիաստերեոմերիայի մասնավոր դեպք է էպիմերիան, երբ իզոմերները տարբերվում են միայն մեկ խիրալ կենտրոնի կոնֆիգուրացիայով։ Դիաստերեոմերները տարբերվում են իրենց ֆիզիկաքիմիական հատկություններով։
Գրականություն[խմբագրել | խմբագրել կոդը]
- Физер Л., Физер М., Органическая химия. Углубленный курс. т. 1. пер с англ., Под ред. д.х.н. Н. С. Вульфсона. Изд. «Химия». М., 1969.
- Пальм В. А., Введение в теоретическую органическую химию, М., 1974;
- Соколов В И., Введение в теоретическую стереохимию, М., 1979;
- Сланина 3., Теоретические аспекты явления изомерии в химии, пер. с чеш., М., 1984;
- Потапов В М., Стереохимия М., 1988.
- Большой энциклопедический словарь. Химия. Изд.։ Большая Российская энциклопедия, 2003, ISBN 5-85270-253-6
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ «IUPAC Gold Book - enantiomer». Արխիվացված է օրիգինալից 2013 թ․ փետրվարի 11-ին. Վերցված է 2013 թ․ փետրվարի 4-ին.
