«Պոլոնիում»–ի խմբագրումների տարբերություն
No edit summary |
No edit summary |
||
| Տող 1. | Տող 1. | ||
[[Պատկեր: |
[[Պատկեր:alpha po lattice.jpg|մինի|Պոլոնիում]] |
||
{{Նշան|Po}} |
{{Նշան|Po}} |
||
'''Պոլոնիում''', քիմիական տարր է, որի նշանն է ''Po'' և ատոմային թիվը՝ 84։ |
'''Պոլոնիում''', քիմիական տարր է, որի նշանն է ''Po'' և ատոմային թիվը՝ 84։ |
||
12:08, 23 Հունիսի 2015-ի տարբերակ
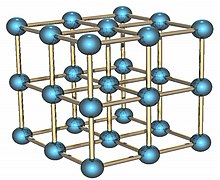
Պոլոնիում, քիմիական տարր է, որի նշանն է Po և ատոմային թիվը՝ 84։
Պոլոնիումը քիմիական տարր է, որի քիմիական նշանն է Po, իսկ կարգատիվը՝84: Տարրը հայտնաբերվել է 1898 թվականին Մարի Կուրիի և Պիեր Կուրիի կողմից: Այն հազվադեպ հանդիպվող և շատ ռադիոակտիվ տարր է, որը չունի լրացված շերտերով իզոտոպներ: Պոլոնիումը քիմիապես նման է բիզմիթին և Թելուրին ու հանդիպվում է ուրանի հանքաքարերում:
Պոլոնիումի կիրառությունները քիչ են: Այն օգտագործվում է տիեզերագնաց և հակաստատիկ սարքերի պատրաստման մեջ: Նաև հանդիսանում է նեյրոնների և ալֆա մասնիկների աղբյուր:
Պարբերական աղյուսակում իր դիրքի պատճառով Պոլոնիումը երբեմն դասվում է որպես մետաղանման, բայց նրա հատկությունները և պահվացքը փաստում են, որ այն միանշանակ մետաղ է:
Հատկություններ
Իզոտոպներ
Պոլոնիումը ունի 33 հայտնի իզոտոպներ, որոնք բոլորը ռադիոակտիվ են: Նրանց հարաբերական ատոմային զանգվածները տատանվում են 188-ից 220: 210Po-ը (կես կիանք-138.376 օր) և բոլոր իզոտոպներից ամենատարածվածն է: Իսկ ամենաերկարակյաց իզոտոպը 209Po-ը (կես կյանք125.2 ± 3.3 տարի) և 208Po-ը (կես կյանք 2.9 տարի):
208Po-ը կարող է ստացվել հատուկ անօդի մեջ կապարի կամ բիզմիթի ալֆա,պրոտոն կամ դուտրոն ռմբակոծումից: Պինդ վիճակ
Պոլոնիումը ռադիոակտիվ տարր է, որը գոյություն ունի երկու մետաղական ալոտրոպներում: Ալֆա վիճակը պարզ խորանարդային կառուցվացքի միակ հայտնի օրինակն է մեկ ատոմի դեպքում, որի գագաթնային չափսերն են 335.2 պիկոմետր է, իսկ բետա վիճակը ռոմբոջրային: Պոլոնիումի կառուցվացքը բնութագրվել է ռենտգենյան ճառադայթների և էլեկտրոնների օգնությամբ:
Միացություններ
Պոլոնիումը չունի հասարակ միացություններ և իր գրեթե բոլոր միացությունները արհեստականորեն են պատրաստվում: Այդ միացություններիցավելի քան 50-ը ճանաչված են: Պոլոնիումի ամենակայուն միացությունները պոլոնիդներն են, որոնք պատրաստվում են երկու տարրերի անմիջական փոխազդեցությունից: Na2Po-ը ունի անտիֆլոռիտ կառուցվացքը, Ca, Ba, Hg, Pb տարրերի պոլոնիդների և լանթինադների փոխազդեցությունից առաջանում է NaCl-ի ցանցեր, իսկ BePo-ը և CdPo-ը ունեն ուըրտզիտ և MgPo-ը նիկել արսենիդ կառուցվացքը:
Պատմություն
Փորձնականորեն Ռադիում Էֆ անվանված պոլոնիումը հայտնաբերել է Մարի Կուրին 1898 թվականին և այն անվանվել է իր հայրենիքի` Հոլանդիայի անունով(Poland): Այդ ժամանակ Հոլանդիան ռուսասական, գերմանական և Ավստրո-Հունգարական բաժանմունքի տակ էինև գոյություն չունեին րպես անկախ երկիր: Կուրին հույս ուներ, որ տարրը իր հայրենիքի անունով անվանելով՝ հայտնի կդառնար իրենց երկրում անկախության պակասը: Այն առաջին տարրն էր, որիանվանումը օգնեց կարևորել քաղաքական հակասություններ:
Այս տարրը Կուրիների կողմից հայնաբերված առաջին տարրն էր:Այն հայտնաբերվեց երբ նրանք ուսումնասիրում էին Փիչբլենդ ռադիոակտիվության պատճառը: Փիչբլենդի միջից ռադիոակտիվ տարրերը՝ ուրանը ու թորիումը հանելուց հետո, ավելի ռադիոակտիվ է քան ուրանը ու թորիումը միասին: Այս գաղափարը ստիպեց Կուրիներին հայթհայթել նոր ռադիոակտիվ տարրեր: 1898 թվականի հուլիսին նրանք փիչբլենդը առանձնացրեցին պոլոնիումից, և հինգ ամիս հետո նաև մեկուսացրեցին ռադիումը:
Տարածվածությունը և Արտադրությունը
Պոլոնիումը շատ հազվադեպ է հանդիպվում բնության մեջ, քանի որ իր բոլոր իզոտոպները ունեն շատ կարճ կես-կյանք: 210Po, 214Po, և 218Po գոյություն ունեն փտած 238U-ի մեջ:
Կիրառությունը
Պոլոնիումային հիմքով ալֆա մասնիկների աղբյուրները առաջացել էին ԽՍՀՄ-ում: Այսպիսի աղբյուրներ օգտագործվում էին արդյունաբերական ծածկույթների հաստությունը որոշելու համար:
Տե՛ս նաև
| Պարբերական աղյուսակ | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
