Հոդատապ
| Հոդատապ | |
|---|---|
 | |
| Տեսակ | հիվանդության կարգ և ախտանիշ կամ նշան |
| Հիվանդության ախտանշաններ | Հոդացավ[1], joint effusion?[1], կարմրություն[1] և այտուց |
| Վնասում է | մարդ և տղամարդ[2] |
| Օժանդակող գործոն | գենետիկա[3], Դիետա[3] և Ճարպակալում[3] |
| Բժշկական մասնագիտություն | ռևմատոլոգիա և ներքին հիվանդություններ |
| Անվանվել է | drop? և թակարդում |
Հոդատապ կամ պոդագրա, պուրինի նյութափոխանակության խանգարման հետևանքով զարգացող հիվանդություն, որի ժամանակ հիմնականում հոդերում առաջանում են միզաթթվային բյուրեղներ, նրանց նկատմամբ օրգանիզմի բուռն հակազդումով։
Եվրոպայում և ԱՄՆ-ում հոդատապի հանդիպման հաճախականությունը կազմում է ընդհանուր հիվանդությունների 0.3%-ը։ Նշանակություն ունեն ինչպես ժառանգական, այնպես էլ սննդային գործոնները։ Տարածվածությունը կախված է սննդային սովորություններից։ Հիմնականում հիվանդանում են 30 տարեկանն անց տղամարդիկ։
Պատմական տեղեկություններ
[խմբագրել | խմբագրել կոդը]Հիվանդությունը հայտնի էր դեռ վաղ անցյալում։ Առաջին նկարագրությունները պատկանում են Հիպոկրատին։ Միզաթթուն երիկամային քարերում հայտնաբերվել է 1976 թ.-ին Կ. Շեելեի կողմից, իսկ 1798 թ. Վ. Վոլլաստոնը և Ա. Լաֆֆը այն հայտնաբերեցին հոդատապային տոֆուսներում։ 1848 թ. Ա. Գերրոդը հայտնաբերեց հիպերուրիկեմիան հոդատապի ժամանակ։ 1899 թ. Մ. Ֆրեդվեյլերը հաստատեց նատրիումի ուրատի բյուրեղների դերը հոդատապի ժամանակ դիտվող հոդաբորբերի ախտածագման հարցում։ 1932 թ. Ջ. Ջեննինգսը հաստատեց սալիցիլատների ուրիկոզուրիկ ազդեցությունը, իսկ 1963 թ. սինթեզվեց ալոպուրինոլը։
Ախտածագումը և ախտահյուսվացքաբանությունը
[խմբագրել | խմբագրել կոդը]Հոդատապը կարող է հանդիպել մի շարք ձևերով, չնայած ամենատարածվածը հոդատապային հոդաբորբի խրոնիկական սուր նոպաներով ընթացքն է (մաշկի կարմրածություն, արտահայտված ցավ, բորբոքված վիճակ, հոդերի այտուցվածություն)։ Ոտնաթաթի բութ մատի հիմքի նախագարշապար-մատնոսկրային հոդը ամենահաճախ ախտահարվող հատվածն է, որն արձանագրվում է դեպքերի կեսում։ Այլ հոդեր, ինչպիսիք են կրունկները, արմունկները և ծնկները, դաստակները և ձեռքի մատները, նույնպես կարող են ախտահարվել։ Հոդացավերը սովորաբար սկսում են գիշերային ժամերին՝ 2–4 ժամվա ընթացքում։ Գիշերային ակտիվության պատճառը մարմնի ավելի ցածր ջերմաստիճանային ռեժիմն է։ Այլ հազվադեպ ախտանշաններն են հոդացավերը, ինչպես նաև հիվանդի շուտ հոգնելը և բարձր ջերմային տենդը։
Սակայն նույնիսկ այսօր չի կարելի ասել, որ հոդատապի ախտածագումը ուսումնասիրված է լիովին։ Ապացուցված է օրգանիզմում միզաթթվի աղերի կենսաստեղծումը խանգարող ժառանգական ֆերմենտոպաթիայի դերը։ Ուրատների հավելուրդային գոյացմանը նպաստում է գերսնումը, ալկոհոլի չարաշահումը, սննդի մեջ պուրիններով հարուստ սննդամթերքների օգտագործումը։ Նշանակություն ունի նաև երիկամներով ուրատների դուրս բերման խանգարումը։ Ըստ այդմ տարբերում են հոդատապի նյութափոխանակային ձևը, երբ բարձր է ուրատների կենսաստեղծման մակարդակը, և երիկամային ձև, երբ խանգարված է ուրատբերի դուրսբերումը։ Բնականաբար կա նաև խառը ձև, երբ նշված երկու գործընթացներն էլ առկա են։ Բացի առաջնային հոդատապից տարբերում են նաև երկրորդային, երբ հիպերուրիկեմիան կապված է օրգանիզմում նուկլեինաթթուների բարձր քայքայման հետ։ Դա դիտվում է արյան հիվանդությունների, ուռուցքների ժամանակ, ծանր վիրահատություններից հետո, որոշ թունավորումների պարագայում, օրինակ՝ կապարային։ Հիպերուրիկեմիայից բացի հոդատապի ժամանակ հաճախ դիտվում են լիպիդային նյութափոխանակության խանգարումներ, ինչի կապակցությամբ հոդատապող տառապողները հաճախ նախատրրամադրված են շաքարախտին, ճարպակալմանը և սրտի իշեմիկ հիվանդությանը։
Հոդատապի ժամանակ նատրիումի մոնոուրատի բյուրեղները նստում են ձուսպաթաղանթներում, աճառներում և ոսկրերի հոդային հատվածներում, ջլերում, աչքի եղջրաթաղանթում, երիկամների միջանկյալ հյուսվածքում, անոթներում։ Ուրատների բյուրեղների գոյացման ժամանակ զարգանում են սուր հոդատապային նոպաներ և առաջանում են հոդատապային տոֆուսներ։ Սուր հոդատապային նոպայի մեխանիզմը կապում են բյուրեղների ֆագոցիտոզի հետ, ինչի հետևանքով պոլիմորֆ կորիզային լեյկոցիտներից ազատվում են մեծ քանակությամբ լիզոսոմային ֆերմենտներ, որոնք առաջացնում են հյուսվածքների կազմալուծում։ Ապացուցված է նաև իմուն մեխանիզմների ներգրավվումը, մանավանդ հոդատապային գլոմերուլոնեֆրիտի դեպքում։
Հիպերուրիկեմիան հանդիսանում է հոդատապի ծագման հիմնական պատճառներից մեկը։ Այն կարող է առաջանալ մի շարք, ներառյալ սննդակարգի, գենետիկական նախատրամադրվածության կամ ուրատ, միզաթթվի աղային կուտակումների[4] կենսաստեղծման հետևանքով։ Միզաթթվի ոչ բավարար քանակությամբ արտազատումը երիկամներից, մոտ 90% դեպքերում, հիպերուրիկեմիայի ախտածագման գլխավոր պատճառն է, մինչդեռ միզաթթվի հավելուրդային արտադրությունը հոդատապի առաջացման պրակտիկայում 10%-ից ցածր ցուցանիշ ունի[5] Հիպերուրիկեմիայով հիվանդ մարդկանց մոտ 10%-ը իրենց կյանքի ընթացքում հիվանդանում են հոդատապով[6]։ Հավանականությունն, այնուամենայնիվ, կախված է հիպերուրիկեմիայի աստիճանից։ Երբ վերջինիս մակարդակը 415-ից 530 Միկրոմոլ/լիտր (7 և 8.9 Միլիգրամ/դեկալիտր) է, հավանականությունը տարեկան 0.5% է կազմում, մինչդեռ 535 Միկրոմոլ/լիտր (9 Միլիգրամ/դեկալիտր), ից բարձր մակարդակի առկայության դեպքում, հավանականությունը 4.5% է տարեկան[7]։
Կենսակերպը
[խմբագրել | խմբագրել կոդը]Հոդատապի ախտածագման մոտ 12%-ը բաժին է ընկնում սննդակարգին[4] և սերտորեն փոխկապակցված է ալկոհոլի, ֆրուկտոզա-քաղցրացված խմիչքների, մսամթերքի և ծովային մթերքների օգտագործման հետ[8][9]։ Այլ նպաստող գործոններ կարող են հանդիսանալ վնասվածքները և վիրահատությունները[5] Վերջին հետազոտությունները ցույց են տալիս, որ մինչ այժմ սննդակարգի գործոնի կարծեցյալ ազդեցություններն անհիմն են, ներառյալ պուրիններով հարուստ բանջարեղենի (օրինակ, լոբազգիների, սիսեռի, ոսպի և սպանախի) և սպիտակուցներով հարուստ սննդամթերքի օգտագործման սահմանափակումները[10][11]։ Սուրճի, վիտամին C-ի և կաթնամթերքի-ի օգտագործումը, ինչպես նաև բուժական ֆիզկուլտուրան նվազեցնում են հիվանդության զարգացումը[12][13][14]։ Սա մասամբ բացատրվում է դրանց ինսուլինային դիմադրության նվազեցման էֆեկտով[14]։
Գենետիկան
[խմբագրել | խմբագրել կոդը]Հոդատապի առաջացումը մասամբ գենետիկական ծագում ունի, որտեղ փոփոխականությունը միզաթթվի մակարդակի վրա ազդող գործոնների թվում մոտ 60% է կազմում[5] Երեք գեներ, որոնց անվանումներն են SLC2A9, SLC22A12 և ABCG2, հաճախ համարվում են հոդատապի առաջացման պատասխանատուներ և դրանց համատեղ առկայությունը կրկնակի մեծացնում է հիվանդության հավանականությունը[15][16]։ SLC2A9 և SLC22A12 գեների գործառնության լրիվ կորստի դեպքում ուրատների նվազ ներծծման և ուրատների անարգել սեկրեցիան առաջանում է ժառանգական հիպերուրիկեմիա[16]։ Մի շարք այլ հազվադեպ գենետիկ խանգարումներ, ներառյալ պատանեկան հիպերուրիկեմիկ նեֆրոպաթիան, մեդուլյար երիկամային հիվանդությունը, ֆոսֆորիբոզիլպիրոֆոսֆատի սինթետազ գերակտիվությունը և հիպոքսանտին-գուանինֆոսֆորիբոզիլտրանսֆերեզայի անբավարարությունը, ինչպես Լեյշ-Նայխանի համախտանիշի ժամանակ, հոդատապի ֆոնի վրա բարդանում են[5]։
Հիվանդությունը
[խմբագրել | խմբագրել կոդը]Հոդատապը հաճախ ուղեկցվում է այլ հիվանդությունների հետ։ Մետաբոլիկ սինդրոմը, որովայնային ճարպակալում, հիպերտոնիա, ինսուլինային դիմադրության և ոչ նորմալ լիպիդային արտադրության համատեղ գործողությունը, հանդիպում են մոտավորապես 75% դեպքերում[17] Այլ հիվանդություններ, որոնք բարդանում են հոդատապի հետևանքով, նշված են ստորև. պոլիցիտեմիա, կապարային թունավորում, երիկամային անբավարարություն, հեմոլիտիկ անեմիա, պսորիազ և տրանսպլանտատներ[5][18]։ Մարմնի զանգվածի ինդեքսի 35 և ավելի նիշից բարձր լինելը եռակի մեծացնում է հոդատապով հիվանդանալու հավանականությունը[11] Խրոնիկական կապարային թունավորումն ու կապարային թունավորմամբ ալկոհոլը ռիսկային գործոններ են հոդատապի համար, քանի որ դրանք վնասակար ազդեցություն ունեն երիկամների գործունեության վրա[19]։ Լեյշ-Նայխանի համախտանիշը հաճախ ուղեկցվում է հոդատապային արթրիտով։
Դեղամիջոցները
[խմբագրել | խմբագրել կոդը]Դիուրետիկներն ազդում են հոդատապի նոպաների ընթացքի վրա։ Սակայն, հիդրոքլորտիազիդի փոքր դեղաչափերով վտանգավոր չի համարվում[20] Այլ դեղամիջոցներ, ներառյալ նիացինը և ասպիրինը(ացետիլսալիցիլաթթուն) նույնպես վտանգավոր են[8]։ Իմունոդեպրեսանտներ ցիկլոսպորինը և տակրոլիմուսը ևս վտանգ են ներկայացնում հոդատապի ժամանակ[5], հատկապես վերջինը, երբ նշանակված է հիդրոքլորտիազիդի հետ[21]։
Ախտաբանական ֆիզիոլոգիան
[խմբագրել | խմբագրել կոդը]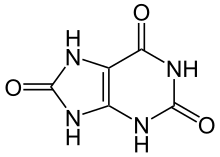
Հոդատապը պուրինի նյութափոխանակության խանգարման հետևանքով զարգացող հիվանդություն է[5] և առաջանում է, երբ այդ նյութափոխանակության արգասիք (մետաբոլիտ) միզաթթուն նատրիումի ուրատի բյուրեղների ձևով ախտահարում է հոդերը, ջլերը և շրջակա հյուսվածքները[8]։ Այս բյուրեղները հետագայում առաջացնում են իմունային համակարգի տեղային բորբոքման հակազդեցություն[8], որը խթանում է բորբոքային շղթայի առանցքային սպիտակուցներից interleukin 1βի արտադրությանը[5]։ Էվոլյուցիայի ընթացքում մարդկանց և բարձր դասի պրիմատների մոտ չգործող միզաթթվի քայքայիչ գենը, որը տրոհում է միզաթթուն այս ֆունկցիան դարձնում է շարունակական[5]։
Միզաթթվի ստեղծման խթանիչ գործոնները չունեն դեռևս լրիվ բացատրություն։ Մինչ բյուրեղացում նկատվում է միզաթթվի նորմալ մակարդակի պայմաններում, այն զգալի ուժեղանում է այդ մակարդակի բարձրացմանը զուգընթաց[8][22]։ Ուրիշ գործոններ, որ էական նշանակություն ունեն սուր արթրիտի նոպաների առաջացման հարցում, թվարկված են ստորև. ցածր ջերմաստիճանային ռեժիմ, միզաթթվի մակարդակի արագ փոփոխականություն, ացիդոզ[23][24], հոդային հիդրատացիա և արտաբջջային հյուսվածքների սպիտակուցների՝ պրոտեոգլիկանների, կոլագենների ու խոնդրոիտին սուլֆատի ձևավորում[5] Միզաթթվի արագացված արտադրությունը ցածր ջերմաստիճանային պայմաններում մասամբ բացատրում է, թե ինչու են հիմնականում ոտքի հոդերն ախտահարվում[4]։ Միզաթթվի մակարդակի արագ փոփոխականությունը կարող է առաջանալ մի շարք գործոնների հետևանքով, ներառյալ՝ վնասվածքի առկայությունը, վիրահատությունները, քիմիաթերապիան, դիուրետիկների օգտագործումը և ալոպուրինոլի ընդունման դադարեցումը կամ վերսկսումը[7]։ Հիպերտոնիան բուժող այլ դեղամիջոցների շարքում, հոդատապ առաջացնելու նվազ ռիսկ են պարունակում կալցիում-անտոգոնիստները և լոզարտանը[25]։
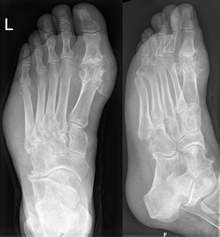
։

Հոդատապը կարող է ախտորոշվել և բուժվել առանց հիպերուրիկեմիայով և դասական պոդագրայով հիվանդի հավելյալ հետազոտության։ Երբ ախտորոշումը կասկածահարույց է, կատարվում է ձուսպային հեղուկի անալիզ[7]։ Քրոնիկ հոդատապի ախտորոշման գործում ռենտգենաբանական հետազոտության դերը նշանակալի է, մինչդեռ սուր նոպաների ժամանակ քիչ օգտակար է[5]։
Ձուսպային հեղուկը
[խմբագրել | խմբագրել կոդը]Հոդատապի վերջնական ախտորոշումը հիմնվում է ձուսպային հեղուկում կամ տոֆուսում նատրիումի ուրատային բյուրեղների հայտնաբերման վրա[17]։ Բորբոքված հոդերից վերցված ձուսպային հեղուկի ախտորոշման ենթակա բոլոր նմուշները պետք է ուսումնասիրվեն նման բյուրեղների առկայությունը հաստատելու համար[5] Բևեռացված լույսով մանրադիտակային հետազոտությունն արտապատկերում է բյուրեղների ասեղաձև մորֆոլոգիական դասակարգումը և խիստ բացասական կրկնակի ճառագայթաբեկմանհատկությունը։ Այս թեստի կատարումն առավել բարդ է և հաճախ պահանջում է որակավորված մասնագետի ներգրավում[26]։ Հեղուկի անալիզը անհրաժեշտ է կատարել բավական արագ aspiration, քամի որ ջերմաստիճանը և pH գործակիցների արժեքները ներազդում են լուծելիության վրա[5]։
Արյան թեստեր
[խմբագրել | խմբագրել կոդը]Հիպերուրիկեմիան հոդատապի դասական հատկանիշներից է, սակայն դեպքերի կեսում այն հանդիպում է առանց հիպերուրիկեմիայի առկայության և միզաթթվի բարձր մակարդակով մարդկանց մեծամասնության մոտ երբևէ հոդատապ չի գրանցվում[17][27]։ Այսպիսով, միայն միզաթթվի մակարդակի չափմամբ ախտորոշում կազմելու հնարավորությունները սահմանափակ են։ref name=PM2010/> Հիպերուրիկեմիան ախտորոշվում է տղամարդկանց մոտ պլազմայում ուրատների մակարդակի 420 միկրոմոլ/լիտր (7.0 Միլիգրամ/դեկալիտր) ցուցանիշի գերազանցմամբ, իսկ կանանց շրջանում՝ 360 միկրոմոլ/լիտր (6.0 Միլիգրամ/դեկալիտր) բաղադրությունը գերազանցող ցուցանիշով[28]։ Այլ հաճախ կատարվող արյան թեստերն են՝ արյան կլինիկական անալիզը, ջրաաղային հավասարակշռության, երիկամային ֆունկցիայի և էրիտրոցիտների նստման արագություն (ԷՆԱ) թեստերը։ Սակայն ինչպես արյան սպիտակ գնդիկների, այնպես էլ ԷՆԱ բարձր մակարդակները պայմանավորված են հոդատապի առկայությամբ, նույնիսկ վարակի բացակայության պայմաններում[29][30]։ Տվյալ դեպքում արյան կլինիկական անալիզի արդյունքներն արձանագրել են 40.0×109/լ (40,000/մմ3) բարձր մակարդակը[7]։
Դիֆերենցիալ դիագնոստիկա
[խմբագրել | խմբագրել կոդը]Հոդատապի դիֆերենցիալ դիագնոստիկա կատարելու հիմնական նպատակը սեպտիկ արթրիտի բացառումն է[5][17] Այս դեպքում պետք է դիտարկել երկու խումբ. հիվանդներ, որոնք ունեն վարակիչ հիվանդություններ և հիվանդներ, որոնց բուժման ընթացքը վիճակի բարելավման չի բերում[17]։ Ախտորոշումը պարզեցնելու համար կիրառվում է ձուսպային հեղուկի Գրամի ներկման մեթոդը և հարուցիչների կուլտուրա մեթոդը[17]։ Որպես այլ հիվանդություններ, որոնց ախտաբանությունը նման է հոդատապին, պետք է նշել պսևդոհոդատապը և ռևմատոիդ արթրիտը[17]։ Հոդատապային տոֆուսները, որ հայտնաբերվում են հոդերից դուրս, կարող են սխալմամբ որպես բազալիոմա[31]։ կամ այլ նեոպլաստիկ նորագոյացություններ ախտորոշվել[32]։
Դասակարգումը և կլինիկան
[խմբագրել | խմբագրել կոդը]
Տարբերում են սուր հոդատապային հոդաբորբ, մեջընդմիջվող հոդատապ, խրոնիկական հոդատապ և հոդատապի արտահոդային ախտահարումները։
Տարբերում են հիվանդության հետևյալ տարատեսակները՝
- թեթև,
- միջին ծանրության,
- ծանր։
Բնորոշ դեպքերում հոդատապը սկսվում է սուր հոդատապային հոդաբորբով։ Այդ նոպան կարող է սկսվել գերսնումից, ալկոհոլի օգտագործումից, ֆիզիկական և հոգեբանական գերբեռնումից, վնասվածքից, մրսելուց և այլ սադրող գործոններից հետո։ Նոպան սովորաբար սկսվում է հանկարծակի, բուռն, որպես օրենք՝ գիշերով։ Հիվանդը նշում է, որ առողջ պառկել է, իսկ արթնանալիս «չի կարող ոտքը գետնին դնել»։ Առավել հաճախ ախտահարվում է առաջին նախագարշապար-մատնոսկրային հոդը։ Հետագայում կարող են ախտահարվել ոտնաթաթի այլ հոդերը։ Սուր բորբոքման բոլոր բաղադրիչները խիստ արտահայտված են՝ մաշկը հիպերէմիկ է (կարմրած), շոշափման ժամանակ կարելի է զգալ տեղային հիպերթերմիայի (տաքության) առկայությունը, ոտնաթաթը այտուցված է, ցավը խիստ արտահայտված։ Ցավը ավելի է ուժեղանում ոտքն իջեցնելիս, վերմակով ծածկելիս կամ շարժելիս։ Կարող է լինել նաև տենդ մինչև 39.0 °C, լեյկոցիտոզ, ԷՆԱ-ի բարձրացում։ Այտուցը երբեմն դուրս է գալիս ախտահարված հոդերից և տարածվում սրունքի վրա։ Նկարագրված պատկերը առանձին դեպքերում ստիպում է տարբերակիչ ախտորոշում անցկացնել սուր թրոմբոֆլեբիտի և կարմիր քամու հետ։ Սակայն, կարմիր քամուն բնորոշ հիպերէմիայի հստակ սահմանի բացակայությունը, Հոմանի բացասական փորձը, հոդաբորբի բնորոշ սկիզբը թույլ է տալիս հակվել հոդատապի ախտորոշմանը։
Սուր հոդատապային նոպան սովորաբար տևում է 3-10 օր և կարող է անցնել նույնիսկ առանց բուժման։ Հոդի գործառությունը լրիվ վերականգնվում է։ Առաջին տարիների ընթացքում դիտվում են իրար խիստ նման 1-2 նոպաներ, միջնոպայական շրջանում բորբոքային փոփոխությունների իսպառ բացակայությամբ։ Աստիճանաբար ավելանում են նոպաների հաճախությունը և տևողությունը, ինչպես նաև ախտահարվող հոդերի քանակը։ Հոդային ախտահարումներին բնորոշ է անզուգաչափ ախտահարումը։
Նոպաների սկզբից 3-4 տարի հետո ձևավորվում են հոդատապային տոֆուսները՝ միզաթթվի աղերի կուտակումները ականջախեցիներում, արմունկների հետին մակերեսով, հազվադեպ՝ մատների վրա։ Տոֆուսները կարող են բացվել՝ արտադրելով միզաթթվի աղերից բաղկացած սպիտակ զանգված։ Տոֆուսները երբեք չեն թարախակալվում։
Հիվանդության ուշ փուլերում զարգանում է խրոնիակակն պոլիարթրիտ՝ հոդերի ապաձևումով։ Հիվանդության ծանր բարդությունն է երիկամների ախտահարումը (հոդատապային երիկամ), հիմնականում ինտերստիցիալ նեֆրիտի, և/կամ գլոմերուլոնեֆրիտի տեսքով։ Արտահոդային ախտահարումներից կարելի է նշել մկանաբորբը, տենդինիտները և տենդովագինիտները։
Հիվանդության թեթև ընթացքի պարագայում, երբ հոդաբորբի նոպաներն առաջանում են տարեկան 1-2 անգամ, բնորոշ է միահոդային ախտահարումը։ Կարող են հայտնաբերվել միայն եզակի տոֆուսներ։ Հոդերում ռենտգենաբանական փոփոխությունները նվազագույն են։ Հիվանդության միջին ծանրության դեպքում հոդաբորբային նոպաների տարեկան հաճախությունը հասնում է 3-4-ի, առավել հաճախ դիտվում է օլիգոարթրիտ, տոֆուսները հաճախ են դիտվում, հստակ նշմարվում են հոդերի ռենտգենաբանական փոփոխությունները։ Ծանր ընթացքի ժամանակ նոպաների հաճախությունը 4-ից ավել է, տոֆուսները բազմաթիվ են, առկա են արտահոդային ախտահարումները։
Հոդատապին բնորոշ ռենտգենաբանական փոփոխությունները սովորաբար դիտվում են հիվանդության սկզբից առնվազն 3 տարի անց և բնորոշվում են ոսկորների էպիֆիզների կլորավուն «դաջված» արատներով («անցահատի» ախտանիշ), սովորաբար առաջին նախագարշապար-մատնոսկրային հոդի ոսկորներում։ Նրանց առաջացումը կապուն են ոսկրային տոֆուսների ձևավորման հետ։ Զուգահեռաբար դիտվում են օստեոարթրոզի ռենտգենաբանական նշանները, փափուկ հյուսվածքների ստվերների լայնացում հոդատապային հանգույցների գոյացման պատճառով։
Հոդատապի ժամանակ դիտվում է հիպերուրիկեմիա (0,06-0,07 գ/լ և ավելին)։ Հիպերուրիկեմիան առավել արտահայտվում է, երբ 3-5 օրվա ընթացքում սննդից հանում են պուրինները։
Երբեմն ախտորոշման համար կատարում են տոֆուսների կենսազննում, ինչպես նաև ախտահարված հոդերի պունկցիա։ Ախտորոշմանը օգնում է ուրատների բյուրեղների հայտնաբերումը տոֆուսներում կամ ձուսպային հեղուկում։
Դիետան և բուժումը
[խմբագրել | խմբագրել կոդը]Բուժման ժամանակ մեծ նշանակություն ունի սննդակարգը։ Այն պետք է լիարժեք լինի, սակայն ցանկալի է չափավոր իջեցնել կալորիականությունը, կտրուկ սահմանափակելով պուրիններով հարուստ սննդամթերքները։ Ճարպերի քանակությունը սննդակարգում սահմանափակում են մինչև 1գ/կգ/օր, սպիտակուցներինը՝ 0.8, աղը՝ 3-4 գրամ շուրջօրյա։ Բացառում են մսի արգանակի, լյարդի, երիկամի, ուղեղի, թրթրնջուկի, գազարի, սպանախի, լոբազգիների օգտագործումը, իսկ միսը կամ ձուկը, այն էլ միայն եփված վիճակում թույլատրում են շաբաթական 1 անգամ 100 գրամ։ Նպատակահարմար է հիմնային հանքային ջրերի առատ օգտագործումը, ընդհանրապես պետք է ավելացնել հեղուկների օգտագործումը մինչև օրական 2-3 լիտրի։ Ալկոհոլը հակացուցված է։
Եթե սննդակարգի միջոցով չի նորմալանում միզաթթվի մակարդակը արյան մեջ պետք է օգտագործել միզաթթվի արտադրությունը ճնշող (ուրիկոդեպրեսանտներ) և/կամ երիկամներից դուրս բերումը խթանող (ուրիկոէլիմինատորներ) պատրաստուկներ։
Ալոպուրինոլ սովորաբար նշանակում են երկարատև (տարիներով)` բուժումը սկսելով ցածր դեղաչափերից, այնուհետև աստիճանաբար բարձրացնելով դեղաչափերը։ Բուժման ֆոնի վրա պարբերաբար պետք է հսկվի ուրիկեմիայի մակարդակը։ Պատրաստուկը սովորաբար լավ է տարվում, սակայն երկարատև ընդունման ժամանակ հնարավոր են ալերգիկ հակազդումներ, որոնք անցնում են դեղաչափի պակասեցումից կամ ժամանակավոր հանումից։ Այն զգուշությամբ են օգտագործում, և ավելի պակաս դեղաչափերով, եթե առկա է երիկամների, լյարդի արտահայտված ախտահարում, ստամոքսի և տասներկումատնյա աղու խոցային հիվանդության ժամանակ։ Եթե այլ պատճառով հիվանդները կիրառում են հակամակարդիչներ, ապա ալոպուրինոլի դեղաչափը պետք է պակասեցնել։
Եթե հոդատապով հիվանդի երիկամները ախտահարված չեն, ապա ուրիկեմիան կարելի է պակասեցնել ուրիկոէլիմինատորների միջոցով։ Ուրիկոճնշիչներով (ուրկոինհիբիտորներ) կամ ուրիկոէլիմինատորներով բուժումը ցանկալի է սկսել սուր հոդաբորբային նոպան անցնելուց հետո։ Ուրիկոճնշիչների երկարատև ընդունումը թույլ է տալիս որոշ չափով ընդլայնել հոդատապով տառապողի սննդակարգը։ Պատրաստուկների ընդունումը ցանկալի է զուգակցել հանքային ջրեր առատ խմելու հետ։
Հոդատապային տոֆուսները հակված են ինքնաբերաբար բացվել և առաջացնել խուղակներ` միզաթթվի բյուրեղների արտադրումով։ Այդպիսի դեպքերում ցանկալի է կիրառել հիպերտոնիկ լուծույթով (NaCl 8-10%) վաննաներ։ Տոֆուսների վրա վիրահատական միջամտությունները ցանկալի չեն, քանի որ այդպիսի վերքերը դժվար են լավանում։ Տոֆուսները սովորաբար չեն թարախակալվում, քանի որ միզաթթուն ունի մանրեասպան հատկություններ։
Բուժման համալիրում կիրառում են նաև բուժական ֆիզկուլտուրան, ֆիզիոթերապևտիկ ազդեցությունները, առողջարանային բուժումը (ռադոնային և սուլֆիսային լոգանքներ)։
Հոդատապի ժամանակ սուր հոդաբորբային նոպաների բուժումն ունի մի շարք առանձնահատկություններ։ Հիվանդը պետք է անշարժ լինի։ Նշանակում են հիմնային հանքային ջրերի առատ ընդունում։ Սահմանափակում են սննդի պուրինները։ Հիվանդին պետք է նախազգուշացնել, որպեսզի սոված չմնա, քանի որ դա առաջացնում է երկրորդային հիպերուրիկեմիա սպիտակուցների քայքայման ուժեղացման հետևանքով։ Հոդատապային նոպան դադարեցնելու լավագույն պատրաստուկներից է կոլխիցինը։ Ճնշելով լեյկոցիտների գաղթը, դժվարեցնելով ֆագոցիտոզը, կայունացնելով նատրիումի մոնոուրատների ֆագոցիտոզը, ինչպես նաև պաշարելով կինինների արտադրությունը կոլխիցինը դադարեցնում է սուր հոդատապային հոդաբորբը։ Պատրաստուկը պետք է ընդունել նոպայի ժամանակ որքան հնարավոր է արագ, ամենասկզբում։ Կոլխիցինի դեղաչափի գերազանցումը կարող է հանգեցնել թունային երևույթների՝ լուծ, փսխում։ Կորտիկոստերոիդներ և ացետիլսալիցիլաթթու չեն նշանակում, քանի որ նրանք բարձրացնում են միզաթթվի մակարդակը արյան մեջ։ Բորբոքված հոդերի վրա դնում են 50 տոկոսանոց դիմեթիլսուլֆօքսիդի լուծույթով թրջոցներ մինչև 40 րոպե տևողությամբ։
Բուժումը
[խմբագրել | խմբագրել կոդը]Բուժման առաջնային նպատակը հոդատապի սուր նոպայի ախտանշանների վերացումն է[33]։ Նոպաների կրկնությունը կարելի է կանխարգելել միզաթթվի ազոտական աղերի մակարդակի նվազեցման համար նախատեսված զանազան դեղամիջոցներով[33] Օրվա ընթացքում մի քանի անգամ 20-ից 30 րոպեով “սառցե թերապիայի” կիրառումը զսպում է ցավը[4][34]։ Արագ բուժման համար նախատեսված դեղամիջոցներ են ոչ ստերոիդային հակաբորբոքային դեղամիջոցներ (NSAIDs), կոլխիցինը և ստերոիդային դեղամիջոցները[4], մինչդեռ կանխարգելիչ դեղամիջոցների շարքին են դասվում ալոպուրինոլը, ֆեբուքսոստատ և պրոբենեցիդը։ Միզաթթվի մակարդակի իջեցումը կարող է բուժել հիվանդությունը[5]։ Կոմորբիդության բուժումը էական նշանակություն ունի[5]։
NSAID ոչ ստերոիդային դեղամիջոցներ
[խմբագրել | խմբագրել կոդը]NSAID ոչ ստերոիդային դեղամիջոցները հոդատապի բուժման առաջատար դեղամիջոցներն են և չկա հստակ ստորաբաժանում, թե որ դեղամիջոցն է ավելի կամ քիչ արդյունավետ[4] Վիճակի բարելավում նկատվում է չորս ժամվա ընթացքում և բուժման կուրսը մեկից երկու շաբաթ է[4][5]։ Այնուամենայնիվ, խորհուրդ չեն տրվում (ստամոքս-աղիքային արյունահոսություններ, երիկամային անբավարարություն կամ սրտի անբավարարություն) հիվանդությունների առկայության դեպքում[35]։ Ինդոմետացինը, լինելով պրակտիկայում ավելի շատ նշանակվող NSAID դեղամիջոց, ի տարբերություն իբուպրոֆենի, գերադասելի է իր առավել քիչ բացասական հետևանքներ ունեցող դեղամիջոցի բնութագրի համար, չունենալով հանդերձ բացարձակ արդյունավետություն[20]։ Այն հիվանդներին, որոնց աղեստամոքսային համակարգում NSAIDների օգտագործումից կարող են բացասական հետևանքներ առաջանալ, լրացուցիչ պրոտոնային պոմպի ինհիբիտորներ կառաջարկվեն[36]։
Կոլխիցին
[խմբագրել | խմբագրել կոդը]Կոլխիցինը այլընտրանք է այն դեպքերում, երբ NSAID-ների օգտագործումը հակացուցված է[4] Բացասական հետևանքները (հիմնականում, ցավերը աղեստամոքսային համակարգում) սահմանափակում են նրա կիրառության հնարավորությունները[37]։ Այնուամենայնիվ, ցավերը աղեստամոքսային համակարգում կախված են դոզավորումից և դրա ռիսկը կարելի է նվազեցնել քիչ, բայց արդյունավետ դեղաչափերի օգտագործմամբ[20]։ Կոլխիցինը կարող է փոխազդել հաճախ նշանակվող այնպիսի դեղամիջոցների հետ, ինչպիսիք ենատորվաստատինը և էրիթրոմիցինը[37]։
Ստերոիդային դեղամիջոցներ
[խմբագրել | խմբագրել կոդը]Գլյուկոկորտիկոիդները համարվում են NSAID-ներից ոչ պակաս արդյունավետ դեղամիջոցներ[38] և կարող են օգտագործվել NSAID-ների սահմանափակումների դեպքում[4]։ Դրական ազդեցություն ունեն նաև ներհոդային ներարկում կատարելիս; այնուամենայնիվ, հոդաբորբը պետք է բացառել, քանի որ ստերոիդային դեղամիջոցները բացասական են ազդում այս հիվանդության վրա[4]։
Pegloticase
[խմբագրել | խմբագրել կոդը]Pegloticase (Krystexxa) թույլատրվել է ԱՄՆ-ում որպես հոդատապի դեղամիջոց 2010 թվականին[39]։ Սա այլընտրանք է մոտ 3% մարդկանց համար, որոնք զգայուն են այլ դեղամիջոցների հանդեպ[39] Pegloticase-ը տրվում է երկու շաբաթը մեկ՝ ներերակային ներարկմամբ[39] և իջեցնում է միզաթթվի մակարդակը նշված հիվանդների շրջանում[40]։
Պրոֆիլակտիկա
[խմբագրել | խմբագրել կոդը]Գոյություն ունեն հոդատապի հետագա զարգացումը կանխարգելող մի շարք դեղամիջոցներ, օրինակ՝ քսանտինօքսիդազի ինհիբիտորը(ներառյալ ալոպուրինոլը, ֆեբուքսոստատը) և ուրիկոզուրիկ դեղամիջոցները (ներառյալ, պրոբենեցիդը և սուլֆինպիրազոնը)։ Բուժումն այս դեղամիջոցներով սովորաբար սկսում են հոդատապի վերջին սուր նոպայից հետո՝ մեկից երկու շաբաթ անց, տեսականորեն նկատի ունենալով նոպայի բարդացման հնարավորությունը[4] և հաճախ նշանակվում են NSAID կամ կոլխիցին դեղամիջոցների հետ՝ առաջին երեքից վեց ամիսների ընթացքում[5] Խորհուրդ չի տրվում հիվանդին տալ մինչև հոդատապի երկու նոպաները[4], եթե առկա են հոդերի ռենտգենաբանական փոփոխություններ, տոֆուսներ կամ ուրատային նեֆրոպաթիա[41],։ քանի որ դեղամիջոցները թանկ են[4] Ուրատաճնշիչ միջոցառումները պետք է ավելացվեն, քանի դեռ շիճուկում միզաթթվի մակարդակը չի իջել մինչև 300–360 Միկրոմոլ/լ (5.0-6.0 Միլիգրամ/դեկալիտր) նիշը և չպետք է դադարեցվեն[4][5]։ Եթե այս դեղամիջոցները օգտագործվում են պարբերական նոպաների ժամանակ, ապա խորհուրդ է տրվում կուրսի ընդհատում[17]։ Եթե միզաթթվի մակարդակը հնարավոր չէ նվազեցնել մինչև 6.0 Միլիգրամ/դեկալիտրը և նոպաները շարունակվում են, ապա բուժումը սխալ է տարվում կամ գործ ունեք քմահաճ հոդատապի հետ[42]։ Ընդհանուր առմամբ, պրոբենեցիդը համարվում է նվազ արդյունավետ դեղամիջոց, քան ալոպուրինոլը[4]։
Որպես կանոն, ուրիկոզուրիկ դեղամիջոցները գերադասելի են, եթե միզաթթու քիչ է արտազատվում. ըստ մեզի 24-ժամյա թեստում արձանագրված արդյունքների՝ միզաթթվի մակարդակը պետք է ցածր լինի 800 Մգ-ից[43]։ Այս դեղամիջոցները երիկամային քարերով հիվանդների համար հակացուցված են[43]։ Եթե մեզի 24-ժամյա թեստում հայտնաբերվում է 800 Մգ-ից ավելի պարունակություն, ինչը խոսում է միզաթթվի հավելուրդային արտադրության մասին, ապա քսանտինօքսիդազի ինհիբիտորի օգտագործումը գերադասելի է[43]։
Քսանտինօքսիդազի ինհիբիտորները (ներառյալ ալոպուրինոլը և ֆեբուքսոստատը) կասեցնում են միզաթթվի արտադրությունը, անվտանգ են երկարատև բուժման պարագայում, զգայունություն չեն առաջացնում, կարող են օգտագործվել երիկամային անբավարարություն կամ ուրատային քարեր ունեցող հիվանդների շրջանում, չնայած նրան, որ ալոպուրինոլը փոքրաթիվ անձանց շրջանում գերզգայունություն առաջացնում է[4] Նման դեպքերում նշանակվում է ֆեբուքսոստատ այլընտրանքային դեղամիջոցը[44]։
Կանխարգելումը
[խմբագրել | խմբագրել կոդը]Հոդատապի առաջնային կանխարգելումը նախ և առաջ ռացիոնալ սնվելն է, ընտանիքում սննդի կուլտուրա դաստիարակելը, մանավանդ այն ընտանիքներում, որոնցում եղել են հոդատապով տառապողներ, ալկոհոլի արգելում, մանավանդ կարմիր գինու և շամպայնի, ճարպակալման կանխարգելումը և այլն։ Երկրորդային կանխարգելումը կանխատեսում է հոդատապի վաղ հայտնաբերումը և բուժումը, հոդատապային նոպաների կանխումը, արտահոդային երևույթների, մանավանդ նեֆրոպաթիայի դեմ պայքարը։
Ծանոթագրություններ
[խմբագրել | խմբագրել կոդը]- ↑ 1,0 1,1 1,2 Chen L. X., Schumacher H. R. Gout: an evidence-based review // Journal of Clinical Rheumatology: practical reports on rheumatic and musculoskeletal disease — Lippincott Williams & Wilkins, 2008. — Vol. 14, Iss. Supplement. — P. S55—S62. — ISSN 1076-1608; 1536-7355 — doi:10.1097/RHU.0B013E3181896921 — PMID:18830092
- ↑ ND J. E. P. J., ND M. T. M., ND H. J. General Considerations // The Clinician's Handbook of Natural Medicine — Edinburgh, NYC: Churchill Livingstone, 2002. — P. 202. — 522 p. — ISBN 978-0-443-07080-8
- ↑ 3,0 3,1 3,2 http://www.niams.nih.gov/Health_Info/Gout/
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 Chen LX, Schumacher HR (2008 թ․ հոկտեմբեր). «Gout: an evidence-based review». J Clin Rheumatol. 14 (5 Suppl): S55–S62. doi:10.1097/RHU.0b013e3181896921. PMID 18830092. S2CID 6644013.
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 5,14 5,15 5,16 5,17 5,18 Richette P, Bardin T (2010 թ․ հունվար). «Gout». Lancet. 375 (9711): 318–328. doi:10.1016/S0140-6736(09)60883-7. PMID 19692116. S2CID 208793280.
- ↑ Vitart V, Rudan I, Hayward C; և այլք: (2008 թ․ ապրիլ). «SLC2A9 is a newly identified urate transporter influencing serum urate concentration, urate excretion and gout». Nat. Genet. 40 (4): 437–42. doi:10.1038/ng.106. PMID 18327257.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 7,0 7,1 7,2 7,3 Eggebeen AT (2007). «Gout: an update». Am Fam Physician. 76 (6): 801–808. PMID 17910294.
- ↑ 8,0 8,1 8,2 8,3 8,4 Terkeltaub R (2010 թ․ հունվար). «Update on gout: new therapeutic strategies and options». Nature Reviews Rheumatology. 6 (1): 30–38. doi:10.1038/nrrheum.2009.236. PMID 20046204. S2CID 19235998.
- ↑ Weaver, AL (2008 թ․ հուլիս). «Epidemiology of gout». Cleveland Clinic journal of medicine. 75 Suppl 5: S9–12. PMID 18819329.
- ↑ Choi HK, Atkinson K, Karlson EW, Willett W, Curhan G (2004 թ․ մարտ). «Purine-rich foods, dairy and protein intake, and the risk of gout in men». N. Engl. J. Med. 350 (11): 1093–103. doi:10.1056/NEJMoa035700. PMID 15014182.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 11,0 11,1 Weaver, AL (2008 թ․ հուլիս). «Epidemiology of gout». Cleveland Clinic Journal of Medicine. 75 (Suppl 5): S9–S12. doi:10.3949/ccjm.75.Suppl_5.S9. PMID 18819329. S2CID 40262260.
- ↑ Hak AE, Choi HK (2008 թ․ մարտ). «Lifestyle and gout». Curr Opin Rheumatol. 20 (2): 179–86. doi:10.1097/BOR.0b013e3282f524a2. PMID 18349748.
- ↑ Williams PT (2008 թ․ մայիս). «Effects of diet, physical activity and performance, and body weight on incident gout in ostensibly healthy, vigorously active men». Am. J. Clin. Nutr. 87 (5): 1480–7. PMID 18469274.
- ↑ 14,0 14,1 Choi HK (2010 թ․ մարտ). «A prescription for lifestyle change in patients with hyperuricemia and gout». Curr Opin Rheumatol. 22 (2): 165–72. doi:10.1097/BOR.0b013e328335ef38. PMID 20035225.
- ↑ Merriman, TR; Dalbeth, N (2011 թ․ հունվար). «The genetic basis of hyperuricaemia and gout». Joint, bone, spine : revue du rhumatisme. 78 (1): 35–40. doi:10.1016/j.jbspin.2010.02.027. PMID 20472486.
- ↑ 16,0 16,1 Reginato AM, Mount DB, Yang I, Choi HK (2012 թ․ սեպտեմբեր). «The genetics of hyperuricaemia and gout». Nat Rev Rheumatol. doi:10.1038/nrrheum.2012.144. PMID 22945592.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 17,0 17,1 17,2 17,3 17,4 17,5 17,6 17,7 Schlesinger N (2010 թ․ մարտ). «Diagnosing and treating gout: a review to aid primary care physicians». Postgrad Med. 122 (2): 157–61. doi:10.3810/pgm.2010.03.2133. PMID 20203467.
- ↑ Stamp L, Searle M, O'Donnell J, Chapman P (2005). «Gout in solid organ transplantation: a challenging clinical problem». Drugs. 65 (18): 2593–611. PMID 16392875.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Loghman-Adham M (1997 թ․ սեպտեմբեր). «Renal effects of environmental and occupational lead exposure». Environ. Health Perspect. Brogan & Partners. 105 (9): 928–38. doi:10.2307/3433873. JSTOR 3433873. PMC 1470371. PMID 9300927.
- ↑ 20,0 20,1 20,2 Laubscher T, Dumont Z, Regier L, Jensen B (2009 թ․ դեկտեմբեր). «Taking the stress out of managing gout». Can Fam Physician. 55 (12): 1209–12. PMC 2793228. PMID 20008601.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Firestein, MD, Shaun; Budd, MD, Ralph C.; Harris Jr., MD, Edward D.; McInnes PhD, FRCP, Iain B.; Ruddy, MD; Sergent, MD, eds. (2008). «Chapter 87: Gout and Hyperuricemia». KELLEY'S Textbook of Rheumatology (8th ed.). Elsevier. ISBN 978-1-4160-4842-8.
{{cite book}}: More than one of|editor1-first=and|editor-first=specified (օգնություն); More than one of|editor3-given=and|editor3-first=specified (օգնություն) - ↑ Virsaladze DK, Tetradze LO, Dzhavashvili LV, Esaliia NG, Tananashvili DE (2007 թ․ մայիս). «[Levels of uric acid in serum in patients with metabolic syndrome]» [Levels of uric acid in serum in patients with metabolic syndrome]. Georgian Med News (Russian) (146): 35–7. PMID 17595458.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ չճանաչված լեզու (link) - ↑ Moyer RA, John DS (2003 թ․ ապրիլ). «Acute gout precipitated by total parenteral nutrition». The Journal of rheumatology. 30 (4): 849–50. PMID 12672211.
- ↑ Halabe A, Sperling O (1994). «Uric acid nephrolithiasis». Mineral and electrolyte metabolism. 20 (6): 424–31. PMID 7783706.
- ↑ Choi HK, Soriano LC, Zhang Y, Rodríguez LA (2012). «Antihypertensive drugs and risk of incident gout among patients with hypertension: population based case-control study». BMJ. 344: d8190. doi:10.1136/bmj.d8190. PMC 3257215. PMID 22240117.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Schlesinger N (2007 թ․ դեկտեմբեր). «Diagnosis of gout». Minerva Med. 98 (6): 759–67. PMID 18299687.
- ↑ Sturrock R (2000). «Gout. Easy to misdiagnose». BMJ. 320 (7228): 132–33. doi:10.1136/bmj.320.7228.132. PMC 1128728. PMID 10634714.
- ↑ Sachs L, Batra KL, Zimmermann B (2009 թ․ նոյեմբեր). «Medical implications of hyperuricemia». Med Health R I. 92 (11): 353–55. PMID 19999892.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «Gout: Differential Diagnoses & Workup - eMedicine Rheumatology».
- ↑ «Gout and Pseudogout: Differential Diagnoses & Workup - eMedicine Emergency Medicine».
- ↑ Jordan DR, Belliveau MJ, Brownstein S, McEachren T, Kyrollos M (2008). «Medial canthal tophus». Ophthal Plast Reconstr Surg. 24 (5): 403–4. doi:10.1097/IOP.0b013e3181837a31. PMID 18806664.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Sano K, Kohakura Y, Kimura K, Ozeki S (2009 թ․ մարտ). «Atypical Triggering at the Wrist due to Intratendinous Infiltration of Tophaceous Gout». Hand (N Y). 4 (1): 78–80. doi:10.1007/s11552-008-9120-4. PMC 2654956. PMID 18780009.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 33,0 33,1 Zhang W, Doherty M, Bardin T; և այլք: (2006 թ․ հոկտեմբեր). «EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT)». Ann. Rheum. Dis. 65 (10): 1312–24. doi:10.1136/ard.2006.055269. PMC 1798308. PMID 16707532.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Schlesinger N; և այլք: (2002). «Local ice therapy during bouts of acute gouty arthritis». J. Rheumatol. 29 (2): 331–4. doi:10.1093/rheumatology/29.5.331. PMID 11838852.
{{cite journal}}: Explicit use of et al. in:|author=(օգնություն) - ↑ Winzenberg T, Buchbinder R (2009). «Cochrane Musculoskeletal Group review: acute gout. Steroids or NSAIDs? Let this overview from the Cochrane Group help you decide what's best for your patient». J Fam Pract. 58 (7): E1–E4. PMID 19607767.
- ↑ Clinical Knowledge Summaries. «Gout - Management -- What treatment is recommended in acute gout?». National Library for Health. Արխիվացված է օրիգինալից 2008 թ․ դեկտեմբերի 16-ին. Վերցված է 2008 թ․ հոկտեմբերի 26–ին-ին.
- ↑ 37,0 37,1 «Information for Healthcare Professionals: New Safety Information for Colchicine (marketed as Colcrys)». U.S. Food and Drug Administration.
- ↑ Man CY, Cheung IT, Cameron PA, Rainer TH (2007). «Comparison of oral prednisolone/paracetamol and oral indomethacin/paracetamol combination therapy in the treatment of acute goutlike arthritis: a double-blind, randomized, controlled trial». Annals of Emergency Medicine. 49 (5): 670–7. doi:10.1016/j.annemergmed.2006.11.014. PMID 17276548.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ 39,0 39,1 39,2 «FDA approves new drug for gout». FDA.
- ↑ Sundy, JS; Baraf, HS, Yood, RA, Edwards, NL, Gutierrez-Urena, SR, Treadwell, EL, Vázquez-Mellado, J, White, WB, Lipsky, PE, Horowitz, Z, Huang, W, Maroli, AN, Waltrip RW, 2nd, Hamburger, SA, Becker, MA (2011 թ․ օգոստոս). «Efficacy and tolerability of pegloticase for the treatment of chronic gout in patients refractory to conventional treatment: two randomized controlled trials». JAMA: the Journal of the American Medical Association. 306 (7): 711–20. doi:10.1001/jama.2011.1169. PMID 21846852.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) CS1 սպաս․ թվային անուններ: authors list (link) - ↑ Tausche AK, Jansen TL, Schröder HE, Bornstein SR, Aringer M, Müller-Ladner U (2009 թ․ օգոստոս). «Gout--current diagnosis and treatment». Dtsch Arztebl Int. 106 (34–35): 549–55. doi:10.3238/arztebl.2009.0549. PMC 2754667. PMID 19795010.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Ali, S; Lally, EV (2009 թ․ նոյեմբեր). «Treatment failure gout». Medicine and health, Rhode Island. 92 (11): 369–71. PMID 19999896.
- ↑ 43,0 43,1 43,2 Elizabeth D Agabegi; Agabegi, Steven S. (2008). Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. էջ 251. ISBN 0-7817-7153-6.
{{cite book}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ «Febuxostat for the management of hyperuricaemia in people with gout (TA164) Chapter 4. Consideration of the evidence». Guidance.nice.org.uk. Արխիվացված է օրիգինալից 2010 թ․ հոկտեմբերի 6-ին. Վերցված է 2011 թ․ օգոստոսի 20–ին-ին.
Արտաքին հղումներ
[խմբագրել | խմբագրել կոդը]| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Հոդատապ» հոդվածին։ |
| ||||||||||||||||
