Ալկաններ
| Այս հոդվածը կարող է վիքիֆիկացման կարիք ունենալ Վիքիպեդիայի որակի չափանիշներին համապատասխանելու համար։ Դուք կարող եք օգնել հոդվածի բարելավմանը՝ ավելացնելով համապատասխան ներքին հղումներ և շտկելով բաժինների դասավորությունը, ինչպես նաև վիքիչափանիշներին համապատասխան այլ գործողություններ կատարելով։ |
Սահմանային կամ հագեցած են կոչվում այն ածխաջրածինները, որոնցում ածխածնի ատոմները իրար միացած են C-C կապով, իսկ մնացած վալենտային կապերը հագեցած են ջրածնի ատոմներով։ Ալկանների ընդհանուր բանաձև է Cn H2n+n։ Ինչպես բոլոր ածխաջրածինները, այնպես էլ սրանք ունեն հոմոլոգիական շարք, որում յուրաքանչյուր անդամ իր նախորդինից տարբերվում է CH2 խմբով, որը կոչվում է հոմոլոգիական տարբերություն։ Միջազգային անունը՝ ալկաններ, պատմական անունը պարաֆիններ, լատիներենից՝ պակաս ակտիվ։ 25 °C ջերմաստիճանում և մթնոլորտային ճնշման տակ հոմոլոգիական շարքի առաջին չորս անդամը գազային նյութեր են, չճյուղավորված ալկանները՝ պենտանից մինչև հեպտադեկան, գտնվում են հեղուկ վիճակում, իսկ բարձր դասի ալկանները պինդ նյութեր են։
Այս դասի առաջին ներկայացուցիչը մեթանն է (CH4)։ Ամենաերկար ածխածնային շղթայով ածխաջրածինը՝ նոնակոնտատրիկտանը (C390H782), որը սինթեզվել է 1985 թվականին անգլիացի քիմիկոսներ Ի․ Բիլլի և Մ․ Կ․ Ուայտինգի կողմից։
Կառուցվածք[խմբագրել | խմբագրել կոդը]
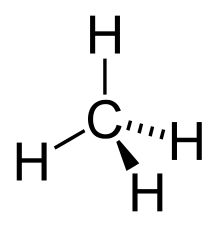
Ալկանների մոլեկուլում C-երը գտնվում են sp3-հիբ. վիճակում։ CH4-ի մոլեկուլում ջրածնի 4 ատոմները C-ի ատոմից գտնվում են միևնույն հեռավորության վրա և տարածության մեջ հեռացված են առավելագույնս դեպի քառանիստի գագաթները կապերի վալենտային անկյունը՝ 109°28' է։ C-C կապերը իրենցից σ-կապեր են ներկայացնում, որոնք ունեն ցածր բևեռայնություն և բևեռանալու ունակություն։ Մնացած ալկաներում կապերի միջև անկյունը նույնն է, իսկ ածխածնային շղթան ընդունում է զիգզագաձև կառուցվածք։ Բոլոր C-H կապերը հավասար են 0,1087 նմ (1 նմ= 10 մ−9), C-C միակ, պարզ կապի երկարությունը 0,154 նմ է։
Անվանակարգում[խմբագրել | խմբագրել կոդը]
Անվանակարգման համար ընտրում ենք ածխածնային ամենաերկար շղթան, համարակալում ենք այն ծայրից, որին մոտ է տեղակալիչը, իսկ եթե տեղակալիչները գտնվում են նույն հեռավորության վրա, ապա համարակալում ենք փոքր ռադիկալի կողմից, թվերի օգնությամբ տալիս ենք տեղակալիչի դիրքը, ապա ռադիկալի անվանումը և վերջում տալիս ենք ածխածնային շղթայի անվանումը։ Սակայն եթե կան մի քանի ռադիկալներ, ապա մինչև ռադիկալի անվանումը գրելը պետք է էնշել միևնույն ռադիկալների թիվը դի-, տրի-, տետրա- և այլ (լատիներեն թվերի օգնությամբ) Օրինակ՝ 2,3,6-տրիմեթիլ, 4-էթիլ, 5-բութիլ օկտան սրա բանաձևը կլինի C17H36։
Հիբրիդացում[խմբագրել | խմբագրել կոդը]
Ածխածնի ատոմները օրգանական միացություններում քառավալենտ են, այսինքն՝ գտնվում են գրգռված վիճակում։ Այս վիճակում տեղի է ունենում հիբրիդացում, որի ընթացքում առաջանում են չորս համարժեք sp3 օրբիտալներ։ Մեթանի մոլեկուլում ջրածնի ատոմները ածխածնի ատոմից գտնվում են հավասար հեռավորության վրա։ Այս կառուցվածքի շնորհիվ այն ստանում է քառանիստ բրգի տեսք, որում անկյունը հավասար է 1090 28'։ Բոլոր ածխաջրածիններում ջրածինը և ածխածինը իրար միացած են սիգմա կապով, որը շատ ամուր կապ է, և քանի որ ալկաններում միայն սիգմա կապեր են, ապա այն շատ պասիվ և քիչ ռեակցունակ է։
Ստացում[խմբագրել | խմբագրել կոդը]
- Մեթանը և իր հոմոլոգները, լինելով պասիվ և քիչ ռեակցունակ, հանդիպում են բնության մեջ ազատ վիճակում։ Հատկապես մեթանը բնական գազի հիմնական բաղադրիչն է, այն կա նաև նավթին ուղեկցող գազերի մեջ։
- Ստացման եղանակներից է ածխածնի և ջրածնի փոխազդեցությունը նիկելե կատալիզատորի առկայությամբ։
C + 2H2 = CH4
- Մեթանը և նրա հոմոլոգները կարելի է ստանալ համապատասխան կատալիզատորի առկայությամբ և համապատասխան հարաբերակցությամբ CO և H2 փոխազդեցությունից՝
CO + 3H2 = CH4 + H2O կամ 4CO + 9H2 = C4H10 + 4H2O
- Մեթանի և նրա ցանկացած հոմոլոգի ստացման կարևորագույն եղանակներից է Դյումայի ռեակցիան
CH3COONa + NaOH = CH4 + Na2CO3 կամ CH3-CH2-CH2-COONa + NaOH = C3H8 + Na2CO3
- Սկսած էթանից ցանկացած ալկան կարելի է ստանալ Վյուրցի եղանակով։ Ռեակցիայի սկզբունքը այն է որ հալոգենածանցյալներից պոկելով հալոգենները ազատ կապերի միջոցով առաջացնել նոր կապ ածխածնային ռադիկալների միջև՝
2CH3-Br + 2 Na = C2H6 + 2 NaBrC5H11-Br + 2 Na + Br-CH3 = C6H14 + 2 NaBr
Հատկություններ[խմբագրել | խմբագրել կոդը]
Ալկանները չեն տալիս միացման ռեակցիաներ, որովհետև նրանցում բոլոր վալենտային կապերը զբաղված են։
1) տալիս են այրման ռեակցիա՝ առաջացնելով ջուր և CO2
- CH4 + 2O2 = CO2 + 2H2O
այս ռեակցիայի ընթացքում անջատվում է 880ԿՋ էներգիա, որի համար էլ այն լայն կիրառություն ունի կենցաղում։ Բոլոր ալկանների այրման ռեակցիաները կարելի է գրել հետևյալ ընդհանուր բանաձևով՝
- CnH2n+2 + (1.5n+0.5) O2 = n CO2 + (n+1) H2O
2) Սահմանային ածխաջրածինները առանց օդի մուտքի 12000 տաքացնելիս քայքայվում են՝ առաջացնելով ածխածին (մուր) և ջրածին
- CH4 = C + 2H2
3) իսկ 15000 պիրոլիզի՝
- 2 CH4 = C2H2 + 3 H2
4) Սահմանային երկու և ավելի ածխածին պարունակող ածխաջրածինները ենթարկվում են դեհիդրման
- C3H8 = C3H6 + H2
կամ ավելի խորը
- C3H8 = C3H4 + 2 H2
5) Ալկանները կարող են փոխազդել հալոգենների հետ, մասնավորապես քլորի հետ լույսի պայմաններում։ Այստեղ քլորի մոլեկուլը ճեղքվում է քլորի երկու ատոմների, որոնք շատ ակտիվ են, և ընթանում է շղթայական ռեակցիա, որի հետևանքով ջրածնի ատոմները տեղակլվում են քլորի ատոմներով, և անջատվում է քլորաջրածին։
- CH4 + Cl2 = CH3Cl
6) ալկանները, որոնք պարունակում 3 և ավելի ածխածնի ատոմներ, բարձր ջերմաստիճանում և կատալիզատորի ներկայությամբ կարող են ենթարկվել կրեկինգի։
Օրինակ՝ CH3-CH2-CH3 = CH4 + CH2=CH2
կամ
- CH3-CH2-CH2-CH3 = CH3-CH3 + CH2=CH2
Սա կոչվում է հոմոլիտիկ կրեկինգ, այսինքն՝ ածխաջրածինը կիսվում է մեջտեղից հավասար, բայց կա նաև հետերոլիտիկ ճեղքում, երբ ածխաջրածինը կիսվում է անհավասարաչափ։
Օրինակ՝ CH3-CH2-CH2-CH3 = CH4 + CH3-CH=CH2
7) Ալկանները որոշակի պայմաններում կարող են փոխազդել ազոտական թթվի հետ
- CH4 + HNO3 = CH3NO2 + H2O
8) արդյունաբերության մեջ մրջնալդեհիդը ստանում են մեթանի օքսիդացումից 4000-6000 C
- CH4 + O2 = HCHO + H2O
9) Երկու և ավելի ածխածին պարունակող ալկանները խորը օքսիդացնելիս կատալիզատորի առկայությամբ ստացվում է կարբոնաթթու։ Առանձնահատկությունը այն է, որ ալկանը կիսվում է մեջտեղից և առաջացնում համապատասխան թթուն։ Օրինակ՝
- 2 C4H10 + 5 O2 = 4 CH3COOH + 2 H2O
Աղբյուրներ[խմբագրել | խմբագրել կոդը]
Գ. Պ. Խոմչենկո (2005). «գլուխ». In Մաշա Մնացականյան (ed.). Քիմիայի ձեռնարկ բուհ ընդունվողների համար. Ռոմիկ Հարությունյան, Գայանե Գրիգորյան, Լուսինե Հարությունյան. Երևան «Զանգակ 97»: Սոկրատ Մկրտչյան.{{cite book}}: CS1 սպաս․ location (link)
| ||||||||||||||||||||||||||||||||||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 6, էջ 40)։ |
