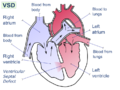
Միջփորոքային միջնապատի արատ
| Միջփորոքային միջնապատի արատ | |
|---|---|
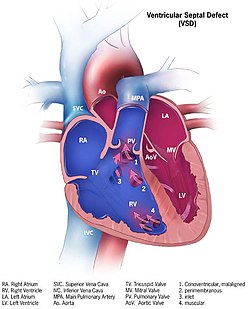 Երևում էմիջփորքային միջնապատի արատի մի քանի ձև՝ 1. կոնվենտրիկուլյար 2. Պերիմեմբրանոզ 3. խորշիկային 4. Մկանային | |
| Տեսակ | հազվագյուտ հիվանդություն և հիվանդության կարգ |
| Պատճառ | բնածին |
| Հիվանդության ախտանշաններ | շնչարգելություն կերակրման ընթացքում, քրտնարտադրություն։ Աուսկուլտատիվ՝ պանսիստոլիկ աղմուկ |
| Բժշկական մասնագիտություն | բժշկական գենետիկա |
| Բուժում | դեղորայքային և վիրաբուժական |
| Հաճախություն | 30-60% |
Սրտի աջ և ձախ փորոքները միմյանից բաժանվում են միջփորոքային միջնապատով, որի ամբողջականության բնածին խախտումը կոչվում է միջփորոքային միջնապատի արատ (ՄՓՄԱ)։ Ընդ որում միջփորոքային միջնապատի դեֆեկտը կարող է հասնել գնդասեղի չափից մինչև հսկա չափերի, ընդհուպ մինչև միջնապատի լրիվ բացակայություն։ Միջփորոքային միջնապատը կազմված է սոտրին մկանային և վերին թաղանթային հատվածներից, որոնք նյարդավորվում են կարդիոմիոցիտներից եկող ազդակններով։
Միջփորոքային միջնապատի թաղանթային հատվածն ավելի մոտ է գտնվում ատրիովենտրիկուլյար հանգույցին, թաղանթային հատվածի դեֆեկտն ավելի հաճախ հանդիպում է մեծահասակների և մեծ տարիքի երեխաների մոտ[1]։ Այս արատը պահանջում է վիրաբուժական միջամտություն, ընդ որում սրտի վրա կատարվող վիրահատությունների մոտ մոտավորապես 80 % դեպքերը պատկանում են հենց միջփորոքային միջնապատի արատին[2]։
Միջփորոքային միջնապատի թաղանթային հատվածի արատն ավելի հաճախ է հանդիպում, քան մկանային հատվածինը և կազմում է սրտի բնածին արատների հիմնական մասը[3]։
Նշաններ և ախտանիշներ[խմբագրել | խմբագրել կոդը]
Միջփորոքային միջնապատի արատը արտահայտվում է երեխայի ծննդից մի քանի շաբաթ անց։ Միջփորոքային միջնապատի արատը դասվում է ացիանոտիկ (ոչ կապույտ) արատների շարքին, առկա է ձախից աջ շունտ, հետևաբար վաղ փուլերում ցիանոզի (կապտության) նշաններ չկան։ Այնուամենայնիվ վիրաբուժական միջամտությամբ չշտկված արատը կարող է բերել թոքային դիմադրության բարձրացմանը, որն էլ իր հերթին կարող է բերել շունտի ուղղության փոխմանը, կունենանք աջից ձախ շունտ, որն էլ կբերի ցիանոզի առաջացման։
- Պանսիստոլիկ (հոլոսիստոլիկ) աղմուկ է լսվում կրծքավանդակի ձախ ստորին հատվածում կրծոսկրին մոտ (կախված է արատի չափից) +/- շոշափվող դող, որը պայմանավորված է արյան տուրբուլենտ հոսքով։ Սրտի տոները նորմալ են։ Մեծ արատը կարող է բերել գագաթային հրոցի տեղաշարժման (տեղաշարժվում է դեպի կողք, պայմանավորված սրտի չափերի մեծացմամբ)։ Նորածինները, ում մոտ առակա է մեծ չափի արատ նկատվում է արտահայտված քրտնարտադրություն և հաճախաշնչություն կրծքով կերակրման ընթացքում[4]։
Միջփորոքային միջնապատի ռեստրիկտիվ փոքր արատներին բնորոշ են աուսկուլտատիվ ավելի բարձր, կոպիտ պանսիստոլիկ աղմուկը կրծոսկրի ձախ եզրով և ավելի ուժեղ շոշափվող դողոցով։ Ավելի մեծ չափի արատներին բնորոշ է ավելի ցածր, փչող բնույթի սիստոլիկ աղմուկը, ինչպես նաև թոքային հիպերտենզիան և ուժեղացած արյունահոսքը։ Ժամանակի ընթացքում ձախից աջ շունտը թոքային հիպերտենզիայի պատճառով կարող է փոխել իր ուղղությունը, դառնալ աջից ձախ շունտ, որն էլ կոչվում է Էյզենմենգերի սինդրոմ։
Պատճառագիտություն[խմբագրել | խմբագրել կոդը]
Միջփորոքային միջնապատի բնածին դեֆեկտը սովորաբար զուգակցվում է այլ բնածին արատների հետ, որոնց է պատկանում Դաունի սինդրոմը[5]։
ՄՓՄԱ-ն կարող է առաջանալ նաև սրտամկանի ինֆարկտից մի քանի օր անց, միջնապատի սուր մեխանիկական վնասման հետևանքով, նախքան սպիական հյուսվածքի ձևավորումը։
Միջփորոքային միջնապատի բնածին արատը պայմանավորված է սաղմնագոյացման 24-28-րդ օրերին սրտի ոչ լիարժեք ձևավավորմամբ։ Արատի պատճառը հիմնականում հանդիսանում է NKX2.5 գենի բացակայությունը։
Պաթոֆիզիոլոգիա[խմբագրել | խմբագրել կոդը]
Փորոքի կծկման կամ սիստոլայի ժամանակ արյան մի փոքր մաս ձախ փորոքից անցնում է դեպի աջ փորոք, որտեղից էլ թոքային զարկերակով անցնում է թոքեր, որն էլ թոքային երակներով կրկին լցվում է ձախ նախասիրտ, որտեղից էլ ձախ փորոք։ Սա ունի երկու հիմնական ազդեցություն։ Առաջինը շրջանառող արյան հետհոսքն է, որը բերում է ձախ փորոքում արյան ծավալի մեծացման։ Երկրորդը՝ քանի որ նորմայում ձախ փորոքում սիստոլիկ ճնշումն ավելի բարձր է (120 մմ․սս․) քան աջ փորոքում (20 մմ․սս․), ապա ձախ փորոքից աջ փորոք եկող արյունը բերում է աջ փորոքում արյան ճնշման և ծավալի բարձրացման, որն էլ իր հերթին հանգեցնում է թոքային հիպերտենզիայի առաջացմանը։ Որոշ ծանր դեպքերում թոքային հիպերտենզիան կարող է բարձրանալ այնքան, որ հավասարվի համակարգային ճնշմանը։ Սրա հետևանքով ձախից աջ շունտը դառնում Է աջից ձախ շունտ, թթվածնով աղքատ արյունը աջ փորոքից անցնում է ձախ փորոք, որտեղից էլ աորտայով անցնում է դեպի համակարգային շրջանառություն և բերում է ցիանոզի առաջացման[6]։
Սա ավելի հաճախ դիտվում է մեծ չափի արատ ունեցող անձանց մոտ, որն արտահայտվում է շնչարգելությամբ, սնուցման խանգարմամբ և նորածինների քաշի և հասկաի աճով սանդղակին համապատասխան։ Փոքր արատով հիվանդները կարող են լինել ասիմպտոմատիկ։ Գոյություն ունեն չորս տեսակի միջնապատային արատներ՝ թաղանթային, ելքային, ատրիովենտրիկուլյար, մկանային[7]։ Ընդ որում ամենից հաճախ հանիդպում են թաղանթային հատվածի արատները և ավելի քիչ մկանային հատվածի արատները։
Ախտորոշում[խմբագրել | խմբագրել կոդը]
ՄՓՄԱ-ն կարող է հայտնաբերվել աուսկուլտատիվ։ ՄՓՄԱ-ի համար պաթոգնոմիկ են հոլոսիստոլիկ աղմուկ։ Աուսկուլտատիվ կարելի է հայտնաբերել նշանակալի չափի արատները։ Աղմուկը պայմանավորված է արյան հոսքով ձախ փորոքից դեպի աջ փորոք, որը նորմայում չպետք է լինի։ Եթե երկու փորոքների միջև չկա արյան ճնշման զգալի տարբերություն, ապա աուսկուլտատիվ որևէ աղմուկ կարող ենք չլսել։ Սա լինում է հետևյալ դեպքերում՝
1)պտղի մոտ (երբ աջ և ձախ փորոքներում ճնշումը հաբասար է),
2)ծնվելուց հետո շատ կարճ ժամանակ (նախքան աջ փորոքի ճնշման նվազումը)
3)որպես ՄՓՄԱ-ի չբուժման դեպքում ուշ փուլերում։ Աուսկուլտատիվ կասկածները կարելի է հերքել կամ հաստատել ոչ ինվազիվ միջամտությամբ, որին է պատկանում էխոսրտագրությունը։ Փորոքներում ճնշման հստակ չափման համար կարող է սրտային կաթետերիզացիայի անհրաժեշտություն լինել։
Դասակարգում[խմբագրել | խմբագրել կոդը]
ՄՓՄԱ-ի դասակարգման բազմաթիվ դասակարգումներ կան, սակայն ընդունված է առաջնորդվել Congenital Heart Surgery Nomenclature և Database Project-ի դասկարգումներով[8]։ Դասակարգումը պայմանավորված է արատի տեղակայմամբ։
Դասակարգում ըստ արատի տեղակայման[խմբագրել | խմբագրել կոդը]
Տիպ 1[խմբագրել | խմբագրել կոդը]
Առաջին տիպին պատկանում են սուբաորտալ տեղակայման արատները
Տիպ 2[խմբագրել | խմբագրել կոդը]
- Երկրորդ տիպը կոչվում է նաև պերիմեմբրանոզ (հարթաղանթային), պարամեմբրանոզ (շուրջթաղանթային), կոնովենտրիկուլյար (դեֆեկտը գտնվում է թոքային և աորտալ փականների անմիջապես ներքևում)։ Երկրորդ տիպին են պատկանում թաղանթային և սուբաորտալ տեղակայման արատները։
- Արատներից ամենահաճախ հանդիպող ձևն է, մոտ 70%
Տիպ 3[խմբագրել | խմբագրել կոդը]
Երրորդ տիպը հայտնի է նաև որպես խորշիկային կամ AV խողովակային։
- Հիմնականում զուգակցված է ատրիովենտրիկուլյար (նախասիրտ-փորոքային) միջնապատի դեֆեկտի հետ, հայտնաբերվում է մոտ 5 % դեպքերում
Տիպ 4[խմբագրել | խմբագրել կոդը]
Չորրորդ տիպը կոչվում է նաև մկանային
- Տեղակայված է միջնապատի մկանային հատվածում, հայտնաբերվում է մոտ 20% դեպքերում։ Ունի ենթադասեր, որը կրկին պայմանավորված է տեղակայմամբ՝ առաջային, գագաթային, հետին և միջին
Տիպ. Գերբոդ[խմբագրել | խմբագրել կոդը]
Տիպ Գերբոդը հայտնի է նաև, որպես ձախ փորոքի և աջ նախասրտի միջև հաղորդակցություն։
- Պատճառը նախասիրտ-փորոքային միջնապատի բացակայությունն է։
-
Սրտի անատոմիական պատկերի կտրվածք, որի վրա երևում են միջփորոքային միջնապատի արատներ։
-
Միջփորոքային միջնապատի արատ։
-
A պատկերը ցույց է տալիս արյան նորմալ շրջանառությունն առողջ սրտում։ B պատկերը ցույց է տալիս միջփորոքային միջնապատի արատի ամենահաճախ հանդիպող տեղակայումը։ Արատի պատճառով թթվածնով հարուստ արյունը ձախ փորոքից անցնում է աջ փորոք և խառնվում թթվածնով աղքատ արյանը։
Բուժում[խմբագրել | խմբագրել կոդը]

Մեծ մաս դեպքերում բուժում չի պահանջվում, քանի որ դեֆեկտն ինքնուրույն փակվում է կյանքի առաջին տարում։ ՄՓՄԱ-ի բուժումը կոնսերվատիվ է կամ վիրահատական։ Փոքր չափի արատները կարող են ինքնուրույն փակվել, սրտի չափերի մեծացմանը զուգահեռ, որոշ դեպքերում կատարվում է կոնսերվատիվ բուժում։
Որոշ դեպքերում, հատակպես հետևյալ զուգակցումների դեպքում անհրաժեշտ է կատարել վիրաբուժական միջամտություն՝
1. Քրոնիկական սրտային անբավարարություն, որոնք դեղորայքային ազդեցությանը չեն ենթարկվում
2. ՄՓՄԱ և թոքային զարկերակի ստենոզ
3. Մեծ ՄՓՄԱ և թոքային հիպերտենզիա
4. ՄՓՄԱ և աորտալ ռեգուրգիտացիա (հետհոսք) Վիրահատական միջամտության համար կատարվում է միջնակ ստերնոտոմիա։ Քիչ դեպքերում կատարվում է նաև միջմաշկային էնդովասկուլյար միջամտություն, որը քիչ ինվազիվ միջամտություն է և սրա համար սրտի աշխատանքը կանգնեցնելու կարիք չկա։ ՄՓՄԱ-ի շտկման ժամանակ հիմնականում տեղի է ունենում սրտի հաղորդչական համակարգի վնասում։ ՄՓՄԱ-ը նորածինների մոտ հիմնականում ենթարկվում է դեղորայքային բուժմանը։ Կիրառվում են սրտային գլիկոզիդներ (օրինակ՝ դիգօքսին 10-20μg/kg օրական), կանթային միզամուղներ (ֆուրոսեմիդ 1-3 մգ/կգ օրական) և ԱՓՖ ինհիբիտորներ (կապտոպրիլ 0,5-2 մգ/կգ օրական)։
Կաթետերով միջնապատի փակում[խմբագրել | խմբագրել կոդը]
Ամպլացեր կոչվող սարքի միջոցով կարելի է կատարել որոշ արատների փակում[9]։ Առաջին անգամ սարքը կիրառվել է 2009 թվականին[9]։ Համարվում է անվտանգ և արդյունավետ մեթոդ[9], ինչպես նաև ֆինանսապես ավելի նպատակահարմար է, քան սրտի բաց վիրահատությունը[9]։ Սարքը տեղադրվում է աճուկային հատվածում արված փոքր կտրվածքի միջոցով[10]։
Սարքը ամբողջությամբ փակում է դեֆեկտը տեղադրելուց հետո 24 ժամվա ընթացքում[11]։ Իմպլանտացիայից հետո կա էմբոլիայի շատ ցածր ռիսկ[12]։ Միջամտությունից հետո շատ հազվադեպ կարող է դիտվել եռափեղկ փականի ռեգուրգիտացիա[11]։ Կան դեպքեր, երբ սարքի իմպլանտացիայից հետո սրտում առաջացել են կյանքին վտանգ սպառնացող արյունազեղումներ[13]։ Որն էլ պատճառ է հանդիսանում, որ սարքի իմպլանտացիայից հետո մոտ 1 % դեպքերում առաջանում է անհապաղ սրտի բաց վիրահատություն կատարելու անհրաժեշտություն[13]։ Եթե սարքը ավելի մեծ է, քան դեֆեկտը, ապա կարող է առաջացնել միջնապատային հյուսվացքի էրոզիա (արյունազեղում)[13]։
Վիրահատություն[խմբագրել | խմբագրել կոդը]
ա)Պերիմեմբրանոզ ՄՓՄԱ-ի վիրաբուժական փակումը կատարվում է սիրտ-թոքային շունտավորմամբ։ Հիվանդը սառեցվում է մինչև 28 աստիճան։ Միջմաշկային սարքի տեղադրումը ԱՄՆ-ում հազվադեպ է կիրառվում, քանի որ այն բերում է վաղ կամ ուշ AV հանգույցային բլոկադայի։
բ)Վիրաբուժական միջամտությունը կատարվում է աջ նախասրտով։ Եռափեղկ փականի փեղկերից մեկը հետ է տարվում կամ հատվում է, որպեսզի երևան դեֆեկտի եզրերը։
գ)Արատը փակելու համար կիրառվող նյութերն են տվյալ հիվանդի պերիկարդից վերցրված հատվածը, խոզի պերիկարդը, պոլիտետրաֆլուրոէթիլեն (PTFE) և դակրոն։
դ)Որպես կարանյութ կիրառվում է պոլիպրոպիլենը։
ե)Վիրահատության ժամանակ անհրաժեշտ է լինել շատ ուշադիր և հետևողական, որպեսզի չվնասվի միջփորոքային միջնապատի ձախ կողմում, պապիլյար մկաններին մոտ տեղակայված հաղորդչական համակրագը։
զ)Անհրաժեշտ է խուսափել կարելու ժամանակ աորտալ փականները վնասելուց։
Է)Վերականգնումից անմիջապես հետո կատարվում է սրտից օդի դուրս բերում, ներարկվում է ածխաթթու գազ և կատարվում օդի դուրս բերում սրտից։
ը)Վիրահատության ընթացքում տրանսէզոֆագեալ էխոկարդիոգրաֆիան օգտագործվում է, որպեսզի համոզվեն, որ արատը լիարժեք փակված է, աորտալ և տրիկուսպիդալ փականները լավ են աշխատում, փորոքային ֆունկցիան չի տուժել և օդը սրտի ձախ կեսից լիարժեք դուրս է բերվել։
թ)Կրծոսկրի, հյուսվածքների և մաշկի ամբողջականությունը վերականգնելուց հետո, տեղադրվում է կաթետեր, որի միջոցով ներարկում են տեղային ցավազրկող միջոցներ։
ժ)Բազմակի մկանային արատները փակելու համար կիրառում են ֆլուրոսցեին[14]։
Համաճարակաբանություն[խմբագրել | խմբագրել կոդը]
ՄՓՄԱ-ն ամենահաճախ հանդիպող բնածին արատներից է։ Բոլոր բնածին արատների մոտ 30-60%-ը պատկանում է հենց ՄՓՄԱ-ին, կամ յուրաքանչյուր 1000 երեխայից 2-6 մոտ։ Զարգացման ընթացքում, երբ սիրտն սկսվում է ձևավորվել տեղի է ունեում զարգացման խանգարում, որն էլ բերում է միջնապատի լիարժեք ձևավորման խանգարում։ Որոշ դեպքերում դեֆեկտը փակվում է ինքնուրույն[15][16][17]։
Տես նաև[խմբագրել | խմբագրել կոդը]
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ Taylor, Michael D (2019 թ․ փետրվարի 2). «Muscular Ventricular Septal Defect». eMedicine. Medscape.
- ↑ Waight, David J.; Bacha, Emile A.; Kahana, Madelyn; Cao, Qi-Ling; Heitschmidt, Mary; Hijazi, Ziyad M. (March 2002). «Catheter therapy of Swiss cheese ventricular septal defects using the Amplatzer muscular VSD occluder». Catheterization and Cardiovascular Interventions. 55 (3): 355–361. doi:10.1002/ccd.10124. PMID 11870941.
- ↑ Hoffman, JI; Kaplan, S (2002). «The incidence of congenital heart disease». Journal of the American College of Cardiology. 39 (12): 1890–900. doi:10.1016/S0735-1097(02)01886-7. PMID 12084585.
- ↑ Cameron P. et al: Textbook of Pediatric Emergency Medicine. p116-117 [Elsevier, 2006]
- ↑ Wells, GL; Barker, SE; Finley, SC; Colvin, EV; Finley, WH (1994). «Congenital heart disease in infants with Down's syndrome». Southern Medical Journal. 87 (7): 724–7. doi:10.1097/00007611-199407000-00010. PMID 8023205.
- ↑ Kumar & Clark 2009
- ↑ Mancini, Mary C (2018 թ․ հունիսի 20). «Ventricular Septal Defect Surgery in the Pediatric Patient». eMedicine. Medscape.
- ↑ Jacobs, Jeffrey; Mavroudis, Constantine (March 2000). «Congenital Heart Surgery Nomenclature and Database Project: ventricular septal defect». Ann Thorac Surg. 69 (3): 25–35. doi:10.1016/S0003-4975(99)01270-9. PMID 10798413.
- ↑ 9,0 9,1 9,2 9,3 Fu, YC (February 2011). «Transcatheter device closure of muscular ventricular septal defect». Pediatrics and Neonatology. 52 (1): 3–4. doi:10.1016/j.pedneo.2010.12.012. PMID 21385649.
- ↑ Amplatzer septal occluder. (2013) U.S. Food and Drug Administration. Retrieved February 26, 2014, from https://www.fda.gov/MedicalDevices/ProductsandMedicalProcedures/DeviceApprovalsandClearances/Recently-ApprovedDevices/ucm083978.htm Արխիվացված 2017-01-18 Wayback Machine
- ↑ 11,0 11,1 Szkutnik; և այլք: (2007). «Use of the Amplatzer muscular ventricular septal defect occluder for closure of perimembranous ventricular septal defects». Heart. 93 (3): 355–358. doi:10.1136/hrt.2006.096321. PMC 1861424. PMID 16980519.
- ↑ Fernando Rajeev; և այլք: (2013). «Patent ductus arteriosus closure using an Amplatzer ventricular septal defect closure device». Experimental & Clinical Cardiology. 18 (1): e50–e54.
- ↑ 13,0 13,1 13,2 Rare Serious Erosion Events Associated with St. Jude Amplatzer Atrial Septal Occluder (ASO). (2013, October 17). U.S. Food and Drug Administration. Retrieved February 26, 2014, from https://www.fda.gov/MedicalDevices/Safety/AlertsandNotices/ucm371145.htm?source=govdelivery(չաշխատող հղում)
- ↑ Mathew, Thomas (2014). «Use of Fluorescein Dye to Identify Residual Defects». Ann Thorac Surg. 97 (1): e27-8. doi:10.1016/j.athoracsur.2013.10.059. ISSN 0003-4975. PMID 24384220.
- ↑ Meberg, A; Otterstad, JE; Frøland, G; Søarland, S; Nitter-Hauge, S (1994). «Increasing incidence of ventricular septal defects caused by improved detection rate». Acta Paediatrica. 83 (6): 653–657. doi:10.1111/j.1651-2227.1994.tb13102.x.
- ↑ Hiraishi, S; Agata, Y; Nowatari, M; Oguchi, K; Misawa, H; Hirota, H; Fujino, N; Horiguchi, Y; Yashiro, K; Nakae, S (March 1992). «Incidence and natural course of trabecular ventricular septal defect: two-dimensional echocardiography and color Doppler flow imaging study». The Journal of Pediatrics. 120 (3): 409–15. doi:10.1016/s0022-3476(05)80906-0. PMID 1538287.
- ↑ Roguin, Nathan; Du, Zhong-Dong; Barak, Mila; Nasser, Nadim; Hershkowitz, Sylvia; Milgram, Elliot (1995 թ․ նոյեմբերի 15). «High prevalence of muscular ventricular septal defect in neonates». Journal of the American College of Cardiology. 26 (6): 1545–1548. doi:10.1016/0735-1097(95)00358-4. PMID 7594083.