Կալիումի հիդրօքսիդ
| Կալիումի հիդրօքսիդ | |
|---|---|
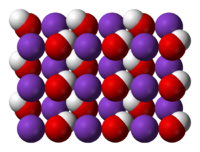 | |
 | |
| Քիմիական բանաձև | KOH |
| Մոլային զանգված | 9,3E−26 կիլոգրամ[1] գ/մոլ |
| Խտություն | 2,04 ± 0,01 գ/սմ³[2] գ/սմ³ |
| Հալման ջերմաստիճան | 716 ± 1 ℉[2], 380 °C[3] և 406 °C[4] °C |
| Եռման ջերմաստիճան | 2415 ± 1 ℉[2], 1324 °C[3] և 1327 °C[4] °C |
| Գոյացան էնթալպիա | −425,8 կՋ/մոլ կՋ/մոլ |
| Հալման էնթալպիա | 7,5 կՋ/մոլ կՋ/մոլ |
| Եռման էնթալպիա | 128,9 կՋ/մոլ կՋ/մոլ |
| Գոլորշու ճնշում | 1 ± 1 mm Hg[2] |
| Քիմիական հատկություններ | |
| Բեկման ցուցիչ | 1,409 և 1,421[5] |
| Դասակարգում | |
| CAS համար | 1310-58-3 |
| PubChem | 14797 |
| EINECS համար | 215-181-3 |
| SMILES | [OH-].[K+] |
| ЕС | 215-181-3 |
| RTECS | TT2100000 |
| ChEBI | 14113 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Կալիումի հիդրօքսիդ, անօրգանական լուծույթ է, քիմիական բանաձևն է KOH։ Այն հայտնի է նաև կծու կալի և կաուստիկ պոտաշ անվանումներով։ 2005 թվին մոտ 700,000 - 800,000 տոննա կալիումի հիդրօքսիդ է արտադրվել։ Տարեկան NaOH (նատրիումի հիդրօքսիդ) արտադրվում է 100 անգամ ավելի շատ, քան KOH[6][7][8]:
Հատկություններ[խմբագրել | խմբագրել կոդը]
Կծու կալինդ պինդ, փխրուն սպիտակ նյութ է։
Հեշտ լուծվում է ջրի մեջ (լուծվում է ավելի լավ, քան կծու նատրոնը)։ Կծու կալին օդից արագ կլանում է ջուր և ածխաթթու գազ։
Կծու նատրոնի նման, կծու կալին փոխազդում է թթուների, թթվային օքսիդների և աղերի հետ՝
- 2 KOH + H2SO4 → K2SO4 + 2H2O
- 2 KOH + CO2 → K2CO3 + H2O
- 2 KOH + CuCl2 → 2 KCl + Cu(OH)2
Օգտագործումը[խմբագրել | խմբագրել կոդը]
Շատ նպատակների համար կալիումի հիդրօքսիդը և նատրիումի հիդրօքսիդը փոխարինում են մեկը մյուսին, սակայն սովորաբար նատրիումի հիդրօքսիդն ավելի գերադասելի է ավելի էժան լինելու պատճառով։
Կալիումի հիդրօքսիդը հիմնականում օգտագործվում է հեղուկ օճառ և տարբեր տիպի կալիումի միացություններ ստանալու համար։
Այն օգտագործվում է բիոդիզելի արտադրության մեջ, քանի որ կալիումի հիդրօքսիդը ռեակցիայի մեջ է մտնում կենդանական յուղերի ճարպերի հետ։
Իր քայքայիչ հատկություների շնորհիվ կալիումի հիդրօքսիդը հաճախ օգտագործվում է դժվար մաքրվող մակերեսների մաքրման և ախտահանման համար։ Կենդանիներից հանված մաշկը մազերից ազատելու համար այն մի քանի ժամով պահում են կալիումի հիդրօքսիդի և ջրի լուծույթի մեջ։
Տեսեք նաև[խմբագրել | խմբագրել կոդը]
Աղբյուրներ[խմբագրել | խմբագրել կոդը]
- Յու․ Վ․ Խոդակով, Լ․ Ա․ Ցվետկով և ուրիշներ։ «Քիմիա», Երևան, 1961։
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ 1,0 1,1 POTASSIUM HYDROXIDE
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 http://www.cdc.gov/niosh/npg/npgd0523.html
- ↑ 3,0 3,1 3,2 3,3 POTASSIUM HYDROXIDE
- ↑ 4,0 4,1 4,2 4,3 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ https://www.chemicalbook.com/ChemicalProductProperty_EN_CB3107908.htm
- ↑ H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim.
- ↑ "Caustic Potash." Oxy.com Արխիվացված 2009-01-25 Wayback Machine Retrieved on January 24 2008.
- ↑ "Potassium Hydroxide." MSDS Retrieved on January 24
| ||||||||||
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Կալիումի հիդրօքսիդ» հոդվածին։ |
| ||||||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 5, էջ 176)։ |
