Պատվաստանյութ գոտևորող որքինի դեմ
 | |
| Պատվաստանյութի նկարագրում | |
| Թիրախ հիվանդություն | Herpes zoster, postherpetic neuralgia, Ramsay Hunt syndrome type II |
| Տիպ | Կաղապար:Ubl |
| Կլինիկական տվյալներ | |
| Վաճառքային անվանումներ | Zostavax, Shingrix |
| Թերապևտիկ ապրանքների կարգավորում |
|
| Հղիության կատեգորիա |
|
| Օգտագործման եղանակներ | Կաղապար:Ubl |
| ԱԹԴ կոդ | |
| Նույնացուցիչներ | |
| ChemSpider |
|
| UNII | |
| KEGG | |
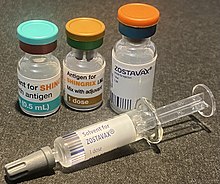
Պատվաստանյութ գոտևորող որքինի դեմ, պատվաստանյութ, որը նվազեցնում է հերպեսի զոստերի ((անգլ.՝ varicella zoster) վիրուսի վերաակտիվացման հետևանքով առաջացած հիվանդություն) դեպքերը, որը նույնպես պատասխանատու է ջրծաղիկի համար[2]։ Գոտևորող որքինը կարող է առաջացնել ցավոտ, բշտիկավոր ցան, որին կարող է հաջորդել քրոնիկ ցավը (հետհերպետիկ նևրալգիա), ինչպես նաև այլ բարդություններ։ Տարեց մարդիկ, ինչպես նաև թույլ իմունային համակարգ ունեցող մարդիկ ավելի հավանական է, որ կհիվանդանան։ և գոտևորող որքինը, և հետհերպետիկ նևրալգիան կարող են կանխվել պատվաստումների միջոցով[3]։
Գոտևորող որքինի դեմ երկու պատվաստանյութ հաստատվել է 50 տարեկանից բարձր մարդկանց օգտագործման համար[3]։ Շինգրիքսը (GSK) ռեկոմբինանտ ենթամիավոր պատվաստանյութ է, որն օգտագործվում է շատ երկրներում 2017 թվականից[4]։ Զոստավաքսը՝ օգտագործվում է 2006 թվականից[4], թուլացած պատվաստանյութ է, որը բաղկացած է ջրծաղիկի պատվաստանյութի սովորական պատվաստանյութի ավելի մեծ չափաբաժնից[2]։ Ի տարբերություն շինգրիկքսի, զոստավաքսը հարմար չէ իմունային ճնշմամբ կամ իմունային համակարգի վրա ազդող հիվանդություններով տառապող մարդկանց համար։ Զոստավաքսը դադարեցվել է ԱՄՆ-ում 2020 թվականի նոյեմբերին[3][5]։
Շինգրիքսը, կարծես, կանխում է գոտևորող որքինի ավելի շատ դեպքեր, քան զոստավաքսը, չնայած կողմնակի ազդեցություններն ավելի տարածված են[6][7]։
Մեկ այլ պատվաստանյութ, որը հայտնի է որպես ջրծաղիկի պատվաստանյութ, օգտագործվում է նույն վիրուսի պատճառած հիվանդությունները կանխելու համար[8]։
Օգտագործումը բժշկության մեջ[խմբագրել | խմբագրել կոդը]
Զոստեր պատվաստումը օգտագործվում է գոտևորող որքինի և դրա բարդությունների կանխարգելման համար, ներառյալ հետհերպետիկ նևրալգիան[2][2][3]։ Այն կարելի է համարել թերապևտիկ պատվաստանյութ, քանի որ այն օգտագործվում է թաքնված վիրուսի բուժման համար, որը վաղ տարիքում ջրծաղիկով վարակվելուց հետո բջիջներում քնած է մնացել։ Զոստերի երկու մատչելի պատվաստանյութերը նախատեսված են 50 տարեկանից բարձր մարդկանց օգտագործման համար[6][9]։ 2021 թվականի դրությամբ անհասկանալի էր, թե արդյոք անհրաժեշտ է ուժեղացուցիչ դոզան, բայց ԱՄՆ-ում իմունիզացիայի պրակտիկայի Խորհրդատվական կոմիտեն (ACIP-անգլ.՝ Advisory Committee on Immunization Practices) խորհուրդ է տալիս շինգրիքսը 50 տարեկանից բարձր մեծահասակների համար, ներառյալ նրանց, ովքեր արդեն ստացել են զոստավաքս[10]։
Շինգրիքս[խմբագրել | խմբագրել կոդը]

ACID-ը (անգլ.՝ atomicity, consistency, isolation, durability) քվեարկել է, որ շինգրիքսը նախընտրելի է զոտավաքսից՝ գոտևորող որքինի կանխարգելման և դրա հետ կապված բարդությունների համար, քանի որ տվյալները ցույց են տվել, որ պատվաստանյութը ավելի քան 90% արդյունավետություն ունի հիվանդության դեմ բոլոր տարիքային խմբերում։ Ի տարբերություն զոտավաքսի, որը տրվում է որպես մեկ ներարկում, շինգրիքսը տրվում է երկու ներմկանային դոզաներով՝ վեց ամիս ընդմիջումներով[4][10]։ Շինգրիքսը պատվաստումից հետո առնվազն 7 տարի ապահովում է անձեռնմխելիության բարձր մակարդակ, բայց հնարավոր է, որ պատվաստանյութը կարող է շատ ավելի երկար պաշտպանություն ապահովել[11]։
Խոշոր, պատահական սկզբունքով ընտրված կլինիկակայում ուսումնասիրությունը ցույց է տվել, որ Շինգրիքսը 50-59 տարեկան տարիքային խմբում 96,6%-ով նվազեցնում է գոտևորող որքինի դեպքերը, իսկ 70 տարեկանից բարձր անձանց մոտ ' 91,3% - ով[4]։
Զոստավաքս[խմբագրել | խմբագրել կոդը]
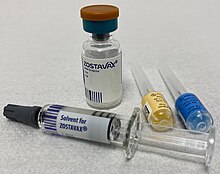
Cochrane-ի վերանայումը եզրակացրեց, որ զոտավաքսը «արդյունավետ է հերպեսի զոստերի հիվանդության կանխարգելման գործում մինչև երեք տարի»[7]։ Հերպեսի զոստերի պատվաստանյութով պատվաստումից չորս տարի անց պաշտպանության տևողությունը անհայտ է։ Կրկնակի պատվաստումների անհրաժեշտությունը դեռ հաստատված չէ[9]։
Պատվաստանյութը, որը ստացած էր 60 և բարձր տարիքի համար՝ 38,000 մեծահասակների մասնակցությամբ ուսումնասիրության արդյունքը ցույց է տրվել, որ զոստավաքսը 51% - ով նվազեցնում է գոտևորող որքինի դեպքերը։ Պատվաստանյութը նաև 67%-ով նվազեցրել է հետհերպետիկ նևրալգիայի դեպքերը և 61% - ով նվազեցրել է գոտևորող որքինի հետ կապված ցավի և անհանգստության խստությունն ու տևողությունը[12][13][14]:Սննդի և դեղերի վարչությունը ի սկզբանե խորհուրդ է տվել պատվաստանյութը 60 տարեկան և ավելի բարձր տարիքի անձանց համար, ովքեր չունեն ուժեղ ալերգիա դրա որևէ բաղադրիչի նկատմամբ և բավարարում են հետևյալ պահանջները[15][16].
- չունեն թուլացած իմունային համակարգ ՄԻԱՎ/ՁԻԱՀ-ի կամ այլ հիվանդության պատճառով, ինչպես նաև չեն օգտագործում դեղամիջոցներ (օրինակ՝ ստերոիդներ, ճառագայթում և քիմիաթերապիա), որոնք ազդում են իմունային համակարգի վրա;
- չունեն ոսկրածուծի կամ ավշային համակարգի վրա ազդող քաղցկեղի պատմություն, ինչպիսիք են լեյկոզը կամ լիմֆոմաները;
- չունեն ակտիվ կամ չբուժված տուբերկուլյոզ։
2006 թվականին ԱՄՆ Իմունիզացիայի Պրակտիկայի Խորհրդատվական Կոմիտեն (անգլ.՝ ACIP-atomicity, consistency, isolation, durability) խորհուրդ տվեց պատրաստի պատվաստանյութ կիրառել 60 և ավելի բարձր տարիքի բոլոր մեծահասակների համար, ներառյալ նրանց, ովքեր նախկինում ունեցել են գոտևորող որքին դրվագ[17] և նրանց, ովքեր չեն հիշում ջրծաղիկ ունենալ, քանի որ 40 և ավելի բարձր տարիքի ամերիկացիների ավելի քան 99% - ը ջրծաղիկ ուներ[18]։
Կողմնակի ազդեցություն[խմբագրել | խմբագրել կոդը]
Շինգրիքս[խմբագրել | խմբագրել կոդը]
Շինգրիքսի պատվաստումից ժամանակավոր կողմնակի ազդեցությունները հավանական են վեց հոգուց մեկի մոտ և կարող են բավականաչափ ծանր լինել՝ ազդեն առօրյա կյանքի բնականոն գործունեության վրա մինչև երեք օր[18]։ Ներարկման տեղում մեղմ և միջին ցավը տարածված է, ոմանք կարող են ունենալ կարմրություն կամ այտուց[18]։ Կողմնակի ազդեցությունները ներառում են հոգնածություն, մկանների ցավ, գլխացավ, ցնցում, ջերմություն և սրտխառնոց:Ախտանիշները սովորաբար անհետանում են երկու-երեք օրվա ընթացքում[18]։ Shingrix-ի կողմնակի ազդեցություններն ավելի ուժեղ են, քան Zostavax-ը և ավելի հաճախ են հանդիպում 50-ից 69 տարեկան մարդկանց մոտ, համեմատած 70 և ավելի բարձր տարիքի մարդկանց հետ[18] Ախտանիշները սովորաբար անհետանում են երկու-երեք օրվա ընթացքում[19][6][18]։
Զոստավաքս[խմբագրել | խմբագրել կոդը]
Զոստավաքսը շատ անվտանգ է՝ մարդկանց մեկից մի քանի տոկոսը զարգացնում է ջրծաղիկի մեղմ ձև, հաճախ ներարկման վայրի շուրջ հինգ կամ վեց բշտիկներով և առանց ջերմության։ Բշտիկներն անվնաս են և ժամանակավոր[20][21]։ Մեկ ուսումնասիրության ընթացքում զոսսավաքս խմբի մասնակիցների 64%-ը և վերահսկիչ խմբի 14%-ը ունեցել են անբարենպաստ ռեակցիաներ։ Այնուամենայնիվ, լուրջ անբարենպաստ իրադարձությունների մակարդակը համեմատելի էր զոստավաքս խմբի (0,6%) և պլացեբո խմբի (0,5%) միջև[22]։ Լեյկոզով տառապող երեխաների շրջանում կատարված ուսումնասիրությունը ցույց է տվել, որ պատվաստումից հետո գոտևորող որքինի ստանալու ռիսկը շատ ավելի ցածր է, քան բնական ջրծաղիկի պատմություն ունեցող երեխաների մոտ գոտևորող որքին ստանալու ռիսկը։ Առողջ երեխաներից և մեծահասակներից ստացված տվյալները ցույց են տալիս նույն ուղղությամբ[20]։
Զոստավաքսը չի օգտագործվում իմունային անբավարարությամբ տարապող մարդկանց մոտ[23][24]։
Բաղադրություն[խմբագրել | խմբագրել կոդը]
Շինգրիքս[խմբագրել | խմբագրել կոդը]
Շինգրիքսը ներմկանային կառավարման կասեցում է, որը բաղկացած է լատին․՝ varicella zoster վիրուսի լիոֆիլացված ռեկոմբինանտ գլիկոպրոտեին e-հակագենից, որը վերականգնվում է AS01B կասեցման հետ օգտագործման ընթացքում՝ որպես իմունաբանական օժանդակ միջոց։ Շինգրիքսը կարող է օգտագործվել նաև որպես իմունաբանական օժանդակ միջոց։ Հակագենը գլիկոպրոտեինի մաքրված, կտրված ձև է, որն հանդիպում է չինական համստերի ձվարանների բջիջներում։ AS01B-ի օժանդակ կախոցը բաղկացած է 3-O-desacyl-4'-monophosphoryl lipide A-ից (MPL) Սալմոնելլաից և Սապոնինների մոլեկուլից (QS-21), որը զտված է լատին․՝ Quillaja saponaria քաղվածքից (օճառի ծառ), որը միավորված է լիպոսոմային բանաձևի մեջ, որը բաղկացած է դիոլեոիլֆոսֆատիդիլխոլինից (անգլ.՝ DOPC - dioleoyl phosphatidylcholine) և խոլեստերինից ֆոսֆատ-բուֆերային աղի մեջ[25]։
Զոստավաքս[խմբագրել | խմբագրել կոդը]
Զոստավաքսը պարունակում է կենդանի թուլացած լատին․՝ varicella-zoster վիրուս[5][20]։ Այն ներարկվում է ենթամաշկային թևի վերին մասում[26]։ Պատվաստանյութը պատրաստվում է MRC-5 (անգլ.՝ Medical Research Council cell strain 5) պտղի բջիջների գծի միջոցով[12]։ Սա կրոնական և էթիկական մտահոգություններ է առաջացնում որոշ հավանական օգտագործողների մոտ, քանի որ այս բջջային գիծը ստացվել է վիժեցված պտուղից[27]։
Տնտեսական արդյունավետություն[խմբագրել | խմբագրել կոդը]
2007 թվականի ուսումնասիրությունը ցույց է տվել, որ պատվաստանյութը, հավանաբար, ԱՄՆ-ում ծախսարդյունավետ է՝ կանխատեսելով տարեկան առողջապահական ծախսերի խնայողություն $ 82-ից $ 103 միլիոն դոլար, ծախսերի արդյունավետության գործակիցներով՝ $ 16,229-ից $ 27,609 մեկ տարվա որակի ճշգրտված կյանքի համար[28]։ 2007 թվականին պատվաստանյութը պաշտոնապես առաջարկվում էր ԱՄՆ-ում 60 և ավելի բարձր տարիքի առողջ մեծահասակների համար, բայց 2020 թվականից այն այլևս չի կիրառվում՝ հաշվի առնելով շինգրիքսի հավանական գերակայությունը[29][30][31]։
Կանադայում շինգրիքսի արժեքը կազմում է մոտ CA$300 երկու դեղաչափի համար:Սա, հավանաբար, ավելի ծախսարդյունավետ միջամտություն է, քան պատվաստանյութը՝ հաշվի առնելով դրա ցածր արժեքը և ավելի բարձր արդյունավետությունը[32]։
Պատմություն[խմբագրել | խմբագրել կոդը]
ևրոպական միություն[խմբագրել | խմբագրել կոդը]
2006 թվականին ևրոպական դեղերի գործակալությունը (անգլ.՝ EMA-European Medicines Agency) Sanofi Pasteur-ին թույլտվություն տվեց վաճառել գոտևորող որքինի դեմ պատվաստանյութ՝ 60 տարեկան և ավելի բարձր տարիքի մարդկանց սովորական պատվաստումների համար[33][34]։ 2007 թվականին EMA-ն թարմացրեց վաճառքի թույլտվությունը 50 տարեկան և ավելի բարձր տարիքի անձանց սովորական պատվաստումների համար[33][35]։
Շինգրիքսը հաստատվել է բժշկական օգտագործման համար ևրամիությունում 2018-ի մարտին՝ 50 տարեկան և ավելի մեծահասակների մոտ հերպեսի զոստերի և հետերպետիկ նևրալգիայի կանխարգելման ցուցումով[36]։
Մեծ Բրիտանիա[խմբագրել | խմբագրել կոդը]
2013 թվականից Մեծ Բրիտանիայի Առողջապահության ազգային ծառայությունը (անգլ.՝ NHS-National Health Service) սկսեց տարեց մարդկանց առաջարկել գոտևորող որքինի պատվաստում։ 70 կամ 79 տարեկան մարդկանց 2013 թվականի սեպտեմբերի 1-ի դրությամբ առաջարկվել է պատվաստանյութ։ Այս ամսաթվին 71-ից 78 տարեկան մարդիկ հնարավորություն ունեցան գոտևորող որքինի պատվաստանյութ ստանալ միայն 79 տարեկան դառնալուց հետո[37]։ Սկզբում ենթադրվում էր, որ 70-ից 79 տարեկան մարդիկ պետք է պատվաստվեն, բայց ավելի ուշ NHS-ն հայտարարեց, որ պատվաստումների ծրագիրը կատարվում է փուլերով, քանի որ անիրագործելի կլինի մեկ տարվա ընթացքում 70 տարեկան բոլոր մարդկանց պատվաստել[38]։
2021 թվականին գոտևորող որքինի դեմ պատվաստումը հասանելի կլինի NHS-ում 70-ից 79 տարեկան մարդկանց համար[39]։ պատվաստումը կատարվում է զոստավաքսի մեկ դեղաչափով, բացառությամբ այն մարդկանց, որոնց համար զոստավաքսը համարվում է ոչ պիտանի, ինչպիսիք են իմունային համակարգի վրա ազդող հիվանդությունները, որոնց համար առաջարկվում է շինգրիքս պատվաստանյութը երկու դեղաչափով[39]։ NHS-ն ասել է. «գոտևորող որքինի պատվաստանյութը NHS-ում հասանելի չէ 80 և ավելի բարձր տարիքի մարդկանց համար, քանի որ այն ավելի քիչ արդյունավետ է թվում այս տարիքային խմբում»[39]։
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ «Zoster vaccine live (Zostavax) Use During Pregnancy». Drugs.com. 2020 թ․ հունվարի 3. Վերցված է 2020 թ․ հունվարի 23-ին.
- ↑ 2,0 2,1 2,2 2,3 Gershon AA, Breuer J, Cohen JI, Cohrs RJ, Gershon MD, Gilden D, և այլք: (July 2015). «Varicella zoster virus infection». Nature Reviews. Disease Primers. 1: 15016. doi:10.1038/nrdp.2015.16. PMC 5381807. PMID 27188665.
- ↑ 3,0 3,1 3,2 3,3 Saguil A, Kane S, Mercado M, Lauters R (November 2017). «Herpes zoster and postherpetic neuralgia: prevention and management». American Family Physician. 96 (10): 656–663. PMID 29431387.
- ↑ 4,0 4,1 4,2 4,3 Pan CX, Lee MS, Nambudiri VE (2022). «Global herpes zoster incidence, burden of disease, and vaccine availability: a narrative review». Therapeutic Advances in Vaccines and Immunotherapy. 10. doi:10.1177/25151355221084535. PMC 8941701. PMID 35340552.
- ↑ 5,0 5,1 «What everyone should know about Zostavax». Centers for Disease Control and Prevention, U.S. Department of Health & Human Services. 2018 թ․ հունիսի 18. Վերցված է 2018 թ․ նոյեմբերի 16-ին.
- ↑ 6,0 6,1 6,2 Tricco AC, Zarin W, Cardoso R, Veroniki AA, Khan PA, Nincic V, և այլք: (October 2018). «Efficacy, effectiveness, and safety of herpes zoster vaccines in adults aged 50 and older: systematic review and network meta-analysis». BMJ. 363: k4029. doi:10.1136/bmj.k4029. PMC 6201212. PMID 30361202.
- ↑ 7,0 7,1 Gagliardi AM, Andriolo BN, Torloni MR, և այլք: (November 2019). «Vaccines for preventing herpes zoster in older adults». The Cochrane Database of Systematic Reviews. 2019 (11). doi:10.1002/14651858.CD008858.pub4. PMC 6836378. PMID 31696946.
- ↑ «Herpes Zoster Vaccination». Centers for Disease Control and Prevention. 2015 թ․ հուլիսի 31. Վերցված է 2021 թ․ հոկտեմբերի 26-ին.
- ↑ 9,0 9,1 «Chapter 28a: Shingles (herpes zoster)». Green Book of immunisation (PDF). 2021 թ․ օգոստոսի 23. էջ 8. «The need for booster doses of either Shingrix and Zostavax has not yet been determined.»
- ↑ 10,0 10,1 Han DH (2017 թ․ հոկտեմբերի 25). «ACIP: New Vaccine Recommendations for Shingles Prevention». MPR. Վերցված է 2017 թ․ հոկտեմբերի 30-ին.
- ↑ Shah RA, Limmer AL, Nwannunu CE, Patel RR, Mui UN, Tyring SK (July 2019). «Shingrix for Herpes Zoster: A Review». Skin Therapy Letter. 24 (4): 5–7. PMID 31339679.
- ↑ 12,0 12,1 «Zostavax – zoster vaccine live injection, powder, lyophilized, for suspension Sterile Diluent – sterile water injection». DailyMed. 2019 թ․ սեպտեմբերի 26. Վերցված է 2020 թ․ սեպտեմբերի 6-ին.
- ↑ Mitka M (July 2006). «FDA approves shingles vaccine: herpes zoster vaccine targets older adults». JAMA. 296 (2): 157–158. doi:10.1001/jama.296.2.157. PMID 16835412.
- ↑ «FDA Licenses New Vaccine to Reduce Older Americans' Risk of Shingles» (Press release). U.S. Food and Drug Administration (FDA). 2006 թ․ մայիսի 26. Վերցված է 2009 թ․ հոկտեմբերի 31-ին.
- ↑ «Patient Information about Zostavax». U.S. Food and Drug Administration (FDA). May 2006. Արխիվացված է օրիգինալից 2009 թ․ հունիսի 19-ին. Վերցված է 2009 թ․ հոկտեմբերի 31-ին.
- ↑ «Patient Information about Zostavax (Text) 12/2008». U.S. Food and Drug Administration (FDA). December 2008. Արխիվացված է օրիգինալից 2009 թ․ օգոստոսի 27-ին. Վերցված է 2009 թ․ հոկտեմբերի 31-ին.
- ↑ «CDC's Advisory Committee Recommends "Shingles" Vaccination» (Press release). U.S. Centers for Disease Control and Prevention (CDC). 2006 թ․ հոկտեմբերի 26. Վերցված է 2009 թ․ հոկտեմբերի 31-ին.
- ↑ 18,0 18,1 18,2 18,3 18,4 18,5 «Shingles Vaccination: What Everyone Should Know». U.S. Centers for Disease Control and Prevention (CDC). 2022 թ․ մայիսի 24. Վերցված է 2023 թ․ հունվարի 1-ին.
- ↑ «Shingrix- zoster vaccine recombinant, adjuvanted kit». DailyMed. 2019 թ․ հոկտեմբերի 4. Վերցված է 2020 թ․ սեպտեմբերի 6-ին.
- ↑ 20,0 20,1 20,2 «About Zostavax». Merck Sharp & Dohme Corp. May 2018. Արխիվացված է օրիգինալից 2018 թ․ նոյեմբերի 17-ին. Վերցված է 2018 թ․ նոյեմբերի 16-ին.
- ↑ Harris S (2011 թ․ հունվարի 18). «Shingles Vaccine: Expert Q&A». WebMD. Վերցված է 2014 թ․ հունվարի 4-ին.
- ↑ Cunha JP. «Zostavax Side Effects Center». RxList. Վերցված է 2014 թ․ հունվարի 4-ին.
- ↑ «Zostavax vaccine». Therapeutic Goods Administration (TGA) (Press release). 2017 թ․ մարտի 7. Վերցված է 2020 թ․ հուլիսի 11-ին.
- ↑ «Zostavax vaccine». Therapeutic Goods Administration (TGA) (Press release). 2020 թ․ հուլիսի 6. Վերցված է 2020 թ․ հուլիսի 11-ին.
- ↑ «FDA Shingrix Briefing Document» (PDF). U.S. Food and Drug Administration (FDA). Վերցված է 2017 թ․ հոկտեմբերի 28-ին.
- ↑ «Shingles Vaccine (Zoster Shingles Vaccine Live, Zostavax)». Medicinenet.com. Վերցված է 2018 թ․ ապրիլի 29-ին.
- ↑ Davidson MW (2015 թ․ նոյեմբերի 13). «Human Fetal Lung Fibroblast Cells (MRC-5 Line)». Florida State University.
- ↑ Pellissier JM, Brisson M, Levin MJ (November 2007). «Evaluation of the cost-effectiveness in the United States of a vaccine to prevent herpes zoster and postherpetic neuralgia in older adults». Vaccine. 25 (49): 8326–8337. doi:10.1016/j.vaccine.2007.09.066. PMID 17980938.
- ↑ Harpaz R, Ortega-Sanchez IR, Seward JF (June 2008). «Prevention of herpes zoster: recommendations of the Advisory Committee on Immunization Practices (ACIP)» (PDF). MMWR. Recommendations and Reports. 57 (RR-5): 1–30, quiz CE2–4. PMID 18528318.
- ↑ Advisory Committee on Immunization Practices (November 2007). «Recommended adult immunization schedule: United States, October 2007-September 2008». Annals of Internal Medicine. 147 (10): 725–729. doi:10.7326/0003-4819-147-10-200711200-00187. PMID 17947396. S2CID 31630647.
- ↑ Dooling KL, Guo A, Patel M, Lee GM, Moore K, Belongia EA, Harpaz R (January 2018). «Recommendations of the Advisory Committee on Immunization Practices for Use of Herpes Zoster Vaccines». MMWR. Morbidity and Mortality Weekly Report (ամերիկյան անգլերեն). 67 (3): 103–108. doi:10.15585/mmwr.mm6703a5. PMC 5812314. PMID 29370152.
- ↑ Le P, Rothberg MB (February 2018). «Cost-effectiveness of the Adjuvanted Herpes Zoster Subunit Vaccine in Older Adults». JAMA Internal Medicine. 178 (2): 248–258. doi:10.1001/jamainternmed.2017.7431. PMC 5838796. PMID 29297049.
- ↑ 33,0 33,1 «Zostavax EPAR». European Medicines Agency (EMA). Վերցված է 2020 թ․ հուլիսի 31-ին.
- ↑ «Zostavax EPAR» (PDF). European Medicines Agency (EMA). July 2006. Վերցված է 2011 թ․ մարտի 27-ին.
- ↑ «Zostavax-H-C-674-II-03 Scientific Discussion» (PDF). 2007 թ․ հունիսի 21. Վերցված է 2011 թ․ մարտի 27-ին.
- ↑ «Shingrix EPAR». European Medicines Agency (EMA). Վերցված է 2020 թ․ հուլիսի 31-ին. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ↑ «Shingles Vaccination (16 July 2013, archived)». NHS UK. Արխիվացված օրիգինալից 2014 թ․ հունիսի 2-ին.
- ↑ «Who can have the shingles vaccine? (16 July 2013, archived)». NHS UK. Արխիվացված օրիգինալից 2014 թ․ ապրիլի 10-ին.
- ↑ 39,0 39,1 39,2 «Shingles vaccine overview». National Health Service (NHS). 2021 թ․ օգոստոսի 31. Վերցված է 2021 թ․ նոյեմբերի 26-ին.
