Յոդի պենտօքսիդ
| Յոդի պենտօքսիդ | |
|---|---|
 | |
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | յոդի (V) օքսիդ |
| Այլ անվանումներ | յոդական թթվի անհիդրիդ |
| Ավանդական անվանում | դիյոդի պենտօքսիդ |
| Քիմիական բանաձև | I₂O₅ |
| Ֆիզիկական հատկություններ | |
| Ագրեգատային վիճակ | բյուրեղային |
| Արտաքին տեսք | սպիտակ բյուրեղներ |
| Մոլային զանգված | 5,5E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 4,799 գ/սմ³ գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | տարբ. 300 °C (573 K) (քայքայվելով) °C |
| Քիմիական հատկություններ | |
| Դասակարգում | |
| CAS համար | 12029-98-0 |
| PubChem | 159402 |
| EINECS համար | 234-740-2 |
| SMILES | O=I(=O)OI(=O)=O |
| ЕС | 234-740-2 |
| ChEBI | 140179 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Յոդի պենտօքսիդը քիմիական միացություն է՝ I2O5 քիմիական բանաձևով. Այս յոդի օքսիդը յոդական թթվի անհիդրիդն է, և յոդի միակ կայուն օքսիդն է։ Ստացվում է յոդական թթվի դեհիդրատացումից՝ 200 °C ջերմաստիճանում՝ չոր օդի հոսքի պայմաններում։
2HIO3 → I2O5 + H2O
Կառուցվածք[խմբագրել | խմբագրել կոդը]
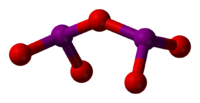
I2O5 ունի անկյունաձև կառուցվածք՝ 139.2° I-O-I ֆրագմենտով։ Մոլեկուլը չունի սիմետրիայի հարթություն հետևաբար նրա սիմետրիա էլեմենտը C2v չէ։ Ծայրային I-O կապերի երկարությունը 1.80 Å է և կամրջային I-O կապերի երկարությունը՝ 1.95 Å.[2]
Ստացում[խմբագրել | խմբագրել կոդը]
- Քլորի (VII) օքսիդով յոդի օքսիդացմամբ։
- Յոդական թթվի դեհիդրատացմամբ։
- Յոդի (V) ֆտորիդի և սիլիցիումի (IV) օքսիդի փոխազդեցությամբ։
Ֆիզիկական հատկություններ[խմբագրել | խմբագրել կոդը]
Յոդի պենտօքսիդը առաջացնում է անգույն (սպիտակ) բյուրեղներ, որոնք լույսի տակ քայքայման հետևանքով մգանում են։
Լավ լուծվում է ջրում և հեղուկ ֆտորաջրածնում, քիչ լուծելի է էթանոլում և գործնականում անլուծելի է բացարձակ էթանոլում, դիէթիլ եթերում, ծծմբածխածնում, քլորոֆորմում։
Քիմիական հատկություններ[խմբագրել | խմբագրել կոդը]
- Լույսի տակ քայքայվում է՝
- Փոխազդում է ջրի հետ՝
- փոխազդում է անջուր ծծմբական թթվի հետ։
- Ալկալիների հետ առաջացնում է յոդատներ։
- Հեղուկ ֆտորաջրածնում հնարավոր է փոխազդեցությունը ֆտորի հետ։
- Հանդիսանում է ուժեղ օքսիդիչ։
Ածխածնի մոնօքսիդի հետ ռեակցիան կարող է օգտագործվել գազային նմուշներում CO պարունակության հետազոտման համար։
Գրականություն[խմբագրել | խմբագրել կոդը]
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ 1,0 1,1 Iodine pentoxide
- ↑ Selte, K.; Kjekshus, A. (1970). «Iodine Oxides: Part III. The Crystal Structure of I2O5» (PDF). Acta Chemica Scandinavica. 24 (6): 1912–1924. doi:10.3891/acta.chem.scand.24-1912. Արխիվացված է օրիգինալից (pdf) 2013 թ․ հունիսի 10-ին. Վերցված է 2015 թ․ նոյեմբերի 26-ին.
{{cite journal}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link)










![{\displaystyle {\mathsf {I_{2}O_{5}+10HCl+2KCl\ {\xrightarrow {}}\ 2K[ICl_{4}]+2Cl_{2}\uparrow +5H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a90f5579e7ee87482f00c6e8b995d568ec80bb38)