Մասնակից:Annie-Art/Ավազարկղ 9
| Annie-Art/Ավազարկղ 9 | |
|---|---|
 | |
 | |
 | |
| Ընդհանուր տեղեկություններ | |
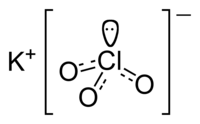
| Քիմիական բանաձև | KClO3 |
| Ֆիզիկական հատկություններ | |
| Ագրեգատային վիճակ | անգույն բյուրեղներ |
| Մոլային զանգված | 122.55 գ/մոլ |
| Խտություն | 2,32 գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | 356 °C |
| Դասակարգում | |
| CAS համար | [3811-04-9] |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Կալիումի քլորատ (Բերթոլեի աղ) — KCIOз, քլորական թթվի կալիումական աղ։ Անգույն բյուրեղներ, խտությունը՝ 2320 կգ/մ3, հալման ջերմաստիճանը՝ 356° С, թունավոր է, ջրում վատ է լուծվում (մոտ 7,5 գՀ 100 գ ջրում, 20°Շ–ում)։ Կալիումի քլորատը օքսիդիչ է, ծծմբի, ֆոսֆորի, ածխածնի և օրգանական նյութերի հետ առաջացնում է պայթուցիկ խառնուրդներ։ Ստացվում է KCl-ի ջրային լուծույթի էլեկտրոլիզով։ Օգտագործվում է լուցկու արդյունաբերությունում և պիրոտեխնիկայում, նաև քիմիական աշխատանոցում թթվածին ստանալու համար, իսկ բժշկության մեջ՝ որպես ախտահանիչ։
Պատմություն
[խմբագրել | խմբագրել կոդը]Առաջին անգամ ստացվել է 1786 թվականին Կլոդ Բերթոլեի կողմից (այստեղից էլ անվանումը` Բերթոլեի աղ), քլորը, տաք խտացրած կալիումի հիդրօքսիդով անց կացնելով:

Քիմիական հատկություններ
[խմբագրել | խմբագրել կոդը]Տաքացնելիս (400°С) քայքայվում է՝ առաջացնելով KCIO4, ավելի բարձր ջերմաստիճաններում (550- 600°С)՝ կալիումի քլորիդ և թթվածին։
- (400 °C);
- (550—620 °C)
Կատալիզատորների (MnO2, Fe2O3, CuO) առկայությամբ քայքայվում է ավելի ցածր ջերմաստիճաններում (200°C)։
- (150—300 °C, կատ. MnO2)
Ջրասպիրտային լուծույթում ռեակցիայի մեջ է մտնում ամոնիումի սուլֆատի հետ, առաջացնելով ամոնիումի քլորատ:
Կիրառում
[խմբագրել | խմբագրել կոդը]Այրվող նյութեր
[խմբագրել | խմբագրել կոդը]Կալիումի քլորատի խառնուրդները վերականգնիչների հետ (ֆոսֆոր, ծծումբ, օրգանական միացություններ) պայթուցիկ և զգայուն են շփման, հարվածների նկատմամբ: Զգայունությունը ավելանում է բրոմատների և ամոնիումի աղերի առկայությամբ: Բերթոլեի աղի հետ բաղադրության բարձր զգայունության պատճառով, նրանք գրեթե չեն օգտագործվում արդյունաբերական և ռազմական պայթուցիկ նյութերի արտադրության համար: Երբեմն օգտագործվում է հրարվեստում, որպես քլորատի աղբյուր, մտնում է լուցկու գլխիկի այրվող նյութի բաղադրության մեջ:
Բժշկության մեջ
[խմբագրել | խմբագրել կոդը]Որոշ ժամանակ կալիումի քլորատի լուծույթները կիրառվում էին թույլ հականեխիչի տեղ, արտաքին դեղամիջոց կոկորդ ողողելու համար:
Թունավորություն
[խմբագրել | խմբագրել կոդը]Կալիումի քլորատի մահացու չափը կազմում է 1գ/կգ:





