Էթիլենգլիկոլ
| Էթիլենգլիկոլ | |
|---|---|
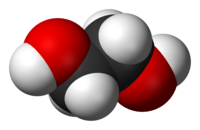 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | Էթիլենգլիկոլ |
| Ավանդական անվանում | գլիկոլ Էթիլենգլիկոլ, 1,2-դիօքսիէթան, 1,2-էթանդիոլ |
| Քիմիական բանաձև | C₂H₆O₂ |
| Ռացիոնալ բանաձև | C2H4(OH)2 |
| Ֆիզիկական հատկություններ | |
| Մոլային զանգված | 1,0E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 1,11 ± 0,01 գ/սմ³[2] գ/սմ³ |
| Դինամիկ մածուցիկություն | 5.9×10−4 Պա/վ |
| Իոնիզացման էներգիա | 1,6E−18 ջոուլ[3] կՋ/մոլ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | 9 ± 0 ℉[2] և −13 °C[4][3] °C |
| Եռման ջերմաստիճան | 388 ± 1 ℉[2], 197 °C[5] և 197,34 °C[3] °C |
| Այրման ջերմաստիճան | 232 ± 1 ℉[2] |
| Բռնկման ջերմաստիճան | +111 °C |
| Եռյակ կետ | 175,45 K (−97,7°C) |
| Կրիտիկական ճնշում | 513,15 K (240 °C), 7,85 բար մթն. |
| Գոյացան էնթալպիա | −234,8 կՋ/մոլ |
| Եռման էնթալպիա | 50,5 կՋ/մոլ[6] և 57,4 կՋ/մոլ[7] կՋ/մոլ |
| Գոլորշու ճնշում | 7900 megapascal[8] |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջր-ում | անսահմանափակ գ/100 մլ |
| pKa | 15,1 ± 0,1[8] |
| Բեկման ցուցիչ | 1,3811[9] |
| Դիպոլ մոմենտ | 7,6E−30 Կլ·մ[3] |
| Դասակարգում | |
| CAS համար | 107-21-1 |
| PubChem | 174 |
| EINECS համար | 203-473-3 |
| SMILES | C(CO)O |
| ЕС | 203-473-3 |
| RTECS | KW2975000 |
| ChEBI | 13835235 |
| Թունավորություն | |
| Թունավորություն |   |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Էթիլենգլիկոլ կամ էթանդիոլ, HO—CH2—CH2—OH, երկատոմ սպիրտ, բազմատոմ սպիրտերի պարզագույն ներկայացուցիչ։
Նկարագրություն[խմբագրել | խմբագրել կոդը]
Անգույն, անհոտ, մածուցիկ հեղուկ է, հալման ջերմաստիճանը՝ 12,3 °C, եռմանը՝ 197,6 °C: Նյութի խտությունը կազմում է 1113 կգ/մ խորանարդ։ Լուծվում է ջրում և շատ օրգանական լուծիչներում, եթերում քիչ է լուծվում։ Էթիլենգլիկոլը ունի գլիկոլներին բնորոշ բոլոր հատկությունները։ Ծծմբական թթվի հետ թորելիս առաջացնում է դիօքսան, մեկ մոլեկուլ ջուր պոկելիս՝ քացախալդեհիդ և այլն։ Էթիլենգլիկոլը ստացվում է 1,2 դիքլորէթանի հիդրոլիզից, էթիլենօքսիդի և ջրի փոխազդեցությունից (արտադրական եղանակ) և այլն։
Էթիլենգլիկոլի խառնուրդը ջրի հետ օգտագործվում է որպես հակասառեցուցիչ միջոց (հայրենական արդյունաբերությունը թողարկում է 40 և 65 մակնիշի էթիլենգլիկոլային հակասառեցուցիչներ, համապատասխանաբար –40 °C և –65 °C սառեցման ջերմաստիճաններով)։
Էթիլենգլիկոլը լայնորեն կիրառվում է նաև պլաստմասսաների, արհեստական մանրաթելերի և այլ նյութերի արտադրության մեջ։
Պատմություն[խմբագրել | խմբագրել կոդը]
Էթիլենգլիկոը առաջին անգամ ստացվել է 1859 թվականին ֆրանսիացի քիմիկոս Շառլ Ադոլֆ Վյուրցի կողմից՝ էթիլենգլիկոլի դիացետատի և կալիումի հիդրօքսիդի օճառացումից (լուծումից), և 1860-ականներին՝ էթիլենօքսիդի հիդրատացումով։ Այն մեծ պահանջ չէր վայելում մինչև Առաջին համաշխարհային պատերազմը, երբ Գերմանիայում սկսեցին ստանալ դիքլորէթանի միջոցով, պայթուցիկ նյութեր արտադրելու համար գլիցերինը փոխարինելով էթիլենգլիկոլով։
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ 1,0 1,1 ETHYLENE GLYCOL
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 http://www.cdc.gov/niosh/npg/npgd0272.html
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 4,0 4,1 Bradley J., Williams A. J., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // Figshare — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ 5,0 5,1 https://comptox.epa.gov/dashboard/DTXSID8020597
- ↑ 6,0 6,1 https://pubchem.ncbi.nlm.nih.gov/compound/174#section=Heat-of-Vaporization
- ↑ 7,0 7,1 https://webbook.nist.gov/cgi/cbook.cgi?ID=C107211&Mask=4
- ↑ 8,0 8,1 http://sitem.herts.ac.uk/aeru/ppdb/en/Reports/1310.htm
- ↑ http://www.refractometer.pl/refraction-datasheet-ethylene-glycol
Արտաքին հղումներ[խմբագրել | խմբագրել կոդը]
- Էթիլենգլիկոլը օնլայն ուղեցույց-գրքում
- Էթիլենգլիկոլ հանրամատչելի քիմիա, քիմիան բոլորի համար
- Քիմիական ռեակցիաներ և փոխազդեցություններ՝ էթիլենգլիկոլ
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Էթիլենգլիկոլ» հոդվածին։ |
| ||||||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 4, էջ 8)։ |
