Ազատ ռադիկալներ
| Այս հոդվածն աղբյուրների կարիք ունի։ Դուք կարող եք բարելավել հոդվածը՝ գտնելով բերված տեղեկությունների հաստատումը վստահելի աղբյուրներում և ավելացնելով դրանց հղումները հոդվածին։ Անհիմն հղումները ենթակա են հեռացման։ |
Ազատ ռադիկալներ, գազում և կոնդենսացված ֆազում, ինչպես նաև կենդանի օրգանիզմում տեղի ունեցող բազմաթիվ կենսաքիմիական պրոցեսներում չափազանց կարևոր դեր են խաղում ազատ ռադիկալները։
Ազատ ռադիկալներ են կոչվում այն մասնիկները, որոնց վալենտային օրբիտալում կա մեկ կամ ավելին չզույգված էլեկտրոն։ Ազատ ռադիկալները քիմիապես շատ ակտիվ են, եթե ազատ վալենտականությունը ինչ-ոտ պատճառով, օրինակ, մոլեկուլի ներսում կրկնակի կապերի հետ զուգորդման հետևանքով չի տեղայնացվում (լոկալացվում)։ Ռադիկալներ կարող են առաջանալ ոչ ռադիկալային մոլեկուլներից մեկ էլեկտրոնի կորուստի
կամ կցման դեպքում։
Ազատ ռադիկալներ իրենց ակտիվությամբ իրարից զգալիորեն տարբերվում են։ Օրինակ, ալկիլ ազատ ռադիկալները՝ H3*C, R*CH2 և այլն, շատ ռեակցունակ են։ Այդ պատճառով էլ դրանք ազատ վիճակում ստանալ, ռեակցիոն խառնուրդից անջատել բավականին դժվար է։ Ազատ ռադիկալների ռեակցունակությունը զգալիորեն նվազում է, երբ կենտ էլեկտրոնը հնարավորություն է ստանում զուգորդվելու π կապերի հետ։ Հաճախ քիմիական ռեակցիաների մեխանիզմի պարզաբանման նպատակով լայնորեն կիրառվում են կայուն ազատ ռադիկալները։ Կիրառական նշանակություն ունեցող ազատ ռադիկալներից են դիֆենիլպիկրիլ հիդրազիլը (սև-մանուշակագույն բյուրեղային նյութ է), մուգ կապույտ գալվին օքսիլ ազատ ռադիկալը և այլն։
Ազատ ռադիկալների հայտնաբերման եղանակները։[խմբագրել | խմբագրել կոդը]
Օպտիկական եղանակ[խմբագրել | խմբագրել կոդը]
- Ազատ ռադիկալն ունի յուրահատուկ կլանման սպեկտր, որը տարբերվում է համապատասխան իոնի կամ մոլեկուլի կլանման սպեկտրից։ Այս եղանակով առաջին անգամ Կոնդրատևի կողմից փորձնականորեն ոչ միայն ապացուցվեց *OH ազատ ռադիկալների առկայությունը ջրածնի և թթվածնի բոցում, այլև որոշվեց դրանց կոնցենտրացիան։
Մասսպեկտորոսկոպիկական եղանակ[խմբագրել | խմբագրել կոդը]
- Այս եղանակը սկսվել է կիրառվել 1942 թվականից։ Ինչպես հայտնի է, լիցքավորված մասնիկները անցնելով էլեկտրաստատիկ և էլեկտրամագնիսական միջով, ունենում են հետագծի որոշ կորացում։ Որոշելով կորացման շառավիղը՝ r-ը և իմանալով էլեկտրաստատիկ և էլեկտրամագնիսական դաշտերի լարվածությունը՝ V և H, կարելի է որոշել հետազոտվող մասնիկի լիցքը (e) և զանգվածի (m) հարաբերությունը։ Այս հարաբերությունը բնութագրական է յուրաքանչյուր մասնիկի համար։ Ստացված սպեկտրալ գծերի սաստկության միջոցով հնարավոր է կատարել նաև քանակական անալիզ։ Այստեղ դժվարությունն այն է, որ մասնիկները ռմբակոծող էլեկտրոնների էներգիան պետք է ընտրել այնպիսին, որ իոնանա միայն ռեակցիայի հետևանքով գոյանա ազատ ռադիկալը R+e--—›R++2e- , և ոչ թե վերջինս առաջանա ռեագենտի մոլեկուլի և ռմբակոծող էլեկտրոնի փոխազդեցության հետևանքով. RX+e--—›R++X+2e-:
Էլեկտրոնային պարամագնիսական ռեզոնանսի եղանակ[խմբագրել | խմբագրել կոդը]
- Քիմիական ռեակցիաների ընթացքում գոյացող ռադիկալների բնույթն ու քանակը որոշելու առումով այս եղանակը ժամանակակից ամենահզոր միջոցներից է։ Այն հիմնված է ազատ ռադիկալների պարամագնիսական հատկությամբ օժտված լինելու վրա։ Մագնիսական դաշտում գտնվող պարամագնիսկան չզույգված էլեկտրոն պարունակող նյութը ընդունակ է էլեկտրամագնիսական ալիքների ռեզոնանսային կլանման։ Պարամագնիսի դերում կարող են հանդես գալ ատոմներ (H, O, F և այլն), որոշ իոններ (Cu2+, Ag+), ազատ ռադիկալներ (HO*, ROO*), կայուն ռադիկալներ։
- Քվանտացման կանոնների համաձայն s = ½ սպինով մասնիկի (օրինակ, էլեկտրոնի) համար հնարավոր են մագնիսական մոմենտի երկու ուղղվածություններ` մագնիսական դաշտին զուգահեռ և հակազուգահեռ։ Այսպիսի յուրաքանչյուր ուղղվածությանը կհամապատասխանի որոշակի փոխազդեցություն մագնիսական դաշտի և պարամագնիսի պարամագնիսկան մոմենտի միջև։ Այս փոխազդեցության հետևանքով չզույգված էլեկտրոնի սկզբնական էներգետիկ մակարդակը (Eսկզբ.) կտրոհվի (2s+1) ենթամակարդակների (Զեմանի էֆեկտ)։ Էլեկտրոնի դեպքում, երբ s = ½ , Еսկզբ.-ը կտրոհվի E1 և E2 էներգիաներով օժտված երկու ենթամակարդակների, ըստ որում ∆E= E1-E2=gβH,(1) որտեղ g-ն կոչվում է սպեկտրոսկոպիկ ճեղքման գործակից կամ g-գործակից։ Ազատ սպինի համար g-ն հավասար է 2.0023-ի։ β-ն Բորի մագնետոնն է ( β= eℏ/2mc,) իսկ H-ը կիրառված հաստատուն մագնիսական դաշտի լարվածությունն է արտահայտված էրստեդներով (նկար 1)։

Յուրաքանչյուր ենթամակարդակում չզույգված էլեկտրոնների բնակեցվածությունը որոշվում է Մաքսվել-Բոլցմանի բաշխման ֆունկցիայով։ Եթե E1 ենթամակարդակի վրա կա n1 հատ էլեկտրոն և E2-ի վրա՝ n2 հատ, ապա n1/n2 =exp(-∆E/KT)=exp(-gβH/KT) Այս հավասարման մեջ n1-ը և n2-ը հավասարակշռական մեծություններ են։ քանի որ E1>E2, ապա n1<n2։
Եթե այժմ քննարկվող համակարգի վրա ազդենք հաստատուն մագնիսական դաշտին ուղղահայաց գերբարձր հաճախության (ν) էլեկտրամագնիսական դաշտով, ապա (1) ռեզոնանսային պայմանը իրագործվելու դեպքում էլեկտրոնները ներքին մակարդակից կանցնեն վերին մակարդակը։ Տեղի կունենա էներգիայի կլանում։ Սակայն միաժամանակ տեղի է ունենում նաև հակառակ անցումը՝ վերին մակարդակից ներքին մակարդակ, որի դեպքում էներգիա է անջատվում։ Երկու հակառակ ուղղությամբ անցումները հավասար հավանական են, բայց քանի որ n2-ը n1-ից մեծ է, ուստի կգերակշռի ներքևից վերև անցումը։
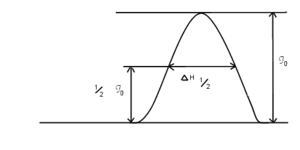
Թվում է, թե ժամանակի ընթացքում երկու հակառակ ուղղություններով անցումների արագությունները իրար պետք է հավասարվեն, որովհետև n2-ը պետք է մեծանա, իսկ n1-ը՝ նվազի։ Բայց իրականում Բոլցմանյան բաշխումը անփոփոխ է մնում։ Հավելյալ էներգիայով օժտված վերևի մակարդակի բնակիչները մի կողմից էներգիա են փոխանակում շրջապատի (միջավայրի) հետ, որը կոչվում է «ցանց», մյուս կողմից տեղի է ունենում էներգիայի փոխանակում ազատ սպինների միջև։ Այս երկու պրոցեսները, որոնք ապահովում են Բոլցմանյան բաշխման անխախտ մնալը, քանակապես բնութագրվում են հավասարակշռական վիճակին նորից մոտենալու ժամանակով, որը կոչվում է ռելակսացման ժամանակ։ Առաջին դեպքում գործ ունենք սպին-«ցանցային» ռելակսացման հետ, իսկ երկրորդ դեպքում՝ սպին-սպինային ռելակսացման հետ։ Հավասարակշռությանը հասնելու տևողությունները համապատասխանաբար կոչվում են սպին-«ցանցային» և սպին-սպինային ռելակսացման ժամանակ և քանի որ դրանք սովորաբար շատ փոքր մեծություններ են, ուստի անընդհատ կլանում է արձանագրվում։ Ինքնաշխատ ռադիոսպեկտրոմետրը գրանցում է կլանված էներգիայի սաստկության (ինտենսիվության) կախումը ըստ մեծության մոնոտոն փոփոխվող հաստատուն մագնիսական դաշտից ֆիքսված ν–ի տակ (նկար 2)։
- Զգայնությունը բարձրացնելու նպատակով սովորաբար գործիքը արձանագրում է ստացված կորագծի առաջին ածանցյալը (նկար 3)։
 Այս պատկերը կոչվում է ԷՊՌ սպեկտր (կամ ազդանշան)։
Այս պատկերը կոչվում է ԷՊՌ սպեկտր (կամ ազդանշան)։
- ԷՊՌ սպեկտրը բնութագրվում է հետևյալ պարամետրերով. կլանման սաստկությամբ (գծված մակերեսը), որը համեմատական է չզույգված էլեկտրոնների թվին (կոնցենտրացիային), g-գործակցով, ազդանշանի լայնությամբ և տեսքով, ինչպես նաև սպեկտրի նուրբ և գերնուրբ կառուցվածքով։ Այս վերջին երեք պարամետրերը հնարավորություն են տալիս բացահայտելու ազատ ռադիկալի (կամ ատոմի) բնույթը։ Ժամանակակից գործիքները կարող են գրանցել ~1010 սպին/մլ կամ ~10-10 մոլ/լ։
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Ազատ ռադիկալներ» հոդվածին։ |
| ||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 1, էջ 96)։ |





