«Գլիցերին»–ի խմբագրումների տարբերություն
չ թարգմանում եմ անգլերեն ամսանունները oգտվելով ԱՎԲ |
չ Ռոբոտ․ Տեքստի ավտոմատ փոխարինում (- <ref +<ref) |
||
| Տող 120. | Տող 120. | ||
== Կիրառություն == |
== Կիրառություն == |
||
Գլիցերինի կիրառության ոլորտները շատ բազմազան են։ Օգտագործվում է սննդային հավելանյութերում, լվացող և կոսմետիկ միջոցներում, [[պլաստմասսա]]ների արտադրությունում, ներկանյութերի արտադրությունում, [[էլեկտրատեխնիկա]]յում, ռադիոտեխնիկայում և այլն։ Համարակալված է որպես սննդային հավելում |
Գլիցերինի կիրառության ոլորտները շատ բազմազան են։ Օգտագործվում է սննդային հավելանյութերում, լվացող և կոսմետիկ միջոցներում, [[պլաստմասսա]]ների արտադրությունում, ներկանյութերի արտադրությունում, [[էլեկտրատեխնիկա]]յում, ռադիոտեխնիկայում և այլն։ Համարակալված է որպես սննդային հավելում<ref>E422</ref><ref>[http://web.archive.org/web/20150212152226/http://www.fiaformulae.com/en/news/2014/september/formula-e-uses-pollution-free-glycerine-to-charge-cars.aspx Formula E uses pollution-free glycerine to charge cars]. fiaformulae.com. 13 September 2014</ref>։ Գլիցերինը օգտագործվում է նաև [[դինամիտ]]ի ստացման համար։ |
||
== Կայքեր == |
== Կայքեր == |
||
12:03, 30 Դեկտեմբերի 2016-ի տարբերակ
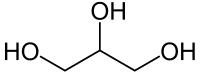
| Գլիցերին | |
|---|---|
 | |
 | |
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | Պրոպանտրիոլ-1,2,3 |
| Ավանդական անվանում | Գլիցերին |
| Քիմիական բանաձև | HOCH2-CH(OH)-CH2OH |
| Ռացիոնալ բանաձև | C3H5(OH)3 |
| Ֆիզիկական հատկություններ | |
| Մոլային զանգված | 92,1 գ/մոլ |
| Խտություն | 1,261 գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | 18 °C |
| Կազմալուծման ջերմաստիճան | 554 ± 1 ℉[1] |
| Եռման ջերմաստիճան | 290 °C |
| Այրման ջերմաստիճան | 320 ± 1 ℉[1] և 160 °C |
| Գոլորշու ճնշում | 0,003 ± 0,001 mm Hg[1] |
| Օպտիկական հատկություններ | |
| Բեկման ցուցիչ | 1,4729 |
| Դասակարգում | |
| CAS համար | 56-81-5 |
| PubChem | 753 |
| EINECS համար | 200-289-5 |
| SMILES | OCC(O)CO |
| ЕС | 200-289-5 |
| RTECS | MA8050000 |
| ChEBI | 733 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Գլիցերին, (1,2,3-տրիօքսիպրոպան, պրոպանտրիոլ-1,2,3), եռատոմ սպիրտների պարզ ներկայացուցիչ[2]։ Իրենից ներկայացնում է մածուցիկ, թափանցիկ հեղուկ[3]։
Ֆիզիկական հատկություններ
Գլիցերինը անգույն, մածուցիկ, շատ հիգրոսկոպիկ հեղուկ է[4]։ Ունի քաղցր համ, այստեղից էլ ստացել է իր անվանումը(գլիկոս-քաղցր)[5]։
Քիմիական հատկություններ
Գլիցերինը ունի տիպիկ բազմատոմ սպիրտներին բնորոշ քիմիական հատկություններ[6]։ Գլիցերինի փոխազդեցությունը հալոգենաջրածինների կամ ֆոսֆորի հալոգենիդների հետ ընթանում է մոնո- և դիհալոգենացմամաբ[7]։ Գլիցերինը փոխազդում է կարբոնաթթուների և հանքային թթուների հետ[8]։ Օրինակ ազոտական թթվի հետ փոխազդելիս, գլիցերինն առաջացնում է եռնիտրատ-նիտրոգլիցերին(ստացել է Ասկանյո Սոբրերոն, 1847 թվականին), օգտագործվում է մեր ժամանակներում անծուխ վառոդ ստանալու նպատակով։ Գլիցերինը դեհիդրատացնելիս այն վեր է ածվում թունավոր ակրոլեինի[9][10].
- HOCH2-CH(OH)-CH2OH H2C=CH-CHO + 2 H2O
Այն օքսիդանում է մինչև գլիցերինային ալդեհիդ CH2OHCHOHCHO, դիհիդրօքսիացետոն CH2OHCOCH2OH կամ գլիցերինաթթու CH2OHCHOHCOOH։ Գլիցերինի և բարձրագույն կարբոնաթթուների եթերները՝ ճարպերը հանդիսանում են շատ կարևոր միացություններ մարդու համար, կարևոր կենսաբանական դեր են խաղում նաև ֆոսֆոլիպիդները[11]։
Ստացում
Գլիցերին առաջին անգամ ստացել է Շելեն 1779 թվականին, ճարպերի օճառացմամբ[12]։ Գլիցերինի հիմնական մասը ստանում են ճարպերի օճառացումից[13]։ Գլիցերինի ստացման սինթետիկ եղանակների հիմնական մասը հիմնված է պրոպիլենի օգտագործման վրա[14]։ 450-500 °C ջերմաստիճաններում պրոպիլենի քլորացումից ստանում են ալիլքլորիդ, HClO-ի հետ միանալիս առաջանում են քլորհիդրիններ, օրինակ՝ CH2ClCHOHCH2Cl, որը ալկալիով մշակելիս առաջանում է գլիցերին[15]։ Գլիցերին կարելի է ստանալ նաև օսլայի հիդրոլիզի միջոցով, առաջացած մոնոսախարիդների հիդրատացմամբ կամ շաքարների սպիրտային խմորումից[16][17]։

Գլիցերինի ածանցյալներ
Գլիցերիդներ
Եռգլիցերիդները հանդիսանում են գլիցերինի ածանցյալներ[18]։ Եռգլիցերիդները հանդիսանում են կարևոր բաղադրիչ՝ կենդանի օրգանիզմներում նյութափոխանակության գործընթացներում[19][20]։
Ճարպեր և յուղեր
Ճարպերը և յուղերը հիդրոֆոբ միացություններ են, ջրում անլուծելի, այնպես ինչպես գլիցերինի մոլեկուլում հիդրօքսիլ խմբերը փոխարինված են ճարպաթթուների մնացորդներով[21][22]։
Կիրառություն
Գլիցերինի կիրառության ոլորտները շատ բազմազան են։ Օգտագործվում է սննդային հավելանյութերում, լվացող և կոսմետիկ միջոցներում, պլաստմասսաների արտադրությունում, ներկանյութերի արտադրությունում, էլեկտրատեխնիկայում, ռադիոտեխնիկայում և այլն։ Համարակալված է որպես սննդային հավելում[23][24]։ Գլիցերինը օգտագործվում է նաև դինամիտի ստացման համար։
Կայքեր
Ռուսերեն և անգլերեն լեզուներով.
Անգլերեն լեզվով.
- What is Glycerin?
- Glossary for the Modern Soap Maker
- Glycerol soap
- Absolute alcohol using glycerol
- Computational Chemistry Wiki
- Health.gov dietary guidelines
Ծանոթագրություններ
- ↑ 1,0 1,1 1,2 http://www.cdc.gov/niosh/npg/npgd0302.html
- ↑ Datta, Rasek Lal (1914). «The Preparation of Allyl Iodide». Journal of the American Chemical Society. 36 (5): 1005–1007. doi:10.1021/ja02182a023.
- ↑ Johnson, Duane T.; Taconi, Katherine A. (2007). «The glycerin glut: Options for the value-added conversion of crude glycerol resulting from biodiesel production». Environmental Progress. 26 (4): 338. doi:10.1002/ep.10225.
- ↑ «Dow achieves another major milestone in its quest for sustainable chemistries» (Press release). Dow Chemical Company. մարտի 15, 2007.
- ↑ Christoph, Ralf; Schmidt, Bernd; Steinberner, Udo; Dilla, Wolfgang; Karinen, Reetta (2006). «Glycerol». Ullmann's Encyclopedia of Industrial Chemistry. Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a12_477.pub2. ISBN 3527306730.
- ↑ Sims, Bryan (հոկտեմբերի 25, 2011). «Clearing the Way for Byproduct Quality: Why quality for glycerin is just as important for biodiesel». Biodiesel Magazine.
- ↑ Yazdani, S. S. and Gonzalez, R. (2007). «Anaerobic fermentation of glycerol: a path to economic viability for the biofuels industry». Current Opinion in Biotechnology. 18 (3): 213–219. doi:10.1016/j.copbio.2007.05.002. PMID 17532205.
{{cite journal}}: Unknown parameter|laydate=ignored (օգնություն); Unknown parameter|laysource=ignored (օգնություն); Unknown parameter|laysummary=ignored (օգնություն)CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Yu, Bin (2014). «Glycerol». Synlett. 25 (4): 601. doi:10.1055/s-0033-1340636.
- ↑ Walt Bogdanich (մայիսի 6, 2007). «From China to Panama, a Trail of Poisoned Medicine». New York Times. Վերցված է մայիսի 8, 2007-ին.
- ↑ «10 Biggest Medical Scandals in History». փետրվարի 20, 2013.
- ↑ Stevens, Alan. «Preserving flowers and decorative foliages with glycerin and dye» (PDF).
- ↑ Nikolov, Ivan. «Functional Food Design Rules».
- ↑ Chemicals in Film
- ↑ «Glycerin Enema». Drugs.com. Վերցված է նոյեմբերի 17, 2012-ին.
- ↑ «Glycerin (Oral Route)». Mayo Foundation for Medical Education and Research. Վերցված է նոյեմբերի 17, 2012-ին.
- ↑ Long, Walter S. (14 January 1916 – 13 January 1917). «The Composition of Commercial Fruit Extracts». Transactions of the Kansas Academy of Science. 28: 157–161. doi:10.2307/3624347. JSTOR 3624347.
- ↑ Does Alcohol Belong In Herbal Tinctures? newhope.com
- ↑ Leffingwell, Georgia and Lesser, Miton (1945) GLYCERIN – Its Industrial and Commercial Applications. Chemical Publishing Co., Inc., Brooklyn, NY.
- ↑ Lawrie, James W. (1928) GLYCEROL AND THE GLYCOLS – Production, Properties and Analysis. The Chemical Catalog Company, Inc., New York, NY.
- ↑ The Manufacture of GLYCEROL – Vol. III (1956). The Technical Press, LTD., London, UK.
- ↑ Hudgens, R. Douglas; Hercamp, Richard D.; Francis, Jaime; Nyman, Dan A.; Bartoli, Yolanda (2007). «An Evaluation of Glycerin (Glycerol) as a Heavy Duty Engine Antifreeze/Coolant Base». doi:10.4271/2007-01-4000.
{{cite journal}}: Cite journal requires|journal=(օգնություն) - ↑ Proposed ASTM Engine Coolant Standards Focus on Glycerin. Astmnewsroom.org. Retrieved on 15 August 2012.
- ↑ E422
- ↑ Formula E uses pollution-free glycerine to charge cars. fiaformulae.com. 13 September 2014
| ||||||||||||||||||||||||||||||

