Ածխածնի օքսիդներ

Ածխածնի օքսիդներ, ածխածնի միացությունները թթվածնի հետ։ Տարածված են երկօքսիդը՝ CO2 և օքսիդը՝ CO։ Հայտնի է նաև ենթօքսիդը՝ C3O2։
Ածխածնի երկօքսիդ[խմբագրել | խմբագրել կոդը]
Ածխածնի երկօքսիդը (ածխաթթվական գազ, ածխաթթվական անհիդրիդ) ածխածնի և օրգանական միացությունների այրման վերջնական արդյունքն է։
Հատկություններ[խմբագրել | խմբագրել կոդը]
Անգույն, թույլ թթվահոտ և թթվահամ, օդից 1,5 անգամ ծանր գազ է։ Հեղուկանում է միայն բարձր ճնշումների տակ։ Մթնոլորտային ճնշման տակ պնդանում է առանց հեղուկանալու (-78,52 °C)՝ առաջացնելով «չոր սառույց»։ Լուծվում է ջրում՝ առաջացնելով ածխաթթու, հիմքերում՝ կարբոնատներ, և օրգանական լուծիչներում։
Քիմիապես իներտ է։ Բարձր ջերմաստիճաններում օքսիդացնում է ածխածինը և որոշ մետաղներ։ Օդը, որպես խառնուրդ, պարունակում է ~ 0,03 ծավալային % CO2։ Այն առաջանում է կենդանի օրգանիզմներում որպես նյութափոխանակման արդյունք և օրգանական միացությունների քայքայման, այրման, խմորման ժամանակ։ Կարևոր դեր ունի բույսերի կյանքում (տես Ֆոտոսինթեզ)։
Ստացում[խմբագրել | խմբագրել կոդը]
Արդյունաբերության մեջ ստանում են կրաքարի կիզումով։

|

| ||||
| CO Ածխածնի մոնօքսիդ |
CO2 Ածխաթթու գազ |
C3O2 Ածխածնի եռօքսիդ |
C12O9 |
C3O | CO4 |
Կիրառում[խմբագրել | խմբագրել կոդը]
Օգտագործվում է հիմնականում շաքարի, գարեջրի, զովացուցիչ և հանքային ջրերի, պահածոների, սոդայի, միզանյութի արդյունաբերության մեջ, ինչպես նաև կրակմարիչներում։ «Չոր սառույցը» օգտագործվում է որպես սառեցնող միջոց։ CO2-ի փոքր քանակները (<3%) օդում թունավոր չեն, մեծ քանակները (>10%) առաջացնում են շնչառական օրգանների գրգռում, աղմուկ ականջներում, գլխապտույտ և կենսակենտրոնների կաթված։
Ֆիզիկական հատկություններ[խմբագրել | խմբագրել կոդը]
Ածխածնի օքսիդը (շմոլք գազ) անգույն, անհոտ թունավոր գազ է (եռման ջերմաստիճանը՝ -191,5 °C, հալմանը՝ -205 °C)։ Ջրում վատ է լուծվում։ Օդում բռնկվում (700 °C) և այրվում է կապույտ բոցով։
Քիմիական հատկություններ[խմբագրել | խմբագրել կոդը]
Սենյակի ջերմաստիճանում MnO–ի և CuO-ի առկայությամբ օքսիդանում է մինչև CO2։ Այդ հատկությունն օգտագործվում է հակագազերում՝ օդը շմոլք գազից մաքրելու համար։ Տաքացնելիս վերականգնում է մետաղների օքսիդները։ Միանում է ծծմբի և քլորի հետ՝ առաջացնելով ծծմբածխածին և ֆոսգեն, մետաղների հետ՝ կարբոնիլներ և կարբիդներ, հիմքերի հետ՝ մրջնաթթվի աղեր։
Ծխնելուզային գազերը պարունակում են 1–4%, ավտոմեքենայի ծուխը՝ 2-10%, ծխախոտինը՝ 0,5% CO։ Չնչին քանակությամբ կա օդում։ Հայտնաբերվել է նաև Արեգակի մթնոլորտում։
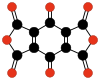
|
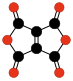
|
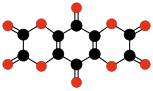
| |||
| C10O8 | C6O6 | C10O10 | |||

|

|

| |||
| C8O8 | C4O6 | C12O12 | |||
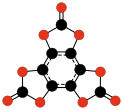
|
|
| |||
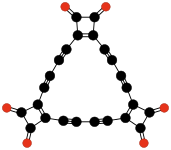
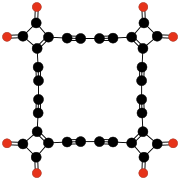
| C9O9 | C24O6 | C32O8 | |||
| |||||
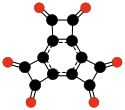
| C12O6 |
Ստացում[խմբագրել | խմբագրել կոդը]
Արդյունաբերության մեջ ստացվում է ածխի թերայրմամբ։ Օգտագործվում է որպես գազային վառելանյութ (լուսագազ, ջրագազ, գեներատորային գազ), ելանյութ՝ բազմաթիվ օրգանական միացությունների (սպիրտներ, օրգանական թթուներ, ալդեհիդներ, արհեստական բենզին՝ սինտին և այլն) և մի շարք մետաղների ստացման համար։ Ածխածնի օքսիդով թունավորումը օրգանիզմում առաջացնում է թթվածնի սով։ Առաջին օգնությունն է մաքուր օդը, անուշադրի սպիրտի գոլորշիների կարճատև ներշնչումը, թթվածինը, մուգ և քաղցր թեյը։
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Ածխածնի օքսիդներ» հոդվածին։ |
| ||||||
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 1, էջ 209)։ |
