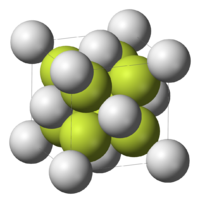
Կալցիումի ֆտորիդ
| Կալցիումի ֆտորիդ | |
|---|---|
 | |
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | կալցիումի ֆտորիդ |
| Քիմիական բանաձև | CaF₂ |
| Մոլային զանգված | 1,3E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 3,18 գ/սմ³ գ/սմ³ |
| Հալման ջերմաստիճան | 1418 °C[2] °C |
| Եռման ջերմաստիճան | 2533 °C և 2533,4 °C[2] °C |
| Գոյացան էնթալպիա | −1221 կՋ/մոլ կՋ/մոլ |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | 0,0015 (18 °C) գ/100 մլ |
| pKa | 1 |
| Բեկման ցուցիչ | 1,4328 |
| Բյուրեղային կառուցվածք | Խորանարդային համակարգ |
| Դասակարգում | |
| CAS համար | 7789-75-5 |
| PubChem | 24617 |
| EINECS համար | 232-188-7 |
| SMILES | [F-].[F-].[Ca+2] |
| ЕС | 232-188-7 |
| RTECS | EW1760000 |
| ChEBI | 23019 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Կալցիումի ֆտորիդը, քիմիական բանաձը՝ CaF2, ֆտորաջրածնական թթվի կալցիումական աղ է։ Անգույն բյուրեղային նյութ է, խտությունը՝ 3180 կգ/մ3, հալման ջերմաստիճանը՝ 1360 °C։ Ջրում գործնականորեն չի լուծվում[3]։
Ստացումը[խմբագրել | խմբագրել կոդը]
Բնության մեջ հանդիպում է ֆլյուորիտ միներալի տեսքով, որը պարունակում է մինչև 90-95% CaF2 և 3, 5-8% SiO2։ Ստացվում է կալցիումի քլորիդի լուծույթի վրա նատրիումի կամ ամոնիումի ֆտորիդով ազդելիս[4]։
CaCl2 + 2NH4F → CaF2 ↓ + 2NH4Cl
Լաբորատորիայում ստացվում է կալցիումի կարբոնատի և պլավիկյան թթվի ռեակցիայի հետևանքով։
CaCo3 + 2HF → CaF2 ↓ + CO2 ↑ + H2O
Ստացվում է նաև նոսր պլավիկյան թթվի և կալցիումի օքսիդի փոխազդելու հետևանքով[5]։
CaO + 2HF → CaF2 ↓ + H2O
Կալցիումի ֆտորիդ ստանում են նաև պարզ նյութերից։
Ca + F2 → CaF2
Կիրառություն[խմբագրել | խմբագրել կոդը]
Կիրառվում է որպես ելանյութ HF և ֆտորի այլ միացություններ ստանալու համար, ինչպես նաև մետալուրգիայում՝ որպես ֆլյուս, նաև հատուկ ապակիներ, կերամիկա, եմալ, օպտիկական և լազերային նյութեր ստանալու համար[6]։
Տես նաև[խմբագրել | խմբագրել կոդը]
Ծանոթագրություններ[խմբագրել | խմբագրել կոդը]
- ↑ 1,0 1,1 Fluorite
- ↑ 2,0 2,1 2,2 2,3 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ G. L. Miessler and D. A. Tarr “Inorganic Chemistry” 3rd Ed, Pearson/Prentice Hall publisher, ISBN 0-13-035471-6.
- ↑ Aigueperse, Jean; Mollard, Paul; Devilliers, Didier; Chemla, Marius; Faron, Robert; Romano, Renée; Cuer, Jean Pierre (2005), "Fluorine Compounds, Inorganic", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, p. 307, doi:10.1002/14356007.a11_307.
- ↑ Aigueperse, Jean; Paul Mollard, Didier Devilliers, Marius Chemla, Robert Faron, Renée Romano, Jean Pierre Cuer (2005), «Fluorine Compounds, Inorganic», Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a11_307
{{citation}}: CS1 սպաս․ բազմաթիվ անուններ: authors list (link) - ↑ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 5, էջ 185)։ |
