Կալիումի ֆերատ
| Կալիումի ֆերատ | |
|---|---|
 | |
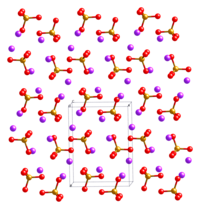 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | կալիումի Ֆերատ(VI) |
| Այլ անվանումներ | կալիումի ֆերատ, դիկալիումի ֆերատ |
| Քիմիական բանաձև | K₂FeO₄ |
| Ֆիզիկական հատկություններ | |
| Արտաքին տեսք | մուգ մանուշակագույն բյուրեղներ |
| Մոլային զանգված | 3,3E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 2.829 գ/սմ3 գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | >198 °C (քայքայվում է) °C |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | լուծելի է 1Մ KOH, փոխազդում է լուծիչների մեծ մասի հետ գ/100 մլ |
| Դասակարգում | |
| CAS համար | 13718-66-6 |
| PubChem | 53493006 |
| SMILES | [K+].[K+].O=[Fe-2](=O)(=O)=O |
| ChEBI | 57579260 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Կալիումի ֆերատ — անօրգանական միացություն է, որը հանդիսանում է ալկալիական մետաղ կալիումի և գոյություն չունեցող երկաթական թթվի աղ K2FeO4 բանաձևով։ Իրենից ներկայացնում է կարմրա-մանուշակագույն բյուրեղներ, որոնք լուծելի են սառը, հիմնայնացված ջրում։
Ստացում[խմբագրել | խմբագրել կոդը]
- փոշի երկաթի լուծմամբ կալիումի նիտրատի և հիդրօքսիդի հալույթում։
- Երկաթի անոդով կոնցենտրիկ կալիումի հիդրօքսիդի էլեկտրոլիզով։
- Երկաթի(III) օքսիդի ալկալու լուծույթում սուսպենզիայի օքսիդացմամբ, հալոգեններով։
Քիմիական հատկություններ[խմբագրել | խմբագրել կոդը]
- Քայքայվում է տաքացնելիս։
- փոխազդում է տաք ջրի հետ։
- փոխազդում է նոսր թթուների հետ։
- քայքայվում է ալկալիների հետ միահալելիս։
- Հանդիսանում է ուժեղ օքսիդիչ (ավելի ուժեղ քան պերմանգանատը)։
- Մտնում է փոխանակման ռեակցիաների մեջ։
Գրականություն[խմբագրել | խմբագրել կոդը]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.









